Kemikere syntetiserer molekylære kringler
Kredit:HIMS
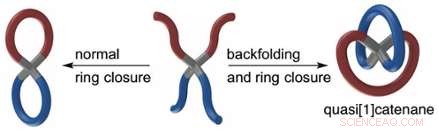
Kemikere ved University of Amsterdams Van 't Hoff Institute for Molecular Sciences har opdaget en ny klasse af molekyler. I denne uge melder de ind Naturkommunikation på deres syntesemetode, der fører til 'kvasi [1] catenanes':kringellignende molekyler bestående af to molekylringe 'modsat' koblet til et centralt carbonatom. Opdagelsen er et vigtigt skridt i retning af syntese af lassopeptider; nye molekyler med potentiel anvendelse som medicin.
Artiklen om naturkommunikation er kronen på en femårig forskningsindsats ved forskergruppen Synthetic Organic Chemistry hos professor Jan van Maarseveen, med ph.d. -studerende Luuk Stemers i spidsen. Han har udviklet en metode, der baner vej for syntese af såkaldte lassopeptider.
Lassopeptider er små proteiner, der, som deres navn angiver, består af en molekylær 'loop' omkring et molekylært 'reb'. De blev først isoleret fra bakterier ved begyndelsen af det nuværende århundrede. For nylig, DNA -analyse har afsløret, at lassopeptider er ret almindelige inden for bakterier. Deres biologiske funktion er at fungere som et antibiotikum mod andre mikroorganismer, hvilket gør dem til en potentiel ny klasse af antibiotika.
Det faktum, at syntetiske kemikere 15 år efter opdagelsen af lasso-peptider endnu ikke har været i stand til at udvikle en strategi, der fører til deres unikke molekylære arkitektur, understøtter kompleksiteten af disse molekyler.
Flaskehalsen her er, at rebet normalt er tæt bundet inden i løkken. Dette adskiller lassopeptider fra rotaxaner, for hvilke den skotske kemiker Sir Fraser Stoddart delte Nobelprisen for kemi sidste år. Under rotaxansyntese 'trækkes' rebet gennem løkken.
Da dette er umuligt for lassopeptidsyntese, Amsterdam -kemikerne brugte en anden tilgang, tvinger løkken til at lukke på det rigtige sted omkring rebet. Dette viste sig at være en ganske stor opgave. Til sidst lykkedes Luuk Stemers at skabe et molekylært stillads, der understøtter syntesen på en sådan måde, at sløjfen dannes korrekt omkring rebet.
Den nye syntesemetode er et stort skridt fremad på den syntetiske vej mod funktionelle lassopeptider. For at demonstrere kraften i metoden anvendte Stemers sit stillads for også at tvinge to ender af rebet til at danne en anden sløjfe.
Dette resulterede i syntesen af en helt ny klasse af kringellignende molekyler, som Amsterdam-forskerne opfandt quasi [1] catenanes. ('Rigtige' catenaner består af to løst sammenflettede molekylære ringlignende strukturer. Den franske kemiker Jean-Pierre Sauvage udviklede catenaner og delte Nobelprisen med Stoddard, og den hollandske kemiker Ben Feringa.)
Det næste trin i forskningsindsatsen fra Amsterdam -forskerne mod lassopeptidsyntese vil være at indføre letbrydelige bindinger i quasi [1] catenane, så ringene kan låses op.
 Varme artikler
Varme artikler
-
 Nye bæredygtige pulpteknologierKredit:Alberto Masnovo, Shutterstock Visionen for papirmasse- og papirindustrien er at reducere udledningen af kuldioxid markant og samtidig forbedre energi- og ressourceeffektiviteten. Derfor,
Nye bæredygtige pulpteknologierKredit:Alberto Masnovo, Shutterstock Visionen for papirmasse- og papirindustrien er at reducere udledningen af kuldioxid markant og samtidig forbedre energi- og ressourceeffektiviteten. Derfor, -
 Forskere udvikler værktøj til at hjælpe med udvikling, effektiviteten af brintdrevne bilerSkematisk indre funktion af elektroderne i en brændselscelle, og vigtigheden af nøgleparametre. Kredit:Heinz et al., 2021 Udbredt anvendelse af brintdrevne køretøjer frem for traditionelle elekt
Forskere udvikler værktøj til at hjælpe med udvikling, effektiviteten af brintdrevne bilerSkematisk indre funktion af elektroderne i en brændselscelle, og vigtigheden af nøgleparametre. Kredit:Heinz et al., 2021 Udbredt anvendelse af brintdrevne køretøjer frem for traditionelle elekt -
 Forskere skaber bioplast til fødevareemballage, som nedbrydes på to årEt team af forskere fra KTU Fakultet for Kemisk Teknologi har skabt en fuldt komposterbar emballage til fødevarer af bioplast. Kredit:KTU/Juste Suminaite En gruppe videnskabsmænd ved Kaunas Univer
Forskere skaber bioplast til fødevareemballage, som nedbrydes på to årEt team af forskere fra KTU Fakultet for Kemisk Teknologi har skabt en fuldt komposterbar emballage til fødevarer af bioplast. Kredit:KTU/Juste Suminaite En gruppe videnskabsmænd ved Kaunas Univer -
 Fejl i titreringseksperimenterTitrering er en følsom analysemetode, der giver dig mulighed for at bestemme en ukendt koncentration af et kemikalie i opløsning ved at introducere en kendt koncentration af et andet kemikalie. Flere
Fejl i titreringseksperimenterTitrering er en følsom analysemetode, der giver dig mulighed for at bestemme en ukendt koncentration af et kemikalie i opløsning ved at introducere en kendt koncentration af et andet kemikalie. Flere


