Adgang til DNA i cellernes kraftcenter til behandling af sygdom
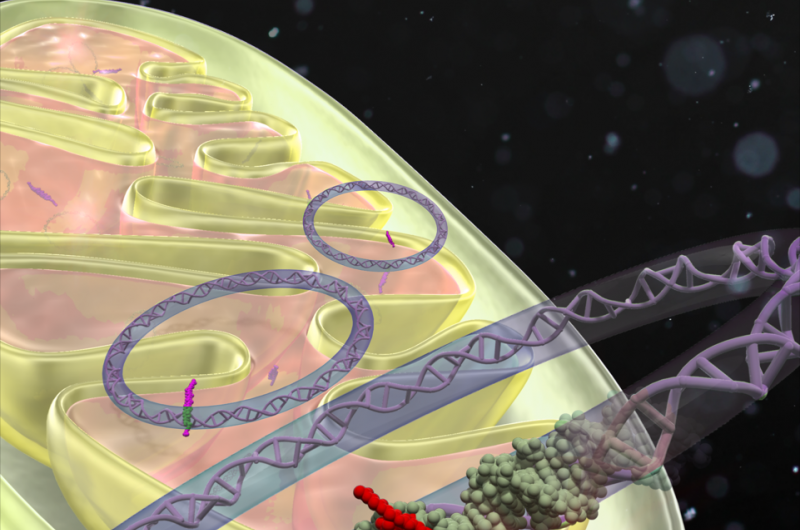
En skematisk illustration af en mitokondrie-specifik DNA-baseret syntetisk ligand, kaldet MITO-PIP'er, der selektivt læser en mål-DNA-sekvens og ændrer gentranskription. Kredit:Kyoto University iCeMS
For første gang, der er lavet en syntetisk forbindelse, der kan binde til DNA i cellernes energikraftværker, undertrykke et gen forbundet med nerve- og muskelsygdomme.
Pyrrol-imidazolpolyamider (PIP'er) er forbindelser, der kan læse specifikke DNA-sekvenser inde i levende celler og dæmpe sygdomsfremkaldende gener. De forhindrer proteiner, kaldet transkriptionsfaktorer, fra binding til specifikke dele af DNA-strengen, dermed undertrykke transkriptionen af DNA til RNA.
Det meste DNA findes i kernen. Men mitokondrier, cellens kraftværker, også vært for en lille mængde DNA. PIP'er er i stand til at krydse kernemembranen for at binde til nuklear DNA, men er ude af stand til at krydse mitokondriemembranen.
Et hold, ledet af Ganesh Pandian Namasivayam, fra Kyoto University's Institute for Integrated Cell-Material Science (iCeMS) lykkedes med at omdirigere PIP til at krydse mitokondriemembranen, så den kan få adgang til dets DNA og ændre gentransskription.
De opnåede denne komplekse bedrift ved at komplementere PIP med et 'mitochondria-penetrating peptide' (MPP), som er i stand til at overvinde mitokondriernes energibarriere. Den MPP-konjugerede PIP kaldet MITO-PIP blev designet til at blokere et specifikt bindingssted for mitokondriel transkriptionsfaktor A (TFAM). TFAM er afgørende for mitokondriemetabolisme og energisyntese, spiller en rolle i transskriptionen af et gen kaldet ND6, siger Takuya Hidaka, undersøgelsens første forfatter.
Holdet fandt, at en TFAM-hæmmende MITO-PIP selektivt læste en mitokondriel DNA-sekvens og forårsagede en 60% til 90% reduktion i ekspressionen af ND6, afhængig af den anvendte koncentration. Holdet mærkede derefter MITO-PIP'erne med et molekyle, der fluorescerer, når det udsættes for lys og, ved hjælp af specielle mikroskoper, bekræftet, at de lokaliserede sig inde i mitokondrierne uden at være til stede i kernerne af behandlede celler.
ND6 er forbundet med flere mitokondrielle lidelser, herunder Lebers arvelige optiske neuropati, som forårsager tab af centralt syn, mitokondriel myopati, muskelsvaghed, anfald og indlæringsvanskeligheder. Derfor, kemisk kontrol over sådanne sygdomsassocierede gener har klinisk potentiale i mitokondriel genterapi. "Vi planlægger at udvikle en avanceret version af MITO-PIP'er, der kun kan identificere og lokalisere inde i syge mitokondrier, " siger Ganesh.
"Vores proof-of-concept-studie giver en frisk platform, der åbner nye veje for DNA-baserede funktionelle ligander, der er i stand til at ændre mitokondriegenomet på en sekvensspecifik måde, " konkluderer hovedforskeren Hiroshi Sugiyama. Undersøgelsen blev offentliggjort i Journal of the American Chemical Society .
 Varme artikler
Varme artikler
-
 Jodidsalte stabiliserer biokatalysatorer til brændselscellerAlaa Oghli, Darren Buesen, Nicolas Plumeré (fra venstre) ønsker at gøre biokatalysatorer mere holdbare. Kredit: RUB, Marquard Ilt er den største fjende af biokatalysatorer til energiomdannelse. En
Jodidsalte stabiliserer biokatalysatorer til brændselscellerAlaa Oghli, Darren Buesen, Nicolas Plumeré (fra venstre) ønsker at gøre biokatalysatorer mere holdbare. Kredit: RUB, Marquard Ilt er den største fjende af biokatalysatorer til energiomdannelse. En -
 Supermagneter fra en 3-D printerForskerholdet er nu lykkedes med at fremstille miniaturiserede supermagneter ved hjælp af laserbaseret 3D-print. Kredit:IMAT – TU Graz Magnetiske materialer er en vigtig bestanddel af mekatroniske
Supermagneter fra en 3-D printerForskerholdet er nu lykkedes med at fremstille miniaturiserede supermagneter ved hjælp af laserbaseret 3D-print. Kredit:IMAT – TU Graz Magnetiske materialer er en vigtig bestanddel af mekatroniske -
 Test for livstruende næringsstofunderskud er lavet af bakteriers indvoldeZinkmangeltesten bliver lilla for at angive sundhedsmæssige zinkniveauer, men forbliver gul, når zinkniveauet er farligt lavt. Der blev ikke brugt blod til dette testdemobillede. Kredit:Georgia Tech /
Test for livstruende næringsstofunderskud er lavet af bakteriers indvoldeZinkmangeltesten bliver lilla for at angive sundhedsmæssige zinkniveauer, men forbliver gul, når zinkniveauet er farligt lavt. Der blev ikke brugt blod til dette testdemobillede. Kredit:Georgia Tech / -
 Gel dråber til regenerativ medicinCellebærende geler lavet af selvsamlende ultrakorte peptider kan producere menneskelignende væv, der kan bruges til regenerative terapier. Kredit:KAUST; Gustavo Ramirez Calderon Geldråber i mikrom
Gel dråber til regenerativ medicinCellebærende geler lavet af selvsamlende ultrakorte peptider kan producere menneskelignende væv, der kan bruges til regenerative terapier. Kredit:KAUST; Gustavo Ramirez Calderon Geldråber i mikrom
- NAFTAs død bringer Canada i straffeboksen, viser undersøgelse
- Miljømæssige bekymringer med natriumbicarbonat
- Hvad er forskellen mellem kovalente og ioniske obligationer?
- Undersøgelse:Tab af vand i tørke fik Sierra Nevada til at stige
- Naturbrande i Rusland spredte sig til centrale regioner
- Næsten 50 % af transportforureningsdødsfaldene er knyttet til diesel:undersøgelse


