Bioprintede vener afslører nye lægemiddelspredningsdetaljer
Kunstigt konstruerede menneskelige væv og organer er blevet udviklet med en række forskellige formål i tankerne, fra avanceret robotteknologi og nye materialer til lægemiddelscreening. Den præcision, der kræves af lægemiddelscreeningsapplikationer, stiller særligt store krav til, hvor præcist biomimetiske konstruktioner replikerer vævskarakteristika og adfærd, der er involveret i lægemiddelabsorption.
Et nyt fremskridt, offentliggjort i denne uge i tidsskriftet Biomikrofluidik , tilbyder nu muligheden for at konstruere vaskulariseret væv og efterligne in vivo lægemiddeladministration i 3-D bioprintet levervæv. Et virkelig internationalt samarbejde, med forskere tilknyttet Chile, Italien, Saudi Arabien, Korea og USA, udviklet denne relativt enkle levermodel for at tilbyde et mere præcist system til test af toksicitet af lægemidler.
"De fleste lægemiddeltestmodeller bruger et todimensionalt (2-D) monolags cellevæv, eller et 3D-væv, men uden dette netværk, "sagde Su Ryon Shin, en instruktør, der forsker på Harvard Medical School og en af undersøgelsens forfattere. "Vores kroppe er faktisk sammensat af en 3D-konstruktion med et vaskulært netværk, ikke består af [bare] enkeltceller. "
3D-strukturen efterligner bedre arkitekturen og funktionaliteten af komplekst humant væv sammenlignet med 2-D monolag af cellemodeller, på grund af deres forbedrede celle-celle-interaktioner og forbedrede cellulære funktioner. Disse 3D-strukturer giver en forbedret vævsmodel og leverer mere realistiske lægemiddelresponser end deres 2-D-modstykker. Denne nye vaskulariserede prøve giver større forudsigelsesevne for reelle toksicitetsniveauer, kroppen ville opleve.
Trykt med bio-blæk, der bruger offermikrokanalstilladser, det endelige endotelcellelagede kanalnetværk tillader observation af in vivo-effekter af lægemiddelabsorption uden egentlig at skulle foretage et in vivo-studie. I øvrigt, teknikken kan tilpasses forskellige celletyper for sandsynligvis at tilbyde patient-skræddersyet test af lægemiddeltoksicitet.
"Vi bruger menneskelige celler, og da vi udviklede denne teknik [gjorde vi det på en måde, der lader os] let ændre celletypen, ved hjælp af måske en patients primære celle eller deres endotelceller, og vi kan [potentielt] oprette en menneskespecialiseret vævsmodel, "Sagde Shin.
Selvom konstruktionen stadig er en ret forenklet version af det faktiske levervæv, denne vaskulære models nye kompleksitetsniveau har allerede hjulpet teamet med at opdage en vigtig mekanisme, som et monolags konstruktion aldrig kunne afsløre.
"Baseret på vores fund, endotellaget forsinker lægemiddeldiffusionsresponset, sammenlignet med uden endotelaget, "Shin sagde." De ændrer ikke nogen medicindiffusionskonstanter, men de forsinker permeabiliteten, så de forsinker [responsen], da det tager tid at passere gennem endotelaget. "
Shin planlægger især at fokusere fremtidig forskning på dette diffusionstrin, og hvordan det kan indstilles for at optimere lægemiddelabsorption. Mere generelt, gruppen håber, at dette kun er et tidligt skridt i udviklingen af mere komplekse og hurtigere bioprintede lægemiddeltestsystemer, såsom multi-organ-on-a-chip-enheder og prøve-modeller til andre organ- og vævssystemer. Kræftmedicinske behandlinger, for eksempel, kræver en forståelse af virkningerne på forskellige væv uden for selve kræftvævet, og ville have stor gavn af en sådan konstruktion.
 Varme artikler
Varme artikler
-
 Kæmpe elektronisk ledningsevneændring drevet af kunstig omskiftning af krystaldimensionalitetDen direkte 3D-2D strukturelle faseovergang blev induceret i (Pb1?xSnx)Se-legeringsepitaksiale film ved anvendelse af en ikke-ligevægtsvækstteknik. Reversibel gigantisk elektronisk egenskabsændring bl
Kæmpe elektronisk ledningsevneændring drevet af kunstig omskiftning af krystaldimensionalitetDen direkte 3D-2D strukturelle faseovergang blev induceret i (Pb1?xSnx)Se-legeringsepitaksiale film ved anvendelse af en ikke-ligevægtsvækstteknik. Reversibel gigantisk elektronisk egenskabsændring bl -
 Hvordan kemiske reaktioner beregnesKredit:Pixabay/CC0 Public Domain Et enkelt molekyle indeholder et væld af information. Det inkluderer ikke kun antallet af hver type af atomer, men også hvordan de er arrangeret og hvordan de knyt
Hvordan kemiske reaktioner beregnesKredit:Pixabay/CC0 Public Domain Et enkelt molekyle indeholder et væld af information. Det inkluderer ikke kun antallet af hver type af atomer, men også hvordan de er arrangeret og hvordan de knyt -
 Forskere finder en måde at gøre pultrudering hurtigereSkoltech-forskere finder en måde at gøre pultrusion hurtigere. Kredit:Timur Sabirov / Skoltech Et forskerhold fra Skoltech Center for Design, Manufacturing and Materials (CDMM) har undersøgt virkn
Forskere finder en måde at gøre pultrudering hurtigereSkoltech-forskere finder en måde at gøre pultrusion hurtigere. Kredit:Timur Sabirov / Skoltech Et forskerhold fra Skoltech Center for Design, Manufacturing and Materials (CDMM) har undersøgt virkn -
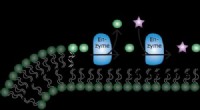 Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøstIllustrationen viser produktionen af forskellige cardiolipiner og fosfolipider ved inkorporering af miljøforbindelser som lipidhovedgruppe. Kredit:Marten Exterkate, Universitetet i Groningen Cel
Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøstIllustrationen viser produktionen af forskellige cardiolipiner og fosfolipider ved inkorporering af miljøforbindelser som lipidhovedgruppe. Kredit:Marten Exterkate, Universitetet i Groningen Cel
- Accuplacer Regler
- Vil vi vende det lille fremskridt, vi har gjort med hensyn til miljøretfærdighed?
- En skole, der værdsætter mangfoldighed, kan resultere i sundhedsmæssige fordele for farvede eleve…
- Strækbar keramik fremstillet af flammeteknologi
- Finjustering af todimensionale materialer
- Austrias Post Office under beskydning over datadeling


