Brug af syntetisk biologi til klamydiavacciner
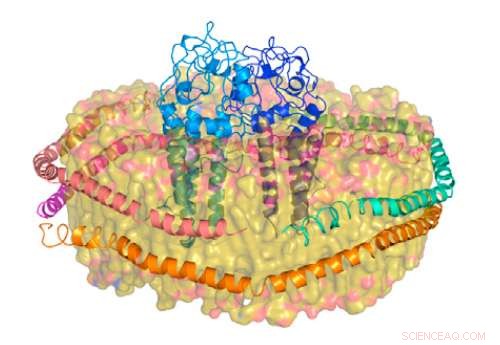
Membran-protein inkorporeret NLP. Kredit:Lawrence Livermore National Laboratory
Et tværfagligt videnskabeligt team ved Lawrence Livermore National Laboratory (LLNL) har gjort betydelige fremskridt med at udvikle en vaccine mod klamydia ved hjælp af syntetisk biologi, sponsoreret af en to-årig bevilling fra National Institutes of Health (NIH). De beskriver deres arbejde i et nyligt papir offentliggjort i Journal of Biochemistry ( JBC ):"Cellefri produktion af en funktionel oligomer form af et Chlamydia Major Ydre Membran Protein (MOMP) til vaccineudvikling." Dette arbejde blev udført i samarbejde med forskere ved University of California, Davis og vaccinationsgruppen hos Synthetic Genomics, Inc.
Klamydia er den mest almindelige smitsomme seksuelt overførte sygdom, forårsaget af den gram-negative bakterie Chlamydia trachomatis. Infektionen er ofte asymptomatisk, og når den ikke behandles, sygdommen kan forårsage alvorlige kroniske helbredsproblemer såsom permanent infertilitet, bækkenbetændelse og blindhed. Mens der findes antibiotikabehandlinger for klamydiainfektioner, tilbagefald af sygdommen hos samme patient er almindelige og vanskelige at behandle.
"Selvom antibiotika bruges til at behandle klamydia, tidlig screening og diagnose er nøglen til at forhindre komplikationer forbundet med langsigtede, ubehandlede infektioner, " sagde Wei He, en postdoc-forsker ved laboratoriet og den primære forfatter til papiret. "Det er vigtigt at bemærke, at personer behandlet med antibiotika er mere tilbøjelige til at blive smittet igen, så at arbejde hen imod en vaccine er et vigtigt skridt i behandlingen af dette omfattende folkesundhedsproblem."
Vacciner interagerer med patientens immunsystem for at producere aktiv immunitet, som giver beskyttelse mod sygdom. De indeholder antigener - normalt rensede proteiner, ligesom et større ydre membranprotein (MOMP) - som udtrykkes af patogenet af interesse. Ved vaccination, der udvikles et antigenspecifikt immunrespons, beskytte patienten mod infektion i virkeligheden. Et antigen, der med succes fremkalder dette immunrespons, kaldes 'immunogent'.
At skabe disse antigener i laboratoriet, imidlertid, kan være svært på grund af fejlfoldning af det afgørende, ekstremt komplekse proteiner, såsom den klamydia-specifikke MOMP, som denne forskningsgruppe målretter mod. Det arbejde, der diskuteres i gruppens tidsskriftsartikel, inkluderer en patentanmeldt teknik, der er unik for Lawrence Livermore (udviklet i samarbejde med Synthetic Genomics, Inc.), der har produceret højt udbytte, funktionelle, immunogen klamydia MOMP – et gennembrud inden for MOMP-produktionsteknikker.
"Vi er den første gruppe i verden, der bruger noget, der kaldes telodendrimer nanolipoprotein-partikler (tNLP'er) til at producere klamydiamembranproteiner i et cellefrit miljø, " sagde Matt Coleman, seniorforfatteren på papiret.
Den eneste anden vellykkede metode til at skabe MOMP'er i laboratoriet involverer at bruge E. coli som værtsceller, ændre deres DNA og bruge deres replikations- og translationsmaskineri til at producere MOMP, som derefter ekstraheres fra E. coli. Denne metode er langvarig og anstrengende, og formår ikke at producere et højt udbytte af korrekt foldede antigener.

Wei He i laboratoriet. Kredit:Lawrence Livermore National Laboratory
"Vores cellefri metode lader os tage de nødvendige værktøjer - de berigede ribosomer og det translationelle maskineri - ud af E. coli. Vi tilføjer derefter et par vigtige komponenter, såsom RNA-polymerase, i det væsentlige at skabe en 'one-pot'-mekanisme til proteinproduktion uden for en værtscelle, "Han sagde. "Vores unikke tNLP'er er selvsamlede i reaktionen for at producere en slags stillads, der understøtter MOMP-proteinet i en funktionel tilstand, selvom det ikke har et cellemiljø til at understøtte det. "
Denne cellefrie metode giver også forskere mulighed for at producere betydeligt større mængder af MOMP, fordi de ikke behøver at kæmpe med MOMP-toksicitet for værten E. coli-celle-fordi der slet ikke er nogen celle. Denne LLNL-pioner, en enkelt reaktionscellefri proces fjerner mange af de trin, der kræves i andre metoder til fremstilling af rekombinante proteiner forbundet med nanopartikler og tager mindre end en dag, hvorimod den anden, mindre effektive metoder kan tage op til tre dage.
"Med dette papir, vi har vist, at det er muligt at tage et potentielt terapeutisk protein, der har en meget kompleks struktur, og genskabe det begyndende med nogle simple biologiske komponenter, hvilket er en lovende udvikling på dette område, " tilføjede Coleman.
"Klamydia påvirker ikke kun over 131 millioner mennesker hvert år på verdensplan, " sagde Coleman, "men forskellige stammer af bakterien udgør også et stort problem for dyrehold. Infektionen har været særligt ødelæggende for koalaerne i Australien. Det har decimeret deres befolkning."
"Udvikler denne chlamydia -vaccine, sammen med den unikke metode, vi har til at fremstille disse antigener "on-demand" eller efter behov til brug i vacciner, kunne være en gave fra epidemien, der påvirker koalaerne, og har naturligvis også implikationer for behandling af sygdomme, der også påvirker mennesker - det er ikke kun klamydia, der er en lang række sygdomsantigener, som er notorisk svære at producere, " Han tilføjede.
Projektet har vigtige konsekvenser for udviklingen af en vaccine, ikke kun for klamydia, men andre bakterier og sygdomme, der også kræver svært at producere antigener for effektiv vaccination – herunder kræft.
Kræftimmunterapi er et spirende felt, der sigter mod at udnytte en patients immunsystem til at genkende og angribe de unikke proteiner, der er forbundet med kræftceller. Dette kan potentielt give en anden vej til effektiv kræftbehandling, og de tNLP-understøttede nanopartikler, kombineret med den cellefri metode, der er banebrydende af LLNL-gruppen (i partnerskab med Synthetic Genomics, Inc.), kunne give en mere effektiv og effektiv metode til at skabe antigener til denne slags cancervacciner.
Holdet går nu videre med forsøg med mus, og har set foreløbige positive resultater i at producere et immunogent respons, der efterlader dyr med en vis grad af beskyttelse mod infektion. De næste faser af forskningen involverer brug af den nye MOMP -produktionsproces til at konstruere den mest effektive vaccineformel. Projektet kunne i sidste ende producere et brugbart produkt, der kunne redde millioner af liv - både koala og mennesker.
 Varme artikler
Varme artikler
-
 Det er en fælde - Forskere identificerer processen, hvorved huller bliver fanget i ZnO nanopartikle…Argonne-forskere hjalp med at identificere den proces, hvorved huller bliver fanget i nanopartikler lavet af zinkoxid, et materiale af potentiel interesse til solenergianvendelser, fordi det absorbere
Det er en fælde - Forskere identificerer processen, hvorved huller bliver fanget i ZnO nanopartikle…Argonne-forskere hjalp med at identificere den proces, hvorved huller bliver fanget i nanopartikler lavet af zinkoxid, et materiale af potentiel interesse til solenergianvendelser, fordi det absorbere -
 Kunne et nyt 2-D-materiale tillade, at halvledere bliver ved med at blive mindre, stærkere bedre og…I modsætning til andre materialer med elektroner, der spredes i mange retninger (nederst til venstre), elektronerne i 2D -antimon (øverst til venstre) kan fås til at bevæge sig sammen på en ordnet måd
Kunne et nyt 2-D-materiale tillade, at halvledere bliver ved med at blive mindre, stærkere bedre og…I modsætning til andre materialer med elektroner, der spredes i mange retninger (nederst til venstre), elektronerne i 2D -antimon (øverst til venstre) kan fås til at bevæge sig sammen på en ordnet måd -
 At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de
At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de -
 Cementfabrikker kan sætte bremserne på global plastforureningFor at fjerne oceanerne for plastik, vi skal først af med plastik på land. Cementfabrikker i Asien kan være en del af løsningen. Kredit:Unsplash.com Håb midt i krisen. Overfyldte lossepladser i As
Cementfabrikker kan sætte bremserne på global plastforureningFor at fjerne oceanerne for plastik, vi skal først af med plastik på land. Cementfabrikker i Asien kan være en del af løsningen. Kredit:Unsplash.com Håb midt i krisen. Overfyldte lossepladser i As
- Tysk Wikipedia blev mørklagt i protest mod EU's ophavsretsplan
- Definition af middelværdi, median & tilstand
- Turbulente omgivelser satte scenen for spring i menneskelig udvikling og teknologi 320, 000 år side…
- Hvordan tilpasser lichens til den tempererede skov?
- Billede:Flevoland, det hollandske gigantiske landvindingsprojekt
- Sådan opretter du et citronbatteri videnskabsprojekt for at drive en calculator


