Kemikere foreslår en ny måde at syntetisere steroidanaloger på
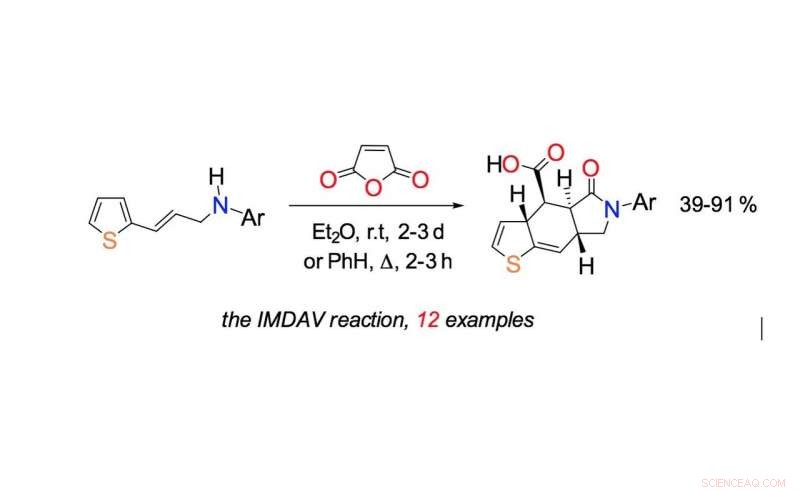
Intramolekylær Diels-Alder reaktion diskuteret i forskningen. Kredit:Fedor Zubkov
Forskere fra RUDN University og Ivan Franko National University of Lviv har fundet en måde at fremstille aromatiske ringe i organiske forbindelser i tre trin. Disse trin forløber successivt i én-beholder-betingelser og ved stuetemperatur. Nu analoger af hormoner, steroider, nogle sukkerarter, terpener og andre komplekse organiske stoffer kan syntetiseres hurtigere og under blødere forhold. Papiret blev udgivet i Tetrahedron Letters.
Steroider er stoffer med høj biologisk aktivitet. De omfatter antiinflammatoriske lægemidler (f. dexamethason), samt nogle hormoner. I øvrigt, steroider bruges til at producere vitamin D. Syv Nobelpriser blev uddelt mellem 1927 og 1975 for at studere disse vigtige stoffer. Syntetisering af steroider er ikke altid let, fordi de er baseret på et polysubstitueret tetracyklisk system. Kemikere fra RUDN University og deres ukrainske kolleger fandt en ny måde at fremstille steroider og andre stoffer, der indeholder seks-leddede ringe.
"Signaturmomentet for den syntetiske del er en tandemkaskade af reaktioner - reaktionerne forløber successivt i den samme kolbe under de samme reaktionsbetingelser:acylering af nitrogenatomet i start-3-thienylallylaminen med maleinsyreanhydrid, den intramolekylære Diels-Alder-reaktion og efterfølgende aromatisering af cycloadditionsadduktet, " siger Fedor Zubkov, adjunkt ved Institut for Organisk Kemi ved RUDN Universitetet.
Diensyntese (eller Diels-Alder-reaktionen) er en af de mest populære reaktioner i organisk kemi. Det involverer synkron dannelse af to sigma-dobbeltbindinger fra en dobbeltbinding af dienofil og to dobbeltbindinger af dien; hovedproduktet er en seksleddet ring med én dobbeltbinding. Otto Diels og Kurt Alder modtog Nobelprisen i 1950 for denne reaktion. Endnu en nobelpristager, Robert Woodward, blev inspireret og bandt sit liv med kemi efter at have læst om Diels-Alders reaktion. Senere, han vendte tilbage til det i sine studier flere gange. Mærkeligt nok, det var Robert Woodward, der grundlagde Tetraeder bogstaver tidsskrift, som udgav dette papir af russiske videnskabsmænd.
Den intramolekylære Diels-Alder-reaktion løber inde i ét molekyle. Med denne reaktion, komplekse molekyler inklusive seks-leddede ringe kan syntetiseres i et trin. Kemikere kan styre retningen af, hvordan reaktionen går, og de bindinger, der er involveret i den. Ved at regulere forholdene, de kan opnå præcis de nødvendige isomerer - stofferne med det samme antal atomer i molekylet, men med forskellige strukturformler. Forskerne fandt ud af, at vinylthiophener er velegnede til denne opgave.
"Vi kan se, at der dannes seksleddede cyklusser - de strukturelle motiver, der oftest findes i naturlige biologisk aktive forbindelser (alkaloider, sukkerarter, hormoner, steroider, terpener og andre). Som regel, interaktionen mellem dien og dienofil (bestanddelene af diensyntese) kræver ikke strenge temperaturforhold eller brug af katalysatorer, og de dannede produkter er meget rene og let isolerede, " kommenterer Fedor Zubkov.
tidligere, ifølge Fedor Zubkov, syntese af de lignende stoffer krævede en temperatur på 160 ° C for at producere den ønskede seksledede ring. I den nye undersøgelse, denne proces tager to til tre dage ved stuetemperatur. Reaktionen kører hurtigere i kogende benzen (ved 80 ° C) - det tager kun to timer. I dette tilfælde, imidlertid, slutproduktet er forurenet med urenheder. Processen kører i tre trin, og udbyttet af ønskede reaktionsprodukter er 39 til 91 procent, hvilket er nok til at syntetisere hormonlignende lægemiddelkomponenter og mange andre kemikalier hurtigere, mere bekvemt og mere effektivt end før.
Sidste artikelForskere syntetiserer analoger af stoffer, der bruges i lægemidler
Næste artikelLegeringer fra laserprinteren
 Varme artikler
Varme artikler
-
 Røntgen tomografi lader forskere se solid-state batterier oplade, udledningSolid-state batterier oplades og aflades i specialfremstillet hardware designet af Georgia Tech. En mindre, modificeret version af cellen vist her blev brugt til at afbilde disse materialer under cykl
Røntgen tomografi lader forskere se solid-state batterier oplade, udledningSolid-state batterier oplades og aflades i specialfremstillet hardware designet af Georgia Tech. En mindre, modificeret version af cellen vist her blev brugt til at afbilde disse materialer under cykl -
 Forskere udvikler ny behandling for knogleinfektion ved hjælp af kobberrigt glasimplantatUndersøgelsens første forfatter Emily Ryan, en nyligt kvalificeret ph.d.-studerende i RCSI Institut for Anatomi, afbilledet med prof Fergal OBrien, Professor i bioingeniør og regenerativ medicin i RCS
Forskere udvikler ny behandling for knogleinfektion ved hjælp af kobberrigt glasimplantatUndersøgelsens første forfatter Emily Ryan, en nyligt kvalificeret ph.d.-studerende i RCSI Institut for Anatomi, afbilledet med prof Fergal OBrien, Professor i bioingeniør og regenerativ medicin i RCS -
 Lagring af data som blandinger af fluorescerende farvestofferBlandinger af fluorescerende farvestofmolekyler, placeret små steder på en epoxyoverflade med en inkjetprinter, kode data. Kredit:American Chemical Society. Efterhånden som verdens behov for datal
Lagring af data som blandinger af fluorescerende farvestofferBlandinger af fluorescerende farvestofmolekyler, placeret små steder på en epoxyoverflade med en inkjetprinter, kode data. Kredit:American Chemical Society. Efterhånden som verdens behov for datal -
 Letvægtsperioden spiller en stor rolle i livet på JordenKredit:Panimoni/Shutterstock.com Selvom brint er letvægtsstoffet for de kemiske grundstoffer, det giver et rigtigt slag når det kommer til sin rolle i livet og dets potentiale som en løsning på no
Letvægtsperioden spiller en stor rolle i livet på JordenKredit:Panimoni/Shutterstock.com Selvom brint er letvægtsstoffet for de kemiske grundstoffer, det giver et rigtigt slag når det kommer til sin rolle i livet og dets potentiale som en løsning på no
- Forskere udvikler lasersystem, der genererer tilfældige tal ved ultrahurtige hastigheder
- Grafen:Potentialet af et kulstofatom-tykt vidundermateriale er ikke undsluppet industriens radar
- Ved floden, ocean, eller vind, klipper rundt på samme måde
- Små polypper redder koraller fra rovdyr og sygdomme
- Vådcellebatteri Vs. Tørcellebatteri
- Hvilke kølemidler er brændbare?


