Guldproteinklynger kunne bruges som miljø- og sundhedsdetektorer

Dette er en prøve af de glødende nanogold-proteinklynger, som lyser en lys rød. Kredit:Canadian Light Source
Peng Zhang og hans samarbejdspartnere studerer bemærkelsesværdigt, små selvsamlende klynger af guld og protein, der lyser en fed rød farve. Og de er nyttige:protein-guld nanoclusters kunne bruges til at opdage skadelige metaller i vand eller til at identificere kræftceller i kroppen.
"Disse strukturer er meget spændende, men er meget, meget svært at studere. Vi prøvede mange forskellige værktøjer, men ingen virkede, " siger Zhang, professor ved Dalhousie University.
Men synkrotron røntgenabsorptionsspektroskopi, eller XAS, udført på den canadiske lyskilde og dens partnerfacilitet CLS@APS, gav den nødvendige indsigt til at identificere den overraskende elegante struktur af de glødende protein guld nanoclusters.
"Synchrotron XAS er det perfekte værktøj, fordi det er meget fleksibelt, og kan give dig strukturel information om specifikke elementer, " han siger.
Strukturen af disse klynger havde længe været et spørgsmål i marken, dels på grund af deres potentielle anvendelser.
I laboratoriet, forskere har vist, at introduktion af andre metaller til proteinguldopløsningen kan slukke nanogoldens dristige glød, en egenskab, der kunne bruges til at opdage metalforurening i floder og andre vandområder. Hvor der fandtes metaller i en vandprøve, nanogold ville holde op med at gløde.
Endnu mere spændende er de potentielle sundhedsanvendelser for disse klynger.
Nanogold og proteiner passer naturligt til sundhedsteknologi, da proteiner er en naturligt forekommende del af den menneskelige krop, og guld er fuldstændig ugiftigt (derfor kan det bruges til at dekorere chokolade og kan findes i nogle typer snaps)
Sammen med de rigtige "detektor" eller "linker" proteiner, glødende nanogold kunne bruges til præcist at visualisere, for eksempel, kræftsvulster. Det rigtige linkerprotein ville simpelthen binde nanogolds til syge celler, som så kunne lokaliseres med et fluorescensmikroskop.
Alt dette er muligt på grund af nanogoldens evne til at gløde.
Guld som vi normalt kender det, i bulk, lyser ikke, eller lyser, under UV-lys. Tilføj protein som base for guld nanoclusters, og de vil lyse klart rødt under UV-lys. Faktisk, nanogolden er en million gange mere selvlysende end bulkguld.
Denne guldluminescens er muliggjort af dens specifikke struktur i proteinguld nanoclusters:hvad Zhang beskriver som en "smuk og overraskende struktur" af ti guldatomer, danner to sammenlåste ringe.
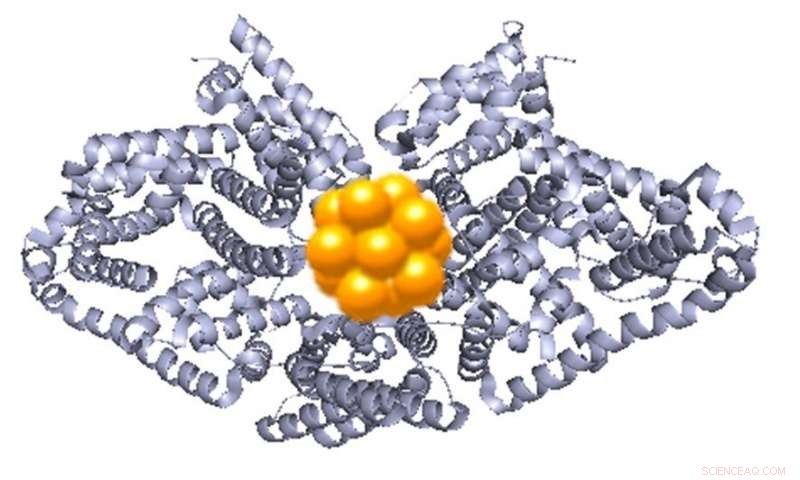
Protein-guld strukturen. Proteinet, som både bygger og holder guldklyngen på plads, er vist i gråt. Kredit:Canadian Light Source
Proteinet fungerer som et slags stillads, giver guldet en stærk struktur med styrker dets glød.
Disse klynger kan samles selv under de rigtige forhold, tilbyder en lav pris, lavenergiproduktionsmetode.
En typisk nanocluster er lavet med en præcis række af kemikalier, der er sat gennem specifikke trin, og kan resultere i forurening. Produktionen til disse klynger, derimod kunne ikke være enklere.
Zhangs team opvarmede en blanding af en kommerciel guldforbindelse og proteiner i vand op til kropstemperatur, 37C. Og efter 10-20 timer, dannede de selvlysende nanogold-klynger. Der kræves ingen andre trin for at skabe de selvlysende klynger.
Processen er kendt som grøn kemisk syntese, og fjerner den forurening, der ellers kunne være forbundet med disse klynger.
"Vi brugte synkrotronen til at følge, hvordan disse smukke strukturer dannes i proteinet, " siger Zhang. Proteinet fungerer i det væsentlige som en minireaktor, med sine cystein-aminosyrer, der knytter sig til guldmolekylerne og trækker dem i form. Disse eksperimenter blev udført af Daniel Chevrier, en ph.d. elev i Zhangs gruppe.
Holdet skabte også klynger mere konventionelt, at verificere deres teknik.
"Hvis du ikke bruger protein, ja du får en meget lignende struktur, men man ser ikke den stærke fluorescens. Hvad skete der?" spørger Zhang.
For at besvare dette spørgsmål, hans team sammenlignede konventionelt producerede og selvsamlede guldklynger, både med og uden proteiner.
Ved at bruge synkrotronen, de viste, at proteinet ikke kun muliggør selvsamling, men holder klyngerne på plads.
"I bund og grund fryser proteinet guldklyngen, så de ikke kan bevæge sig frit, og så kan du se den stærke fluorescens, " siger Zhang. En frit bevægende klynge, derimod drejninger og bevægelser, hvilket svækker fluorescensen.
"Vi er så begejstrede for disse nye resultater. Både guld og protein er meget interessante materialer, og når du kombinerer disse to, får du noget endnu mere interessant, og potentielt nyttige, " siger Zhang.
 Varme artikler
Varme artikler
-
 Nyt biomateriale kan beskytte mod skadelig strålingHumane celler behandlet med selenomelanin nanopartikler. Kredit:Northwestern University Pakning til det ydre rum? Her er en ting, du ikke vil glemme. Northwestern University-forskere har syntetis
Nyt biomateriale kan beskytte mod skadelig strålingHumane celler behandlet med selenomelanin nanopartikler. Kredit:Northwestern University Pakning til det ydre rum? Her er en ting, du ikke vil glemme. Northwestern University-forskere har syntetis -
 Forskning beskriver, hvordan ioner spiller en nøglerolle i at kontrollere slimhindeoverfladerKredit:KC Jones (Keck Graduate Institute) To nylige artikler fra Keck Graduate Institute (KGI) professor James Sterling og Shenda Baker, President og COO hos Synedgen, beskrive hvordan ioner inter
Forskning beskriver, hvordan ioner spiller en nøglerolle i at kontrollere slimhindeoverfladerKredit:KC Jones (Keck Graduate Institute) To nylige artikler fra Keck Graduate Institute (KGI) professor James Sterling og Shenda Baker, President og COO hos Synedgen, beskrive hvordan ioner inter -
 Sjældent jernmineral fra sten fundet i bløddyrstænderScanning elektronmikroskop billede af den forreste ende af radula med modne tænder. Kredit:Northwestern University Northwestern University forskere har, for første gang, opdagede et sjældent miner
Sjældent jernmineral fra sten fundet i bløddyrstænderScanning elektronmikroskop billede af den forreste ende af radula med modne tænder. Kredit:Northwestern University Northwestern University forskere har, for første gang, opdagede et sjældent miner -
 Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch
Et stof, der findes i brunkul, kan hjælpe med at bekæmpe viraAntiviral aktivitet af ti humusstofprøver (HS) blev vurderet mod flåtbåren encephalitisvirus reproduktion. For at afsløre mulige aktive komponenter i HS -prøver blev der søgt efter FTICR MS -data i Ch
- Undersøgelse finder store besparelser ved at fjerne dæmninger frem for reparationer
- Hvilke vejrforhold forårsager blizzards?
- Anvendelser af mikroskoper i retsmedicinsk videnskab
- Hvad forskerne fandt efter at have sigtet gennem støv i solsystemet
- Sådan finder du antallet af overskydende elektroner
- Leder efter CRISPR-schweizisk hærskniv


