Computermodel kan hjælpe forskere med at skille sig op, gensamle proteiner på kommando
Kredit:CC0 Public Domain
At skilles og finde sammen igen er altid svært at gøre, men for proteiner, det er næsten umuligt.
Imidlertid, en computerstyret algoritme kan hjælpe videnskabsmænd med at finde det helt rigtige sted at opdele et protein og derefter samle det til funktionalitet, ifølge et hold af biokemikere og biofysikere, der rapporterer deres resultater i dag (2. oktober) i Naturkommunikation . De tilføjer, at dette kunne være endnu et skridt - måske endda et dansetrin - mod at bruge kemiske og lyssignaler til at skabe nye medicinske behandlinger og biosensorer.
"Mit laboratorium er interesseret i at undersøge, hvordan cellulært liv fungerer ved at målrette mod de molekylære spillere, såsom proteiner og RNA, og i dette omfang, vi har udviklet værktøjer til at kontrollere disse spillere, " sagde Nikolay V. Dokholyan, G. Thomas Passananti professor, Penn State College of Medicine.
"Vi ønsker at få disse proteiner til at reagere med visse aktiviteter baseret på de lys-optogenetiske eller kemiske-kemogenetiske signaler, som vi leverer. Og, så, bare ved at skinne et lys eller tilføje et kemikalie, cellen begynder at bevæge sig, eller dans, eller hvad vi nu vil have dem til at gøre, baseret på det protein, vi kontrollerer."
Proteiner, som er foldet ind i komplekse 3-D strukturer, der ligner lidt et molekylært bånd slik, spiller roller i mange af kroppens vigtigste processer, herunder kommunikation mellem celler, opbygning af DNA og dannelse af antistoffer.
I fortiden, forskere fandt ud af, at de kunne opdele proteiner ved hjælp af lys og kemiske signaler, men at finde det præcise sted at foretage opdelingen var et spørgsmål om forsøg og fejl, hvilket ikke ville være praktisk til egentlige medicinske behandlinger og videnskabelige procedurer.
Processen med at splitte et protein er lidt som at dele et æble, men når folk deler æbler, har de normalt ingen intentioner om at samle stykkerne igen til et sundt æble, sagde Onur Dagliyan, forskningsstipendiat i neurobiologi, Harvard Medical School. Dagliyan arbejdede med Dokholyan og Klaus M. Hahn, Thurman Distinguished Professor of Pharmacology, University of North Carolina-Chapel Hill, på studiet.
"I dette særlige arbejde, vi forsøgte at etablere designprincipper for, hvordan man kan se på strukturen, eller sekvens af et protein og identificere de steder, der muliggør denne opdeling og gensamling, " sagde Dagliyan.
For at finde de bedste steder for proteinspaltninger, forskerne analyserede, hvordan flere proteiner blev delt i fortiden og brugte disse data til at skabe en matematisk model af proteinets struktur, eller fysisk scoringsmodel. Modellen, derefter, gav forskerne muligheden for at finde spots, der havde de bedste odds for en vellykket split.
Forskerne brugte algoritmen til at identificere opdelte steder på en række proteiner, herunder tyrosinkinase Lyn, guanosin nukleotid dissociationshæmmer og guanin udvekslingsfaktor.
Evnen til at opdele proteiner - og derefter gøre dem funktionelle igen - kunne have vidtrækkende konsekvenser, ifølge forskerne. Holdet, for eksempel, kunne se fremtidige anvendelser af denne teknik i terapier som CAR T-celleterapi. I CAR T-celleterapi, læger tager patienters immunceller fra deres krop og modificerer dem til at dræbe unormale celler, som kræftceller. Læger reinjicerer derefter disse modificerede celler i patienterne.
"Hvis vi vil levere noget - en konstrueret celle, eller stamceller, eller manipuleret bakteriecelle, for eksempel - til en krop til terapeutiske formål, Vi ønsker måske ikke, at de skal være aktive hele tiden, " sagde Dagliyan. "Du vil slukke dem og tænde dem, og folk i marken forsøger at finde måder at kontrollere disse proteiner på, bare for at kunne styre disse celler. Så, det er en mulighed, man kan se på."
Dagliyan tilføjede, at processen kunne bruges til at vedhæfte biosensorer til proteiner, som derefter kunne bruges til at hjælpe med at identificere ikke kun adfærden af et protein, men hvordan netværk af proteiner fungerer.
Spaltning af proteiner ville være et andet værktøj for medicinske forskere, sagde Dokholyan, som tilføjede, at hans laboratorium har hjulpet med at udvikle optogenetisk og chomogenetisk signalering af individuelle og grupper af proteiner.
Forskerne har lagt programmet online på spell.dokhlab.org.
"Dette er et værktøj, der grundlæggende automatiserer processen, så det ikke hjælper os med at kontrollere kun ét protein på denne måde, men det vil blive en hel platform – og denne platform er nu tilgængelig for videnskabsmænd over hele verden, " sagde Dokholyan.
 Varme artikler
Varme artikler
-
 Teamarbejde i et molekyleDr. Helmar Görls studerer enkeltkrystaller af nye forbindelser ved hjælp af et røntgendiffraktometer ved Institut for Uorganisk og Analytisk Kemi ved Friedrich Schiller University i Jena, Tyskland. Kr
Teamarbejde i et molekyleDr. Helmar Görls studerer enkeltkrystaller af nye forbindelser ved hjælp af et røntgendiffraktometer ved Institut for Uorganisk og Analytisk Kemi ved Friedrich Schiller University i Jena, Tyskland. Kr -
 Magnesiumlegering som et lettere alternativ til aluminiumslegeringOrtogonal rillespændingspresning og hurtig udglødning krymper dramatisk kornstørrelsen af AZ31 magnesiumlegering, hvilket resulterer i øget styrke og duktilitet ved stuetemperatur. Før behandling (v
Magnesiumlegering som et lettere alternativ til aluminiumslegeringOrtogonal rillespændingspresning og hurtig udglødning krymper dramatisk kornstørrelsen af AZ31 magnesiumlegering, hvilket resulterer i øget styrke og duktilitet ved stuetemperatur. Før behandling (v -
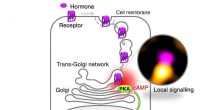 Hvordan receptorer for medicin virker inde i cellerNyopdaget mekanisme for GPCR-signalering ved trans-Golgi-netværket (TGN). Ved binding af et hormon (TSH), receptoren optages af cellen (internalisering) og transporteres til TGN, hvor det inducerer lo
Hvordan receptorer for medicin virker inde i cellerNyopdaget mekanisme for GPCR-signalering ved trans-Golgi-netværket (TGN). Ved binding af et hormon (TSH), receptoren optages af cellen (internalisering) og transporteres til TGN, hvor det inducerer lo -
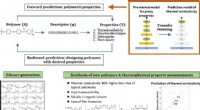 Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
Succesfuld anvendelse af maskinlæring i opdagelsen af nye polymererKredit:Tokyo Tech En fælles forskergruppe, herunder Ryo Yoshida (professor og direktør for Data Science Center for Creative Design and Manufacturing ved Institute of Statistical Mathematics [ISM],
- Team bruger 3D-print til at optimere gennemstrømningselektroder til elektrokemiske reaktorer
- Magnetiske nanopartikler kan forbrænde kræftceller
- Ny forskning tyder på, at robotter virker mere overbevisende, når de foregiver at være mennesker
- Fakta om tilpasning af duer til børn
- Madvaner hos gamle elefantslægtninge afsløret fra græsstumper, der sidder fast i deres tænder
- Sandsynligheder i genetik: Hvorfor er det vigtigt?


