Lifes biokemiske netværk kunne have dannet sig spontant på Jorden
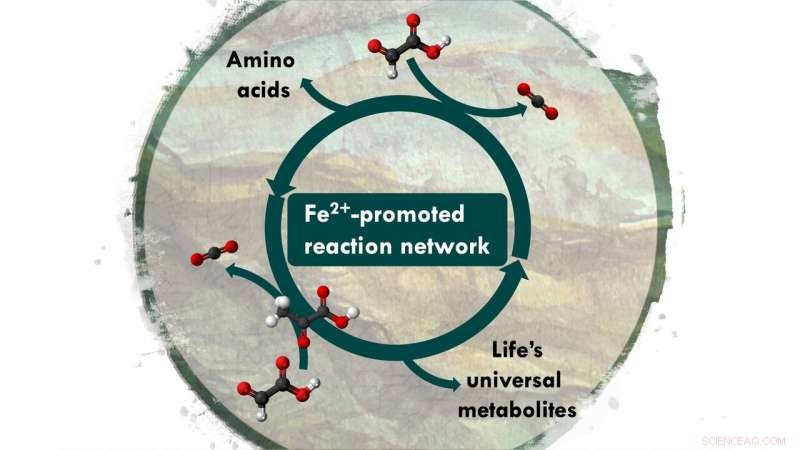
Syntese og nedbrydning af universelle metaboliske forstadier fremmet af jern Kredit:University of Strasbourg
Forskere i Strasbourg, Frankrig, har fundet ud af at blande to små biomolekyler, glyoxylat og pyruvat, i jern-salt-rigt vand producerer et reaktionsnetværk, der ligner livets kernebiokemi. Denne opdagelse giver indsigt i, hvordan kemi på den tidlige jord grundlagde udviklingen af det ældste liv. Undersøgelsen blev offentliggjort i tidsskriftet Natur .
Forskere, der undersøger livets oprindelse på Jorden, har længe kæmpet for at forklare, hvordan livets biokemi startede for over 4 milliarder år siden. Biokemi er organiseret omkring kun fem universelle metaboliske forstadier bygget på C, O og H - ligesom tung trafik i en stor metropol er organiseret omkring et par transitcentre. Hvorfor livet bruger de molekyler og kemiske reaktioner, det gør, blandt utallige alternativer, er et komplet mysterium.
En gruppe forskere ledet af prof. Joseph Moran ved universitetet i Strasbourg har brugt de sidste par år på at arbejde med oprindelsen til biologisk stofskifte. "Ideen om, at biologisk metabolisme havde en nært beslægtet kemisk forløber, der brugte lignende mellemprodukter og transformationer, er en attraktiv mulighed, "siger Moran. For nylig har gruppen genskabte en rent kemisk ækvivalent af AcCoA -vejen, et sæt reaktioner, der bruges af mikrober til at producere acetat (to carbonatomer) og pyruvat (tre carbonatomer) fra CO 2 . Bygningsmidler større end tre carbonatomer fra byggesten fremstillet af CO 2 var hvor fremskridt gik i stå. For at opnå sådanne bedrifter, livet er afhængigt af komplekse enzymer og en kemisk energibærer, ATP. Men både enzymer og ATP er komplekse strukturer, der ikke kunne have eksisteret på en livløs jord. Hvordan opbyggede livet så sin biokemi før enzymer og ATP?
Moran forklarer:"Gennembruddet kom fra at indse, at et kemisk stofskifte kan have fungeret på en lidt anden måde end det fungerer i livet i dag, samtidig bevare det store billede. "Teamet blev inspireret af den centrale rolle som en metabolisme med to kulstof, glyoxylat, i en model udgivet tidligere af teoretiske biolog Daniel Segrè. En anden anelse kom fra organiske kemikere Ram Krishnamurthy og Greg Springsteen, der rapporterede, at pyruvat (tre carbonatomer) og glyoxylat (to carbonatomer) let reagerer for at danne C-C-bindinger i vand. Kamila Muchowska, en postdoktor i Morans team og første forfatter til den aktuelle undersøgelse siger, "Vi blandede glyoxylat og pyruvat i varmt, jernholdigt vand og bemærkede, at det giver anledning til et reaktionsnetværk med over 20 biologiske mellemprodukter, herunder dem, der er så store som seks carbonatomer. "Netværket øger ikke kun kompleksiteten over tid, men det bryder også mellemprodukterne ned til CO 2 , ligesom livet gør. "Det livlignende kemiske system, der opnås på denne måde, ligner konceptmæssigt funktionen af biologisk anabolisme og katabolisme-ingen enzymer er nødvendige, tilføj bare jern, «siger Moran.
Som en del af undersøgelsen, forskerne testede, hvad der sker, hvis en kilde til nitrogen og en kilde til elektroner indføres i systemet. "Da vi tilføjede hydroxylamin og metallisk jern til forsøget, reaktionsnetværket producerede fire biologiske aminosyrer, "forklarer Sreejith Varma, medforfatter af undersøgelsen. Moran siger, "Interessant nok, i den genetiske kode, de samme fire aminosyrer har alle kodoner, der starter med G, understøtter ideer om, at stofskifte og den genetiske kode kan være opstået parallelt. "
Det nyopdagede reaktionsnetværk har så meget tilfælles med kendte biologiske cyklusser, at teamet undrer sig over, om Krebs- og glyoxylatcyklusserne kunne have haft en rent kemisk oprindelse. "Vi tror, at kemisk stofskifte kunne have opbygget forstadier til biologiske cyklusser på denne måde, før ATP og enzymer fandtes, "siger Muchowska. Strasbourg -forskerne er nu ivrige efter at se, hvordan reaktionsnetværket kan ændre sig som reaktion på forskellige elementer, og om det kan føre til genetikens molekyler.
 Varme artikler
Varme artikler
-
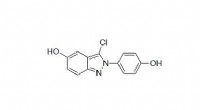 Kemisk forbindelse producerer gavnlig inflammation, remyelinisering, der kan hjælpe med at behandle…Kemisk struktur af indazolchlorid. Kredit:J. Katzenellenbogen, UIUC. Lægemidler til rådighed til behandling af multipel sklerose, en førende årsag til neurologisk handicap, der påvirker omkring 2,
Kemisk forbindelse producerer gavnlig inflammation, remyelinisering, der kan hjælpe med at behandle…Kemisk struktur af indazolchlorid. Kredit:J. Katzenellenbogen, UIUC. Lægemidler til rådighed til behandling af multipel sklerose, en førende årsag til neurologisk handicap, der påvirker omkring 2, -
 Makromolekylær orden i plastikrigetMange plastiklegetøj er lavet af polypropylen. Kredit:MIPT Et team af forskere ved Institute of Synthetic Polymer Materials of the Russian Academy of Sciences, MIPT og andre steder har bestemt, hv
Makromolekylær orden i plastikrigetMange plastiklegetøj er lavet af polypropylen. Kredit:MIPT Et team af forskere ved Institute of Synthetic Polymer Materials of the Russian Academy of Sciences, MIPT og andre steder har bestemt, hv -
 Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende
Avancerede biomaterialer med silkefibroin-bioaktivt glas til at konstruere patientspecifikke 3D-knog…Udvikling af avancerede hybride biomaterialer ved hjælp af tilpasset 3D-printsoftware. Kredit:RoboCAD, 3D blæk, LLC, doi:10.1088/1748-605X/aad2a9 Den komplekse arkitektur af knogler er udfordrende -
 Praktisk løsning til at forhindre korrosiv opbygning i nukleare systemerForskere har udtænkt en praktisk løsning til at forhindre ætsende ophobning i nukleare systemer. Billedet viser prøver af en standard reaktor zirconium legering med og uden vores CRUD-resistente belæg
Praktisk løsning til at forhindre korrosiv opbygning i nukleare systemerForskere har udtænkt en praktisk løsning til at forhindre ætsende ophobning i nukleare systemer. Billedet viser prøver af en standard reaktor zirconium legering med og uden vores CRUD-resistente belæg
- Forskere studerer organisk stof processer i rismarker
- Er der noget australierne gør ved klimaforandringer?
- Biobaserede erstatninger til fossilt brændstofplast
- Storbritannien spilder millioner af tons mad hvert år - her er hvordan vi kan ændre det
- Fællesskabet i kaotisk Jakarta går grønt for at bekæmpe fraflytning
- Udtrækning af skjult kvanteinformation fra en lyskilde


