Forskere udvikler teknologi til at fange tumorceller

Leidong Mao, venstre, med eleverne Sam Arsenault og Zhaojie Deng i et "rent" laboratorium sammenkrøbet ved siden af en bio-inkubator, der bruges til at dyrke kræftceller, som Mao bruger i sin forskning. Kredit:UGA
I stedet for at lede efter en nål i en høstak, hvad hvis du var i stand til at feje hele høstakken til den ene side, efterlader kun nålen tilbage? Det er den strategi, forskere ved University of Georgia College of Engineering fulgte i udviklingen af en ny mikrofluidisk enhed, der adskiller undvigende cirkulerende tumorceller (CTC'er) fra en prøve af fuldblod.
CTC'er bryder væk fra kræftsvulster og strømmer gennem blodbanen, potentielt føre til nye metastatiske tumorer. Isoleringen af CTC'er fra blodet giver et minimalt invasivt alternativ til grundlæggende forståelse, diagnose og prognose af metastatisk cancer. Men de fleste undersøgelser er begrænset af tekniske udfordringer med at fange intakte og levedygtige CTC'er med minimal forurening.
"En typisk prøve på 7 til 10 milliliter blod kan kun indeholde nogle få CTC'er, " sagde Leidong Mao, professor ved UGA's School of Electrical and Computer Engineering og projektets hovedefterforsker. "De gemmer sig i fuldblod med millioner af hvide blodlegemer. Det er en udfordring at få fingrene i nok CTC'er, så forskerne kan studere dem og forstå dem."
Cirkulerende tumorceller er også vanskelige at isolere, fordi inden for en prøve på et par hundrede CTC'er, de enkelte celler kan have mange karakteristika. Nogle minder om hudceller, mens andre minder om muskelceller. De kan også variere meget i størrelse.
"Folk sammenligner ofte at finde CTC'er med at finde en nål i en høstak, " sagde Mao. "Men nogle gange er nålen ikke engang en nål."
For hurtigere og mere effektivt at isolere disse sjældne celler til analyse, Mao og hans team har skabt en ny mikrofluidisk chip, der fanger næsten alle CTC i en blodprøve - mere end 99% - en betydeligt højere procentdel end de fleste eksisterende teknologier.
Holdet kalder sin nye tilgang til CTC-detektion for "integreret ferrohydrodynamisk celleadskillelse, " eller iFCS. De skitserer deres resultater i en undersøgelse offentliggjort i Royal Society of Chemistry's Lab on a Chip .
Den nye enhed kan være "transformativ" i behandlingen af brystkræft, ifølge Melissa Davis, en assisterende professor i celle- og udviklingsbiologi ved Weill Cornell Medicine og en samarbejdspartner på projektet.
"Læger kan kun behandle det, de kan opdage, " sagde Davis. "Vi kan ofte ikke opdage visse undertyper af CTC'er, men med iFCS-enheden vil vi fange alle undertyper af CTC'er og endda bestemme, hvilke undertyper der er de mest informative om tilbagefald og sygdomsprogression."
Davis mener, at enheden i sidste ende kan give læger mulighed for at måle en patients respons på specifikke behandlinger meget tidligere, end det er muligt i øjeblikket.
Mens de fleste bestræbelser på at fange cirkulerende tumorceller fokuserer på at identificere og isolere de få CTC'er, der lurer i en blodprøve, iFCS tager en helt anden tilgang ved at eliminere alt i prøven, der ikke er en cirkulerende tumorcelle.
Enheden, på størrelse med et USB-drev, virker ved at lede blod gennem kanaler, der er mindre i diameter end et menneskehår. For at forberede blod til analyse, holdet tilføjer magnetiske perler i mikronstørrelse til prøverne. De hvide blodlegemer i prøven binder sig til disse perler. Når blodet strømmer gennem enheden, magneter på toppen og bunden af chippen trækker de hvide blodlegemer og deres magnetiske perler ned ad en bestemt kanal, mens de cirkulerende tumorceller fortsætter ind i en anden kanal.
Enheden kombinerer tre trin i en mikrofluidisk chip, endnu et fremskridt i forhold til eksisterende teknologier, der kræver separate enheder til forskellige trin i processen.
"Det første trin er et filter, der fjerner store snavs i blodet, " sagde Yang Liu, en ph.d.-studerende i UGAs afdeling for kemi og avisens medforfatter. "Den anden del udtømmer ekstra magnetiske perler og størstedelen af de hvide blodlegemer. Den tredje del er designet til at fokusere resterende hvide blodlegemer til midten af kanalen og til at skubbe CTC'er til sidevæggene."
Wujun Zhao er avisens anden hovedforfatter. Zhao, en postdoc ved Lawrence Berkeley National Laboratory, arbejdet på projektet, mens han færdiggjorde sin doktorgrad i kemi på UGA.
"Succesen med vores integrerede enhed er, at den har evnen til at berige næsten alle CTC'er uanset deres størrelsesprofil eller antigenekspression, " sagde Zhao. "Vores resultater har potentialet til at give kræftforskningssamfundet nøgleinformation, som kan gå glip af nuværende proteinbaserede eller størrelsesbaserede berigelsesteknologier."
Forskerne siger, at deres næste skridt inkluderer automatisering af iFCS og gør det mere brugervenligt til kliniske omgivelser. De er også nødt til at sætte enheden igennem sine trin i patientforsøg. Mao og hans kolleger håber, at yderligere samarbejdspartnere vil slutte sig til dem og give deres ekspertise til projektet.
 Varme artikler
Varme artikler
-
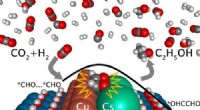 Katalysatorundersøgelse fremmer omdannelsen af kuldioxid til ethanolGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c03940 Et internationalt samarbejde mellem forskere har taget et væsentligt skridt hen imod realiseringen af en næsten grøn nul-net-kulstofteknologi, d
Katalysatorundersøgelse fremmer omdannelsen af kuldioxid til ethanolGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c03940 Et internationalt samarbejde mellem forskere har taget et væsentligt skridt hen imod realiseringen af en næsten grøn nul-net-kulstofteknologi, d -
 Kommer snart:En blodprøve for Alzheimers sygdom?Kredit:CC0 Public Domain Mennesker med symptomer på Alzheimers sygdom (AD), såsom kognitive vanskeligheder, adfærdsændringer og humørsvingninger, kan vente måneder eller endda år for at få en ende
Kommer snart:En blodprøve for Alzheimers sygdom?Kredit:CC0 Public Domain Mennesker med symptomer på Alzheimers sygdom (AD), såsom kognitive vanskeligheder, adfærdsændringer og humørsvingninger, kan vente måneder eller endda år for at få en ende -
 Video:Den eneste detox, du nogensinde får brug forKredit:The American Chemical Society Folk taler hele tiden om, hvordan de skal afgifte. Og der er en række virksomheder, der er en kilometer lang og venter på at sælge juicer og smoothies til dig
Video:Den eneste detox, du nogensinde får brug forKredit:The American Chemical Society Folk taler hele tiden om, hvordan de skal afgifte. Og der er en række virksomheder, der er en kilometer lang og venter på at sælge juicer og smoothies til dig -
 Meteoritnedslag kan skabe uventede former for silicaRøntgendiffraktionsbilleder, der viser den nye form for silica skabt ved at sende en intens stødbølge gennem en prøve af kvarts ved hjælp af en specialiseret gaspistol. Når røntgenstrålerne preller af
Meteoritnedslag kan skabe uventede former for silicaRøntgendiffraktionsbilleder, der viser den nye form for silica skabt ved at sende en intens stødbølge gennem en prøve af kvarts ved hjælp af en specialiseret gaspistol. Når røntgenstrålerne preller af


