Programmerbare sværmbotter hjælper med at lave fleksible biologiske værktøjer
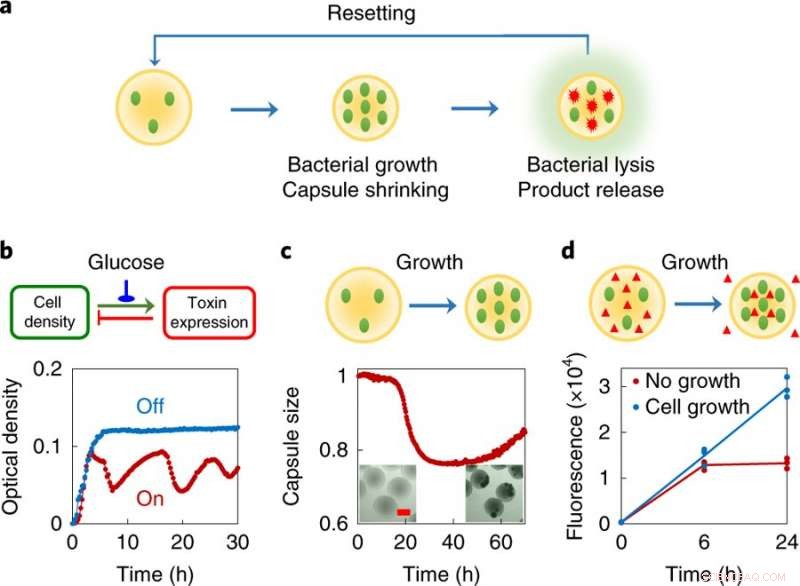
en, Design koncept, hver sværmbot består af en lille population af konstruerede bakterier indkapslet i polymere mikrokapsler. Disse bakterier er konstrueret til at undergå delvis lysering ved en tilstrækkelig høj lokal densitet. Omvendt det indkapslende materiale vil krympe som reaktion på det ændrede kemiske miljø forårsaget af cellevækst. Da bakterierne gennemgår programmeret autolyse, de frigiver intracellulære proteiner. De tværbundne polymere kapsler fanger de levende celler og stort affald indeni, og den tilsvarende krympning letter eksporten af proteinprodukter fra kapslerne. Systemet nulstilles ved at genopbygge med frisk medium. b, Programmeret autonom lysering af ePop -kredsløbet (øverst, kredsløb logik; bund, eksperimentelle data). En densitetsafhængig stigning i antallet af plasmidkopier fører til en stigning i ekspressionen af et toksin (E-proteinet fra fag φX174). Ved en tilstrækkelig høj koncentration, E -proteinet forårsager cellelyse, hvilket fører til et fald i celletæthed. Når den er tændt (rød kurve), kredsløbet førte til en reduceret kulturtæthed på MC4100Z1 (ePop) afbalanceret af vækst og reguleret drab. Med henblik på det overordnede systemdesign, generering af svingninger er ikke afgørende. Kredsløbet kan slukkes (blå kurve) ved at tilføje 1% glucose. Forsøget blev gentaget mere end tre gange uafhængigt med lignende resultater. c, Krympning af kapsler som reaktion på vækst af indkapslede bakterier (top, skematisk; bund, eksperimentelle data). MC4100Z1 (ePop/GFP) celler blev indkapslet i kitosankapsler og dyrket i M9. Alle data blev normaliseret til værdien på tidspunktet nul. Indsat, mikroskopibilleder af MSB'er efter 0 timer (venstre) og 48 timer (højre). Skala bar, 200 μm. Forsøget blev gentaget mere end tre gange uafhængigt med lignende resultater. d, Vækstmedieret kapsel krympning letter eksport af makromolekyler fra kapslerne (øverst, skematisk; bund, eksperimentelle data). MG1655 -celler og dextran -rhodamin (molekylvægt ≈ 70, 000 g mol − 1) blev indkapslet i kitosankapslerne og dyrket i M9. Kapsler blev behandlet med eller uden ampicillin (100 ug ml -1). Skrumpende kapsler, forårsaget af bakterievækst i fravær af antibiotika, førte til en ~ 2,25 gange stigning i rhodaminfluorescensen sammenlignet med ikke-krympende kapsler efter 24 timer, som indeholdt ikke-voksende bakterier (undertrykt af antibiotika). Forsøget blev udført i tre eksemplarer som uafhængige biologiske replikater, og dataene er vist som individuelle prikker, linjen angiver middelværdien. Kredit: Naturens kemiske biologi (2019). DOI:10.1038/s41589-019-0357-8
Biomedicinske ingeniører ved Duke University har udviklet en ny platform til at skabe biologiske lægemidler ved hjælp af specialfremstillede bakterier, der brister og frigiver nyttige proteiner, når de fornemmer, at deres kapsel bliver for overfyldt.
Platformen er afhængig af to hovedkomponenter:de konstruerede bakterier, kaldet "sværmboter, "der er programmeret til at fornemme tætheden af deres jævnaldrende i deres beholder, og biomaterialet, der begrænser sværmbotterne, en porøs kapsel, der kan krympe som reaktion på ændringer i bakteriepopulationen. Når det krymper, kapslen presser målrettede proteiner ud af de fangede bakterier.
Denne selvstændige platform kunne gøre det lettere for forskere at oprette, analysere og rense forskellige biologiske stoffer til brug i småskala bioproduktion.
Forskningen optrådte online 16. september i tidsskriftet Naturens kemiske biologi .
Bakterier bruges ofte til at producere biologiske stoffer, som er produkter som vacciner, genterapier og proteiner, der er skabt eller syntetiseret fra biologiske kilder. I øjeblikket, denne proces involverer en række sofistikerede trin, herunder celledyrkning, proteinisolering og proteinrensning, som hver især kræver en delikat infrastruktur for at sikre effektivitet og kvalitet. Til industriel drift, disse trin udføres i stor skala. Selvom dette hjælper med at producere store mængder af bestemte molekyler, denne opsætning er ikke fleksibel eller økonomisk levedygtig, når forskere skal producere små mængder af forskelligartet biologi eller arbejde i ressourcebegrænsede miljøer.
Den nye teknologi blev udviklet af Lingchong You, professor i biomedicinsk teknik ved Duke University, og en tidligere hertug postdoktoral forsker, Zhuojun Dai, nu lektor ved Shenzhen Institute of Advanced Technologies. I den nye undersøgelse, de viser, hvordan deres nye platform bruger kommunikation mellem sværmbotter og deres kapsel til at opnå alsidig produktion, analyse og oprensning af forskellige proteiner og proteinkomplekser.
I et tidligere bevis på koncept, Du og hans team konstruerede en ikke-patogen stamme af E. coli-bakterier til at producere en modgift mod antibiotika, når bakterierne nåede en vis tæthed. Disse sværmbotter blev derefter begrænset til en kapsel, som blev badet i antibiotika. Hvis en bakterie forlod kapslen, blev den ødelagt, men hvis den blev inde i beholderen, hvor befolkningstætheden var høj, den overlevede.
"Vores første undersøgelse viste hovedsageligt envejskommunikation, hvor cellerne kunne mærke miljøet i kapslen, men miljøet ikke reagerede på cellerne, "sagde du." Nu, vi har tovejskommunikation-de konstruerede sværmbotter kan stadig fornemme deres tæthed og deres indeslutning, men vi har introduceret et materiale, der kan reagere, når bakteriepopulationen inde i det ændrer sig. Det er som om de to komponenter taler til hinanden, og samlet giver de dig en meget dynamisk adfærd. "
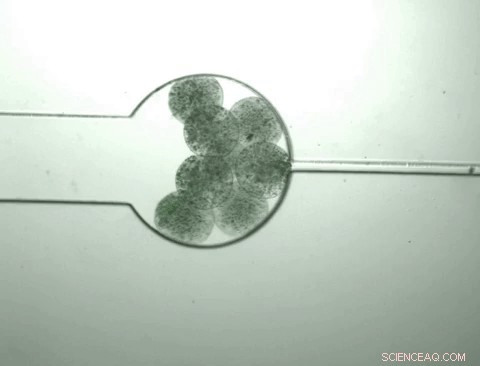
Kapsler indeholdende skræddersyede bakterier kaldet "sværmbotter" vokser og krymper som reaktion på det kemiske miljø, de indeholder. Sværmbotterne fornemmer, at deres egen befolkningstæthed har nået et vist niveau og åbner sig for at frigive deres indhold, herunder et protein, de er konstrueret til at fremstille. Kapslen krymper derefter, og processen genoptages, når næringsstoffer indføres. Kredit:Zhuojun Dai
Når befolkningen inde i kapslen når en vis densitet, bakterierne begynder at 'poppe', 'frigiver alt deres mobilindhold, herunder proteinproduktet af interesse. På samme tid, denne bakterievækst ændrer det kemiske miljø i kapslen, får det til at skrumpe. Når det krymper, det presser proteinet ud, der frigives fra de sprængende celler, mens bakterierne og celleaffald opbevares i kapslen.
Når proteinerne er indsamlet, forskere kan tilføje et næringsstofpåfyldning til fadet som et tegn på, at kapslerne kan forstørres. Dette nulstiller det indre miljø og gør det muligt for bakterierne at begynde at vokse igen, genstarte processen. Ifølge dig, denne cyklus kan gentages i op til en uge.
For at gøre fremgangsmåden nyttig til biofremstilling, holdet tilføjede kapslerne til en mikrofluidisk chip, som inkluderede et kammer for dem til at detektere og kvantificere hvilke proteiner der blev frigivet. Dette kunne erstattes med et rensningskammer for at forberede proteinerne til brug i biologiske stoffer.
"Det er en meget kompakt proces. Du behøver ikke elektricitet, og du behøver ikke en centrifuge for at producere og isolere disse proteiner, "sagde Du." Det gør dette til en god platform til biofremstilling. Du har evnen til at producere en bestemt type medicin i et meget kompakt format til en lav pris, og det er let at levere. Oven i købet, denne platform giver en nem måde at producere flere proteiner samtidigt. "
Ifølge dig, denne brugervenlighed har gjort det muligt for teamet at producere, kvantificere og rense mere end 50 forskellige proteiner i samarbejde med laboratoriet i Ashutoshi Chilkoti, Alan L. Kaganov Professor og formand for Institut for Biomedicinsk Teknik ved Duke. De har også undersøgt, hvordan deres platform kan forenkle oprettelsen af proteinkomplekser, som er strukturer lavet af flere proteiner.
På et proof-of-concept eksperiment for at producere en fedtsyresyntesebane fra flere enzymer, "vi var i stand til at bruge syv versioner af vores mikrobielle sværmboter, som hver var programmeret til at producere et andet enzym, "sagde du." Normalt, for at producere en metabolisk vej skal du balancere forsyningskæden, hvilket kunne indebære at opregulere ekspressionen af et enzym og nedregulere ekspressionen af et andet. Med vores platform behøver du ikke at gøre det, du skal bare indstille det korrekte forhold mellem sværmbotter. "
"Denne teknologi er utrolig alsidig, "sagde han." Det er en kapacitet, vi vil udnytte. "
 Varme artikler
Varme artikler
-
 Kemikere udvikler MRI-lignende teknik til at opdage, hvad der fejler batterierEt team af kemikere har udviklet en MRI-baseret teknik, der hurtigt kan diagnosticere, hvad der fejler visse typer batterier - fra at bestemme, hvor meget ladning der er tilbage til at opdage interne
Kemikere udvikler MRI-lignende teknik til at opdage, hvad der fejler batterierEt team af kemikere har udviklet en MRI-baseret teknik, der hurtigt kan diagnosticere, hvad der fejler visse typer batterier - fra at bestemme, hvor meget ladning der er tilbage til at opdage interne -
 Lab gør 4-D print mere praktiskFormskiftende materialer produceret på Rice University med en 3D-printermorph fra deres oprindelige form til en alternativ gennem ændringer i temperatur, elektrisk strøm eller stress. Dette eksempel v
Lab gør 4-D print mere praktiskFormskiftende materialer produceret på Rice University med en 3D-printermorph fra deres oprindelige form til en alternativ gennem ændringer i temperatur, elektrisk strøm eller stress. Dette eksempel v -
 Hvad sker der med en kogende temperatur, når trykket falder?Når det omgivende lufttryk falder, falder også den nødvendige temperatur til kogning af en væske. For eksempel tager det længere tid at fremstille nogle fødevarer i store højder, fordi vand koger ved
Hvad sker der med en kogende temperatur, når trykket falder?Når det omgivende lufttryk falder, falder også den nødvendige temperatur til kogning af en væske. For eksempel tager det længere tid at fremstille nogle fødevarer i store højder, fordi vand koger ved -
 Selvmontering, biomimetiske kompositter besidder usædvanlige elektriske egenskaberBiomimetiske kompositter fremstilles ved topologiske interaktioner, udvidelse af grænserne for de fysiske egenskaber, såsom elektrisk ledningsevne. Kredit:Mert Vural, Penn State Sommetider, bryde
Selvmontering, biomimetiske kompositter besidder usædvanlige elektriske egenskaberBiomimetiske kompositter fremstilles ved topologiske interaktioner, udvidelse af grænserne for de fysiske egenskaber, såsom elektrisk ledningsevne. Kredit:Mert Vural, Penn State Sommetider, bryde
- Gamle zirkonmineraler fra Mars afslører den uhåndgribelige indre struktur af den røde planet
- Sovende skønheder og betydningen af historiefortælling i videnskab
- Stjerneeksplosion i Jordens nærhed
- Næste skridt mod et gravitationsbølgeobservatorium i rummet
- Øger regnen Alkalinitet?
- Studerer kviksølvforurening i Virginias South River


