Overvågning af korrosion af bioresorberbart magnesium
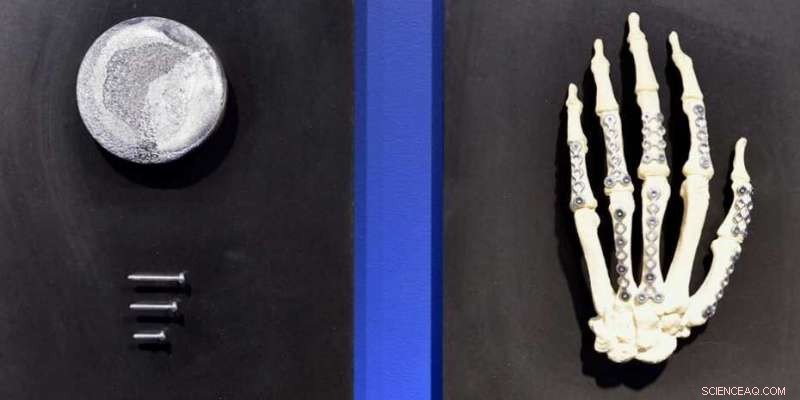
legeringer af magnesium, zink og calcium er velegnede til anvendelse som bioresorberbare implantater til at fikse brækkede knogler. Kredit:ETH Zürich
ETH-forskere har for nylig været i stand til at overvåge korrosionen af bioresorberbare magnesiumlegeringer på nanoskala over en tidsskala på få sekunder til mange timer. Dette er et vigtigt skridt i retning af præcist at forudsige, hvor hurtigt implantater resorberes af kroppen for at muliggøre udviklingen af skræddersyede materialer til midlertidige implantatapplikationer.
Magnesium og dets legeringer bliver i stigende grad anvendt i knoglekirurgi, især som osteosynteseimplantater såsom skruer eller plader, og som kardiovaskulære stents til at udvide forsnævrede koronare blodkar.
Dette letmetal har den store fordel, at det er bioresorberbart - i modsætning til opførselen af konventionelle implantatmaterialer såsom rustfrit stål, titanium eller polymerer. Dette gør en anden operation for at fjerne et implantat fra kroppen unødvendig. Derudover er det attraktivt, at magnesium fremmer knoglevækst og derfor aktivt understøtter helingen af brud.
Rent magnesium som sådan, imidlertid, er for blød til anvendelse i kirurgiske applikationer, og legeringselementer skal tilføjes for at styrke det. Disse er generelt sjældne jordarters grundstoffer såsom yttrium eller neodym. Imidlertid, disse elementer er fremmede for den menneskelige krop og kan ophobes i organer under implantatnedbrydning, med hidtil ukendte konsekvenser. De er derfor særligt utilstrækkelige til anvendelser inden for pædiatrisk kirurgi.
Implementering af en ny familie af legeringer
Forskere ved ETH Zürichs laboratorium for metalfysik og teknologi, ledet af professor Jörg F. Löffler, har derfor udviklet en ny familie af legeringer, der udover magnesium kun indeholder legeringselementerne zink og calcium, bevidst i indhold på mindre end 1 pct.
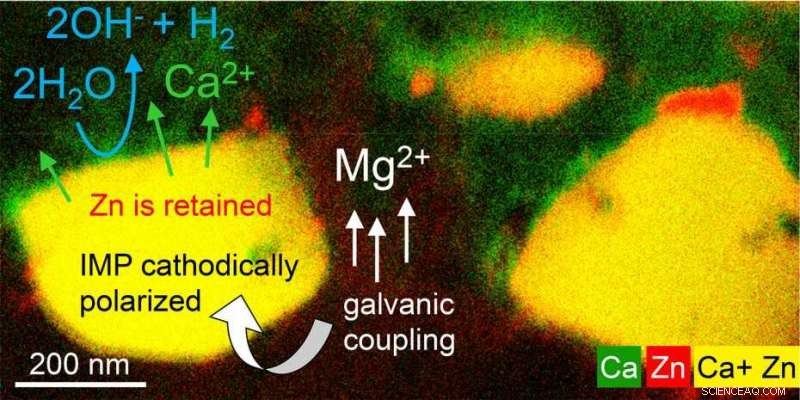
Ved at bruge banebrydende teknologier, ETH-forskere var i stand til at observere en tidligere udokumenteret aflegeringsmekanisme for magnesiumlegeringer. Kredit:Laboratory of Metal Physics and Technology / ETH Zürich
Zink og calcium er ligesom magnesium også biokompatible og kan resorberes af den menneskelige krop. Ved specifik behandling, de nye legeringer danner bundfald af varierende størrelse og tæthed, som er sammensat af alle tre elementer. Disse bundfald, som kun er nogle få snese nanometer store, er afgørende for at forbedre de mekaniske egenskaber og kan påvirke nedbrydningshastigheden.
På trods af disse lovende resultater, en vigtig faktor hindrer stadig en bred udbredelse af disse biokompatible magnesiumlegeringer i kirurgiske applikationer:for lidt er kendt om de mekanismer, hvorigennem disse materialer nedbrydes i kroppen under såkaldte fysiologiske forhold, og levedygtige forudsigelser om, hvor længe et sådant implantat vil forblive i den menneskelige krop, har således været umulige.
Overvågning af ændringer på nanoskalaen
Ved hjælp af analytisk transmissionselektronmikroskopi (TEM), Jörg Löffler og hans kolleger Martina Cihova og Robin Schäublin har nu formået at overvåge i detaljer de strukturelle og kemiske ændringer i magnesiumlegeringer under simulerede fysiologiske forhold over tidsskalaer fra få sekunder til mange timer, med hidtil uopnåede opløsninger på få nanometer. De har for nylig offentliggjort deres resultater i Avancerede materialer .
Ved hjælp af moderne TEM-teknologi, leveret af ETHs kompetencecenter "ScopeM, "Forskerne var i stand til at dokumentere en hidtil uobserveret aflegeringsmekanisme, der i væsentlig grad styrer bundfaldenes opløsning i magnesiummatrixen. De observerede - praktisk talt i realtid - hvordan calcium- og magnesiumioner opløses fra bundfaldene, når de er i kontakt med simuleret kropsvæske, mens zinkioner forbliver stabile og akkumuleres. Den resulterende løbende ændring i bundfaldenes kemiske sammensætning, kaldet "delegering, " genererer en dynamisk ændring i deres elektrokemiske aktivitet og accelererer nedbrydningen af magnesiumlegeringen generelt.
"Dette fund omstøder et fremherskende dogme, som antog, at bundfaldenes kemiske sammensætning i magnesiumlegeringer forbliver uændret, " siger Löffler. Den tidligere antagelse havde for det meste ført til falske forudsigelser vedrørende nedbrydningstider. "Den mekanisme, vi rapporterer, ser ud til at være universelt gyldig, og vi forventer, at det forekommer i både andre magnesiumlegeringer og andre aktive materialer, der indeholder intermetalliske præcipitater, " tilføjer Martina Cihova, ph.d.-studerende af Jörg Löffler og førsteforfatter til undersøgelsen.
Takket være den nye indsigt beskrevet ovenfor, det er nu muligt at designe magnesiumlegeringer, således at deres nedbrydningshastighed i kroppen bedre kan forudsiges og kontrolleres mere præcist. Dette er et vigtigt fremskridt i betragtning af, at magnesiumimplantater kan nedbrydes meget hurtigere hos børn end hos voksne, og at nedbrydningen af stenter skal være væsentligt langsommere end for knogleplader eller skruer. "Ved at indsamle detaljeret viden om de virkende korrosionsmekanismer, vi har taget et vigtigt skridt i retning af at skræddersy magnesiumlegeringer til forskellige patienter og medicinske anvendelser, " kommenterer Cihova. For at styrke forståelsen af korrosionsmekanismer yderligere, hendes postdoktorale forskning vil nu fokusere på elektronmikroskopiske analyser af in vivo magnesiumimplantater.
 Varme artikler
Varme artikler
-
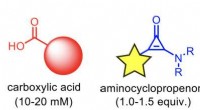 Lysinduceret modifikation af en carboxylsyre med en aminocyclopropenonFotoudløst modifikation af en carboxylsyre ved hjælp af en aminocyclopropenon. Reaktionen afsluttes på kort tid (5-10 min) selv ved lav koncentration (10-20 mM). Modifikationsreaktionen forløber i op
Lysinduceret modifikation af en carboxylsyre med en aminocyclopropenonFotoudløst modifikation af en carboxylsyre ved hjælp af en aminocyclopropenon. Reaktionen afsluttes på kort tid (5-10 min) selv ved lav koncentration (10-20 mM). Modifikationsreaktionen forløber i op -
 Spliceosomet - nu tilgængeligt i high definitionUCLA-forskere har løst strukturen i høj opløsning i en massiv mobilmaskine, spliceosome, udfylde det sidste store hul i vores forståelse af RNA -splejsningsprocessen, der tidligere var uklar. Kryo -e
Spliceosomet - nu tilgængeligt i high definitionUCLA-forskere har løst strukturen i høj opløsning i en massiv mobilmaskine, spliceosome, udfylde det sidste store hul i vores forståelse af RNA -splejsningsprocessen, der tidligere var uklar. Kryo -e -
 Ny katalysator opgraderer drivhusgas til vedvarende kulbrinterDr. Cao-Thang Dinh, venstre, og Dr. Md Golam Kibria demonstrerer deres nye katalysator. I et papir offentliggjort i dag i Science, deres team demonstrerede den mest effektive og stabile proces til at
Ny katalysator opgraderer drivhusgas til vedvarende kulbrinterDr. Cao-Thang Dinh, venstre, og Dr. Md Golam Kibria demonstrerer deres nye katalysator. I et papir offentliggjort i dag i Science, deres team demonstrerede den mest effektive og stabile proces til at -
 En effektiv måde at fjerne atrazin og dets biprodukter i overfladevandKredit:Institut national de la recherche scientifique Atrazin, meget brugt som ukrudtsmiddel, er kendt for at have skadelige virkninger på akvatiske dyreliv og udgør en risiko for menneskers sundh
En effektiv måde at fjerne atrazin og dets biprodukter i overfladevandKredit:Institut national de la recherche scientifique Atrazin, meget brugt som ukrudtsmiddel, er kendt for at have skadelige virkninger på akvatiske dyreliv og udgør en risiko for menneskers sundh
- Graphene og terahertz -bølger kan lede vejen til fremtidig kommunikation
- Hvad COVID-19 kan lære os om bæredygtighed
- Maskinlæringssystem kan hjælpe kritiske beslutninger i sepsisbehandling
- Superledende blæk opvarmer vandet øjeblikkeligt
- Forsvarskontrakten stiller Amazon op imod resten af Big Tech
- Børn i Sydasien hårdest ramt af luftforurening, siger undersøgelse


