Tethered chem combos kunne revolutionere kunstig fotosyntese

Klik på billedet for at downloade en version i høj opløsning.Brookhaven Lab kemiker Javier Concepcion og Lei Wang, en kandidatstuderende ved Stony Brook University, udtænkt et skema til samling af lysabsorberende molekyler og vandsplittende katalysatorer på en nanopartikelbelagt elektrode. Resultatet:produktion af brintgasbrændstof via kunstig fotosyntese og en platform til at teste forskellige kombinationer for yderligere at forbedre effektiviteten. Kredit:Brookhaven National Laboratory
Forskere ved det amerikanske energiministeriums Brookhaven National Laboratory har fordoblet effektiviteten af en kemisk kombination, der fanger lys og spalter vandmolekyler, så byggestenene kan bruges til at producere brintbrændstof. Deres studie, udvalgt som et American Chemical Society "Editors' Choice", der vil blive vist på forsiden af Journal of Physical Chemistry C , giver en platform til at udvikle revolutionerende forbedringer i såkaldt kunstig fotosyntese - en laboratoriebaseret efterligning af den naturlige proces, der sigter mod at generere ren energi fra sollys.
I naturlig fotosyntese, grønne planter bruger sollys til at omdanne vand (H 2 O) og kuldioxid (CO 2 ) til kulhydrater såsom sukker og stivelse. Energien fra sollys er lagret i de kemiske bindinger, der holder disse molekyler sammen.
Mange kunstige fotosyntesestrategier starter med at lede efter måder at bruge lys til at opdele vand i dets bestanddele, brint og ilt, så brinten kan senere kombineres med andre grundstoffer - ideelt set kulstoffet fra kuldioxid - for at lave brændstoffer. Men selv at få brintatomerne til at rekombinere som ren brintgas (H 2 ) er et skridt mod solcelledrevet produktion af rent brændstof.
For at opnå vandspaltning, forskere har udforsket en lang række lysabsorberende molekyler (også kaldet kromoforer, eller farvestoffer) parret med kemiske katalysatorer, der kan lirke vands meget stærke brint-iltbindinger fra hinanden. Den nye tilgang bruger molekylære "tethers" - simple kulstofkæder, der har en høj affinitet for hinanden - til at fastgøre kromoforen til katalysatoren. Forbindelserne holder partiklerne tæt nok sammen til at overføre elektroner fra katalysatoren til kromoforen - et vigtigt trin for at aktivere katalysatoren - men holder dem langt nok fra hinanden til, at elektronerne ikke hopper tilbage til katalysatoren.
"Elektroner bevæger sig hurtigt, men kemiske reaktioner er meget langsommere. Så, at give systemet tid til, at vandspaltningsreaktionen kan finde sted, uden at elektronerne bevæger sig tilbage til katalysatoren, du skal adskille disse afgifter, " forklarede Brookhaven Lab kemiker Javier Concepcion, der ledede projektet.
I den komplette opsætning, kromoforerne (bundet til katalysatoren) er indlejret i et lag af nanopartikler på en elektrode. Hver nanopartikel er lavet af en kerne af tindioxid (SnO2) omgivet af en titaniumdioxid (TiO) 2 ) skal. Disse forskellige komponenter giver effektive, trinvis shuttling af elektroner for at blive ved med at trække de negativt ladede partikler væk fra katalysatoren og sende dem derhen, hvor de er nødvendige for at lave brændstof.
Sådan fungerer det fra start til slut:Lys rammer kromoforen og giver en elektron nok et stød til at sende den fra kromoforen til overfladen af nanopartikler. Derfra bevæger elektronen sig til nanopartikelkernen, og derefter ud af elektroden gennem en ledning. I mellemtiden kromoforen, at have mistet en elektron, trækker en elektron fra katalysatoren. Så længe der er lys, denne proces gentager sig, sender elektroner, der strømmer fra katalysator til kromofor til nanopartikel til ledning.
Hver gang katalysatoren mister fire elektroner, den bliver aktiveret med en stor nok positiv ladning til at stjæle fire elektroner fra to vandmolekyler. Det skiller brint og ilt fra hinanden. Ilten bobler ud som en gas (i naturlig fotosyntese, sådan laver planter den ilt, vi indånder!), mens brintatomerne (nu ioner, fordi de er positivt ladede) diffunderer gennem en membran til en anden elektrode. Der rekombinerer de med elektronerne båret af ledningen for at producere brintgas - brændstof!
Bygger på erfaring
Brookhaven-teamet havde prøvet en tidligere version af denne kromofor-katalysator-opsætning, hvor det lysabsorberende farvestof og katalysatorpartikler var forbundet meget tættere med direkte kemiske bindinger i stedet for bindinger.
"Dette var meget svært at gøre, tage mange trin af syntese og oprensning, og det tog flere måneder at lave molekylerne, " sagde Concepcion. "Og præstationen var ikke så god til sidst."
I modsætning, ved at fæstne kulstofkæderne til begge molekyler kan de selv samles.
"Du dypper bare elektroden belagt med kromoforerne i en opløsning, hvori katalysatoren er suspenderet, og bindingerne på de to typer molekyler finder hinanden og forbinder, " sagde Stony Brook University kandidatstuderende Lei Wang, en medforfatter på det aktuelle papir og hovedforfatter på et papir offentliggjort tidligere på året, der beskrev selvsamlingsstrategien.
Det nye papir indeholder data, der viser, at systemet med forbundne forbindelser er betydeligt mere stabilt end de direkte tilsluttede komponenter, og det genererede dobbelt så meget strøm - antallet af elektroner, der strømmer gennem systemet.
"Jo flere elektroner du genererer fra lyset, der kommer ind, jo mere du har til rådighed til at generere brintbrændstof, " sagde Concepcion.
Forskerne målte også mængden af produceret ilt.
"Vi fandt ud af, at dette system, ved hjælp af synligt lys, er i stand til at opnå bemærkelsesværdige effektiviteter til lysdrevet vandopdeling, " sagde Concepcion.
Men der er stadig plads til forbedringer bemærkede han. "Det, vi har gjort til dette punkt, arbejder for at fremstille brint. Men vi vil gerne gå over til at lave kulbrintebrændstoffer af højere værdi." Nu hvor de har et system, hvor de nemt kan udveksle komponenter og eksperimentere med andre variabler, de er sat til at udforske mulighederne.
"Et af de vigtigste aspekter af dette setup er ikke kun ydeevnen, men nem montering, " sagde Concepcion.
"Fordi disse kombinationer af kromoforer og katalysatorer er så nemme at lave, og tøjrene giver os så meget kontrol over afstanden mellem dem, nu kan vi studere, for eksempel, hvad er den optimale afstand. Og vi kan lave eksperimenter, der kombinerer forskellige kromoforer og katalysatorer uden at skulle lave meget kompleks syntese for at finde de bedste kombinationer, " sagde han. "Alsidigheden af denne tilgang vil give os mulighed for at lave grundlæggende undersøgelser, som ikke ville have været mulige uden dette system."
 Varme artikler
Varme artikler
-
 Forskere udvikler vandtrykssensor, der kan udskrives påI tør tilstand (til venstre; her i en vandfri væske) er sensormaterialet lilla, i våd tilstand (f.eks. fra luftfugtighed) bliver den blå. De trykte emner vist her er hver cirka en centimeter brede. Kr
Forskere udvikler vandtrykssensor, der kan udskrives påI tør tilstand (til venstre; her i en vandfri væske) er sensormaterialet lilla, i våd tilstand (f.eks. fra luftfugtighed) bliver den blå. De trykte emner vist her er hver cirka en centimeter brede. Kr -
 Sådan konverteres AMU til muldvarpAtomenmasseenheder (AMU) og mol er to måder at måle et atom eller en anden partikel på. AMU er i det væsentlige en måling af vægten af et enkelt proton eller neutron. En mol, på den anden side, e
Sådan konverteres AMU til muldvarpAtomenmasseenheder (AMU) og mol er to måder at måle et atom eller en anden partikel på. AMU er i det væsentlige en måling af vægten af et enkelt proton eller neutron. En mol, på den anden side, e -
 Open source-software behandler hurtigt spektrale data, identificerer og kvantificerer lipidarter nø…LIQUID-grænsefladen. Kredit:Pacific Northwest National Laboratory Lipider spiller en nøglerolle i mange stofskiftesygdomme, herunder hypertension, diabetes, og slagtilfælde. Så det er vigtigt at h
Open source-software behandler hurtigt spektrale data, identificerer og kvantificerer lipidarter nø…LIQUID-grænsefladen. Kredit:Pacific Northwest National Laboratory Lipider spiller en nøglerolle i mange stofskiftesygdomme, herunder hypertension, diabetes, og slagtilfælde. Så det er vigtigt at h -
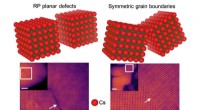 Når en defekt kan være gavnligVed hjælp af atomopløsningselektronmikroskopi, Arashdeep Singh Thind, en kandidatstuderende i Rohan Mishras laboratorium, studeret korngrænser i krystaller (se pile). Kredit:Washington University i St
Når en defekt kan være gavnligVed hjælp af atomopløsningselektronmikroskopi, Arashdeep Singh Thind, en kandidatstuderende i Rohan Mishras laboratorium, studeret korngrænser i krystaller (se pile). Kredit:Washington University i St
- Undersøgelse viser, at klimaforandringer dramatisk kan ændre skrøbelige bjerghabitater
- VENUS-konstruktion på vej til ORNLs nyeste neutron-billeddannelsesinstrument
- Dentin nanostrukturer-et super-naturligt fænomen
- Mere regn, mindre sne øger oversvømmelserne
- Hvad er den umiddelbare effekt af vedvarende energi?
- En kemisk kappe af usynlighed kan afsløre RNAs hemmeligheder


