Ny undersøgelse giver beviser for årtier gammel teori til at forklare vandets ulige adfærd

En ny undersøgelse fra Princeton University og Sapienza University of Rome giver stærke beviser for en kontroversiel teori om, at vand ved meget kolde temperaturer kan eksistere i to forskellige flydende former, den ene er mindre tæt og mere struktureret end den anden. Kredit:Foto af John Salatas, Creative Commons -licens
Vand, så almindeligt og så vigtigt for livet, handler på måder, der er ret forvirrende for forskere. For eksempel, hvorfor er is mindre tæt end vand, flyder frem for at synke som andre væsker gør, når de fryser?
Nu giver en ny undersøgelse stærkt bevis for en kontroversiel teori om, at vand ved meget kolde temperaturer kan eksistere i to forskellige flydende former, den ene er mindre tæt og mere struktureret end den anden.
Forskere ved Princeton University og Sapienza University i Rom gennemførte computersimuleringer af vandmolekyler for at opdage det kritiske punkt, hvor den ene flydende fase omdannes til den anden. Undersøgelsen blev offentliggjort i denne uge i tidsskriftet Videnskab .
"Tilstedeværelsen af det kritiske punkt giver en meget enkel forklaring på vandets underligheder, "sagde Princetons dekan for forskning Pablo Debenedetti, klasse af 1950 professor i teknik og anvendt videnskab, og professor i kemisk og biologisk teknik. "Fundet af det kritiske punkt svarer til at finde en god, enkel forklaring på de mange ting, der gør vand ulige, især ved lave temperaturer. "
Vandets særheder inkluderer, at når vandet afkøles, det udvides frem for at indgå kontrakt, derfor er frosset vand mindre tæt end flydende vand. Vand bliver også mere klemmeligt - eller komprimerbart - ved lavere temperaturer. Der er også mindst 17 måder, hvorpå dets molekyler kan arrangere, når de er frosset.
Et kritisk punkt er en unik værdi af temperatur og tryk, hvor to faser af stof bliver umulige at skelne, og det sker lige før materien omdannes fra den ene fase til den anden.
Vandets særheder forklares let ved tilstedeværelsen af et kritisk punkt, Sagde Debenedetti. Tilstedeværelsen af et kritisk punkt mærkes på stoffets egenskaber ret langt væk fra selve det kritiske punkt. På det kritiske punkt, komprimerbarheden og andre termodynamiske mål for, hvordan molekylerne opfører sig, såsom varmekapacitet, er uendelige.
Ved hjælp af to forskellige beregningsmetoder og to meget realistiske computermodeller af vand, holdet identificerede det væske -væske -kritiske punkt som liggende i et område på omkring 190 til 170 grader Kelvin (ca. -117 grader til -153 grader Fahrenheit) ved cirka 2, 000 gange atmosfæretrykket ved havets overflade.
Opdagelsen af det kritiske punkt er et tilfredsstillende trin for forskere, der er involveret i den årtier gamle søgen efter at bestemme den underliggende fysiske forklaring på vandets usædvanlige egenskaber. For flere årtier siden, fysikere teoretiserede, at kølevand til temperaturer under dets frysepunkt, samtidig med at det beholdes som en væske-en "superafkølet" tilstand, der forekommer i skyer i højder-ville udsætte vandets to unikke væskeformer ved tilstrækkeligt høje tryk.
For at teste teorien, forskere vendte sig til computersimuleringer. Eksperimenter med virkelige vandmolekyler har hidtil ikke givet entydige beviser for et kritisk punkt, dels på grund af tendensen til, at underkølet vand hurtigt fryser til is.
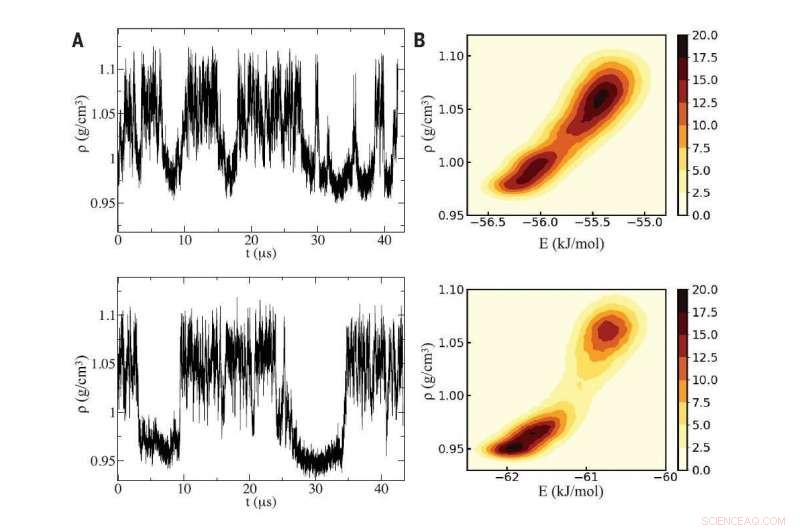
Fig A (til venstre):Ved hjælp af to forskellige computersimuleringer af vand (øverste og nederste panel), forskere opdagede svingninger i densitet, der er karakteristisk for underkølet vand, der oscillerer mellem to flydende faser, der adskiller sig efter densitet. Fig B (til højre):Simuleringerne afslørede et kritisk punkt mellem de to flydende faser, hvis forskellige tætheder stammer mikroskopisk i indtrængen af et ekstra vandmolekyle i det lokale miljø af et generisk centralt molekyle i højdensitetsvæsken. Kredit:Genoptrykt med tilladelse fra PG Debenedetti et al., Videnskab Vol 369, udgave 6501, DOI:10.1126/science.abb9796
Francesco Sciortino, professor i fysik ved Sapienza Universitet i Rom, gennemførte en af de første sådanne modelleringsundersøgelser, mens han var postdoktor i 1992. Denne undersøgelse, offentliggjort i tidsskriftet Natur , var den første, der antydede eksistensen af et kritisk punkt mellem de to flydende former.
Det nye fund er yderst tilfredsstillende for Sciortino, som også er medforfatter til det nye studie i Videnskab . Den nye undersøgelse brugte nutidens meget hurtigere og mere kraftfulde forskningscomputere og nyere og mere præcise modeller af vand. Selv med nutidens kraftfulde forskningscomputere, simuleringerne tog cirka 1,5 års beregningstid.
"Du kan forestille dig glæden, da vi begyndte at se de kritiske udsving nøjagtigt opføre sig som de skulle, "Sagde Sciortino." Nu kan jeg sove godt, fordi efter 25 år, min oprindelige idé er blevet bekræftet. "
I tilfælde af de to flydende former for vand, de to faser sameksisterer i urolig ligevægt ved temperaturer under frysepunktet og ved tilstrækkeligt høje tryk. Når temperaturen falder, de to flydende faser indleder tovtrækkeri, indtil en vinder ud, og hele væsken bliver lavdensitet.
I de simuleringer udført af postdoktorforsker Gül Zerze ved Princeton og Sciortino i Rom, da de bragte temperaturen langt under frysepunktet ned i det superkølede område, vandtætheden svingede vildt som forudsagt.
Nogle af vandets ulige adfærd ligger sandsynligvis bag vandets livgivende egenskaber, Sagde Zerze. "Livets væske er vand, men vi ved stadig ikke præcist, hvorfor vand ikke kan udskiftes med en anden væske. Vi tror, at årsagen har at gøre med vandets unormale opførsel. Andre væsker viser ikke den adfærd, så dette skal være forbundet med vand som livets væske. "
De to faser af vand opstår, fordi vandmolekylets form kan føre til to måder at pakke sammen på. I væsken med lavere densitet, fire molekyler klynge sig omkring et centralt femte molekyle i en geometrisk form kaldet et tetraeder. I væsken med højere densitet, et sjette molekyle presser sig ind, hvilket har den virkning, at den lokale tæthed øges.
Teamet opdagede det kritiske punkt i to forskellige computermodeller af vand. For hver model, forskerne udsatte vandmolekylerne for to forskellige beregningsmetoder til at lede efter det kritiske punkt. Begge tilgange gav fund af et kritisk punkt.
Peter Poole, professor i fysik ved St. Francis Xavier University i Canada, og en kandidatstuderende, da han samarbejdede med Sciortino og var medforfatter til papiret fra 1992 i Nature, sagde, at resultatet var tilfredsstillende. "Det er meget trøstende at få dette nye resultat, "sagde han." Det har været en lang og til tider ensom ventetid siden 1992 at se endnu et utvetydigt tilfælde af en væske-væske-faseovergang i en realistisk vandmodel. "
C. Austen Angell, Regents Professor ved Arizona State University, er en af pionererne inden for eksperimenter i 1970'erne med karakteren af underkølet vand. "Ingen tvivl om, at dette er en heroisk indsats i simulering af vandfysik med en meget interessant, og velkommen, konklusion, "sagde Angell, der ikke var involveret i denne undersøgelse, i en e -mail. "Som en eksperimentel med adgang til ligevægt (langsigtede) fysiske målinger på ægte vand, Jeg havde altid følt mig 'sikker' mod forudbetaling af computersimulatorer. Men de data, der præsenteres i det nye papir, viser, at dette ikke længere er sandt. "
 Varme artikler
Varme artikler
-
 Polymerbaseret optisk fiber til visualisering af materialespændingOvergang af outputspektrum af en fluorophor-doteret polymer optisk fiber ved påført belastning. Kredit:University of Electro Communications Fiberoptisk strain sensing er kendt for sin evne til at
Polymerbaseret optisk fiber til visualisering af materialespændingOvergang af outputspektrum af en fluorophor-doteret polymer optisk fiber ved påført belastning. Kredit:University of Electro Communications Fiberoptisk strain sensing er kendt for sin evne til at -
 Synkrotronstråling kaster lys over dannelsesmekanismen for aromatisk polyimid-precursorSynkrotronstråling kaster lys over mekanismen for dehydrogenativ kobling af dimethylphthalat katalyseret af palladium- og kobberkomplekser. Kredit:Institut for Anvendt Kemi, Ingeniørskolen, Tokyo Univ
Synkrotronstråling kaster lys over dannelsesmekanismen for aromatisk polyimid-precursorSynkrotronstråling kaster lys over mekanismen for dehydrogenativ kobling af dimethylphthalat katalyseret af palladium- og kobberkomplekser. Kredit:Institut for Anvendt Kemi, Ingeniørskolen, Tokyo Univ -
 Røntgenforsøg bidrager til undersøgelser af et lægemiddel, der nu er godkendt til at bekæmpe tu…En Pretomanid pille. Lægemidlet blev udviklet af nonprofit TB Alliance. Kredit:TB Alliance U.S. Food and Drug Administration har godkendt et nyt antibiotikum, i kombination med to eksisterende ant
Røntgenforsøg bidrager til undersøgelser af et lægemiddel, der nu er godkendt til at bekæmpe tu…En Pretomanid pille. Lægemidlet blev udviklet af nonprofit TB Alliance. Kredit:TB Alliance U.S. Food and Drug Administration har godkendt et nyt antibiotikum, i kombination med to eksisterende ant -
 Flertrins deformationsproces i højentropi-legeringer ved ultralave temperaturer afsløretDeformationsvej for CrMnFeCoNi HEA-prøve ved 15 K. Lodrette stiplede linjer er tegnet for at udpege ændringerne i deformationsadfærden:(1) Start af dislokationsglidning; (2) start af stablingsfejl; (3
Flertrins deformationsproces i højentropi-legeringer ved ultralave temperaturer afsløretDeformationsvej for CrMnFeCoNi HEA-prøve ved 15 K. Lodrette stiplede linjer er tegnet for at udpege ændringerne i deformationsadfærden:(1) Start af dislokationsglidning; (2) start af stablingsfejl; (3
- Hvordan man kender forskellen mellem en lodret asymptote og et hul i grafen for en rationel funktion…
- Forskere finder overraskende beviser for hurtige ændringer i Arktis
- Kontroversiel testflyvning med det formål at afkøle planeten aflyst
- Tasmanian Devil Facts for Kids
- Nordlys er et stort savn, Det siger en amerikansk rumfartsekspert
- Matryoshka -effekten:Forskere beskriver undervandsfænomen


