Team udvikler peptid, der gør lægemiddelresistente bakterier følsomme over for antibiotika igen
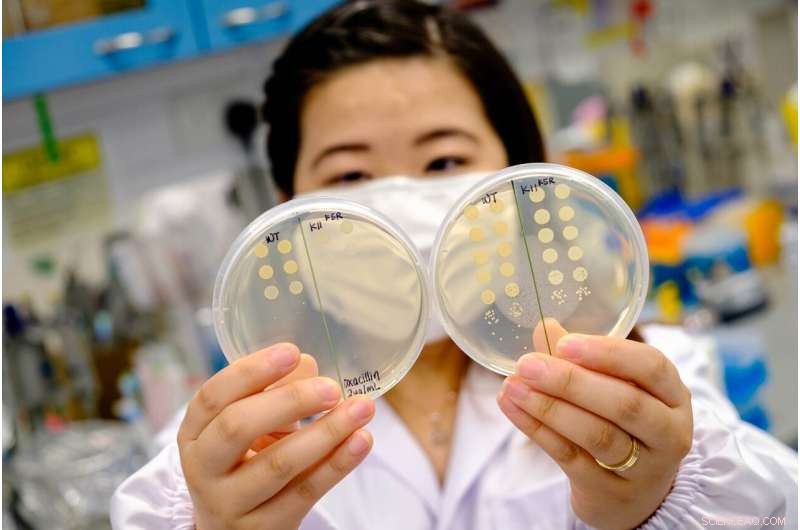
Den forbedrede styrke af det antimikrobielle peptid, når det bruges sammen med antibiotika, giver håb for udsigten til en kombinationsbehandlingsstrategi til at tackle visse antibiotika-tolerante infektioner. Kredit:NTU Singapore
Forskere ved Nanyang Technological University, Singapore (NTU Singapore) har udviklet et syntetisk peptid, der kan gøre multiresistente bakterier følsomme over for antibiotika igen, når de bruges sammen med traditionelle antibiotika. giver håb om udsigten til en kombinationsbehandlingsstrategi til at tackle visse antibiotika-tolerante infektioner.
På egen hånd, det syntetiske antimikrobielle peptid kan også dræbe bakterier, der er blevet resistente over for antibiotika.
Hvert år, anslået 700, 000 mennesker globalt dør af antibiotika-resistente sygdomme, ifølge Verdenssundhedsorganisationen. I mangel af nye terapier, infektioner forårsaget af resistente superbugs kan dræbe yderligere 10 millioner mennesker hvert år på verdensplan i 2050, overgå kræft. Antibiotikaresistens opstår i bakterier, når de kan genkende og forhindre lægemidler, der ellers ville dræbe dem, fra at passere gennem deres cellevæg.
Denne trussel accelereres af den udviklende COVID-19-pandemi, med patienter indlagt på hospitaler, der ofte får antibiotika for at holde sekundære bakterielle infektioner i skak, forstærker muligheden for, at resistente patogener kan dukke op og spredes.
NTU Singapore-holdet, ledet af lektor Kimberly Kline og professor Mary Chan, udviklet et antimikrobielt peptid kendt som CSM5-K5 omfattende gentagne enheder af chitosan, et sukker, der findes i skaldyrsskaller, og som har strukturel lighed med bakteriecellevæggen, og gentagne enheder af aminosyren lysin.
Forskerne mener, at chitosans strukturelle lighed med bakteriecellevæggen hjælper peptidet til at interagere med og indlejre sig i det, forårsager defekter i væggen og membranen, der til sidst dræber bakterierne.
Holdet testede peptidet på biofilm, som er slimede lag af bakterier, der kan klamre sig fast på overflader som levende væv eller medicinsk udstyr på hospitaler, og som er svære for traditionelle antibiotika at trænge igennem.
I både præformede biofilm i laboratoriet og biofilm dannet på sår hos mus, det NTU-udviklede peptid dræbte mindst 90 procent af bakteriestammerne på fire til fem timer.
I separate forsøg, når CSM5-K5 blev brugt sammen med antibiotika, som bakterierne ellers er resistente over for, flere bakterier blev dræbt sammenlignet med når CSM5-K5 blev brugt alene, tyder på, at peptidet gjorde bakterierne modtagelige for antibiotika. Mængden af antibiotika, der blev brugt i denne kombinationsbehandling, var også i en koncentration, der var lavere end det, der almindeligvis er ordineret.
Resultaterne blev offentliggjort i det videnskabelige tidsskrift ACS infektionssygdomme i maj.
Associate Professor Kimberly Kline, en hovedefterforsker ved Singapore Center for Environmental Life Sciences Engineering (SCELSE) ved NTU, sagde:"Vores resultater viser, at vores antimikrobielle peptid er effektivt, uanset om det bruges alene eller i kombination med konventionelle antibiotika til at bekæmpe multiresistente bakterier. Dets styrke øges, når det bruges sammen med antibiotika, genoprette bakteriernes følsomhed over for lægemidler igen. Vigtigere, vi fandt ud af, at de bakterier, vi testede, udviklede ringe eller ingen resistens mod vores peptid, gør det til en effektiv og gennemførlig tilføjelse til antibiotika som en levedygtig kombinationsbehandlingsstrategi, da verden kæmper med stigende antibiotikaresistens."
Prof Mary Chan, direktør for NTU's Center for Antimicrobial Bioengineering, sagde:"Mens indsatsen er fokuseret på at håndtere COVID-19-pandemien, Vi bør også huske, at antibiotikaresistens fortsat er et voksende problem, hvor sekundære bakterielle infektioner, der udvikler sig hos patienter, kan komplicere sagerne, udgør en trussel i sundhedsvæsenet. For eksempel, virale luftvejsinfektioner kan gøre det lettere for bakterier at trænge ind i lungerne, fører til bakteriel lungebetændelse, som almindeligvis er forbundet med COVID-19."
Hvordan det antimikrobielle peptid virker
Antimikrobielle peptider, som bærer en positiv elektrisk ladning, fungerer typisk ved at binde sig til de negativt ladede bakteriemembraner, forstyrre membranen og få bakterierne til at dø til sidst. Jo mere positivt ladet et peptid er, jo mere effektivt er det til at binde sig til bakterier og dermed dræbe dem.
Imidlertid, peptidets toksicitet over for værten øges også i takt med peptidets positive ladning – det beskadiger værtsorganismens celler, da det dræber bakterier. Som resultat, manipulerede antimikrobielle peptider til dato har haft begrænset succes, sagde lektor Prof Kline, som også er fra NTU School of Biological Sciences.
Peptidet designet af NTU-teamet, kaldet CSM5-K5, er i stand til at klynge sig sammen for at danne nanopartikler, når det påføres bakteriebiofilm. Denne klyngedannelse resulterer i en mere koncentreret forstyrrende effekt på bakteriecellevæggen sammenlignet med aktiviteten af enkeltkæder af peptider, hvilket betyder, at det har høj antibakteriel aktivitet, men uden at forårsage unødig skade på raske celler.
For at undersøge CSM5-K5's effektivitet alene, NTU-forskerne udviklede separate biofilm bestående af methicillin-resistente Staphylococcus aureus, almindeligvis kendt som MRSA superbug; en meget virulent multidrug-resistent stamme af Escherichia coli (MDR E. Coli); og vancomycin-resistent Enterococcus faecalis (VRE). MRSA og VRE er klassificeret som alvorlige trusler af US Centers for Disease Control and Prevention.
I laboratorieforsøg, CSM5-K5 dræbte mere end 99 procent af biofilmbakterierne efter fire timers behandling. I inficerede sår på mus, det NTU-udviklede antimikrobielle peptid dræbte mere end 90 procent af bakterierne.
Når CSM5-K5 blev brugt sammen med konventionelle antibiotika, NTU-holdet fandt ud af, at kombinationstilgangen førte til en yderligere reduktion af bakterierne i både laboratorieformede biofilm og inficerede sår hos mus sammenlignet med, når kun CSM5-K5 blev brugt, tyder på, at det antimikrobielle peptid gjorde bakterierne følsomme over for de lægemidler, de ellers ville være resistente over for.
Vigtigere, NTU-holdet fandt ud af, at de tre undersøgte bakteriestammer (MRSA, VRE og MDR E. coli) udviklede ringe eller ingen resistens mod CSM5-K5. Mens MRSA udviklede lav-niveau modstand mod CSM5-K5, dette gjorde MRSA mere følsom over for det lægemiddel, det ellers er resistent over for.
Prof Chan sagde:"At udvikle nye lægemidler alene er ikke længere tilstrækkeligt til at bekæmpe vanskelige at behandle bakterielle infektioner, efterhånden som bakterier fortsætter med at udvikle sig og overliste antibiotika/ Det er vigtigt at se på innovative måder at tackle vanskelige at behandle bakterielle infektioner forbundet med antibiotikaresistens og biofilm, som at tackle bakteriernes forsvarsmekanismer. En mere effektiv og økonomisk metode til at bekæmpe bakterier er gennem en kombinationsterapitilgang som vores."
Det næste skridt fremad for teamet er at undersøge, hvordan en sådan kombinationsterapi-tilgang kan bruges til sjældne sygdomme eller til sårforbinding.
Sidste artikelAt se kemiske reaktioner med musik
Næste artikelKemikere bygger naturlig anti-cancer forbindelse med en effektiv ny proces
 Varme artikler
Varme artikler
-
 Vendbar klæbrighed i tandcement er noget at smile afKredit:Institut for Organiske Biomaterialer, TMDU Alle, der har fået fyldt tandhuller, ved, at de bedste tandmaterialer bliver, hvor tandlægen lægger dem. Vedhæftningen af i øjeblikket tilgængel
Vendbar klæbrighed i tandcement er noget at smile afKredit:Institut for Organiske Biomaterialer, TMDU Alle, der har fået fyldt tandhuller, ved, at de bedste tandmaterialer bliver, hvor tandlægen lægger dem. Vedhæftningen af i øjeblikket tilgængel -
 Ny biologisk afledt metal-organisk ramme efterligner DNASION-19, en biologisk afledt MOF baseret på adenin blev brugt til at låse Thymin (Thy) molekyler i kanalerne gennem hydrogenbindingsinteraktioner mellem adenin og thymin. Ved bestråling, thyminmolekyl
Ny biologisk afledt metal-organisk ramme efterligner DNASION-19, en biologisk afledt MOF baseret på adenin blev brugt til at låse Thymin (Thy) molekyler i kanalerne gennem hydrogenbindingsinteraktioner mellem adenin og thymin. Ved bestråling, thyminmolekyl -
 Aflytning af australske edderkoppers hemmeligheder unikt silkeKurve-spindderkoppen i sin naturlige form med sin unikke hummerpottespind og silke, som nu er blevet afsløret som enestående robust. Kredit:Professor Mark Elgar, University of Melbourne Et interna
Aflytning af australske edderkoppers hemmeligheder unikt silkeKurve-spindderkoppen i sin naturlige form med sin unikke hummerpottespind og silke, som nu er blevet afsløret som enestående robust. Kredit:Professor Mark Elgar, University of Melbourne Et interna -
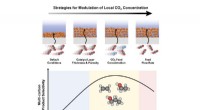 En ny strategi for optimal elektroreduktion af CO2 til højværdiprodukterTre strategier anvendt i denne undersøgelse til at modulere lokal CO2-koncentration i et katalysatorlag (øverst) og forholdet mellem lokal CO2-koncentration og selektiviteten for multi-carbon-produkte
En ny strategi for optimal elektroreduktion af CO2 til højværdiprodukterTre strategier anvendt i denne undersøgelse til at modulere lokal CO2-koncentration i et katalysatorlag (øverst) og forholdet mellem lokal CO2-koncentration og selektiviteten for multi-carbon-produkte
- Ni klimatippepunkter er nu aktive, advare videnskabsmænd
- Kortlægning af kemiske reaktioner på nanoskala inde i batterier i 3-D
- Bolsonaros holdning til coronavirus øger risikoadfærd i Brasilien
- Hvad er de mest almindelige årsager til udryddelse?
- Kinesisk fusionsværktøj skubber forbi 100 millioner grader
- Infanteritank Mark II A-12


