Kemikere bygger naturlig anti-cancer forbindelse med en effektiv ny proces
Kredit:CC0 Public Domain
Scripps Research kemikere Hans Renata, Ph.D., og Alexander Adibekian, Ph.D., har opdaget en måde til effektivt at skabe en syntetisk version af en værdifuld naturlig forbindelse kaldet cepafungin I, som har vist sig lovende som et middel mod kræft.
Igennem dette, de var i stand til at forstå, hvordan den bakterielle sekretion er i stand til at blokere et stykke molekylært maskineri kendt som et proteasom - en strategi, som mange eksisterende kræftmedicin bruger til at ødelægge tumorceller. De fandt ud af, at cepafungin I bandt til ikke ét men to steder på proteasomet, fremkalder et stærkt resultat. Deres rapport vises i journalen Cellekemisk biologi.
"Fordi cepafungin I er i stand til at engagere proteasomet på to måder, det giver mulighed for forstærkning af dens virkning, " siger Renata. "Vi viste, at denne forbindelse fremkalder mange lignende biologiske reaktioner nedstrøms som den FDA-godkendte kemoterapi bortezomib, samtidig med at de har visse kvaliteter, der kan udmønte sig i færre uønskede bivirkninger for patienterne."
At genskabe naturen
Cepafungin Jeg fascinerede først forskere på grund af dets anvendelighed som et svampedræbende stof, og senere som et lovende middel mod kræft. Det dræber celler ved at virke på proteasomet, som er ansvarlig for at rydde væk "skrald" produceret af celler. Når proteasomets funktion er blokeret, celler overvindes med deres affald og dør.
Men at lave nok af stoffet til at kunne studere dets aktivitet eller muliggøre dets endelige brug af en medicin har vist sig at være udfordrende, hovedsageligt på grund af dens komplekse molekylære struktur. Inden for kemi, videnskabsmænd søger at skabe den ønskede struktur i så få trin som muligt, hvilket medfører omkostnings- og tidsbesparelser. Men med komplekse forbindelser, det er ikke en nem opgave.
Scripps Research-teamet var i stand til at overvinde disse udfordringer og syntetisere forbindelsen i kun ni trin. Til sammenligning, en beslægtet forbindelse kendt som glidobactin A blev syntetiseret i 21 trin i 1992 - og det blev betragtet som et vartegn på det tidspunkt.
Holdet var i stand til at fremskynde processen ved at bruge visse enzymer, der muliggjorde konstruktion af en af forbindelsens vigtigste byggesten, en aminosyre. Derefter udviklede de andre kreative kemimetoder for at forenkle konstruktionen af andre dele af molekylet, inklusive en forgrenet lipiddel, som efterfølgende viste sig at bidrage til forbindelsens kraftige aktivitet.
"Vores tilgang sparede os for mange trin i at syntetisere den endelige forbindelse sammenlignet med at bruge klassiske kemiske tilgange, " siger Alexander Amatuni, en kandidatstuderende ved Scripps Research.
Et godt tegn for sikkerhed
Efter at have oprettet forbindelsen, kemikerne opdagede, at ud over at være usædvanligt selektive til at målrette to steder på proteasomet, det viste ikke nogen uønsket krydsreaktion med andre proteiner i celler, en funktion, der kunne gøre det til en bedre lægemiddelkandidat.
Tre proteasomhæmmere - bortezomib, carfilzomib og ixazomib - er allerede blevet godkendt af U.S. Food and Drug Administration til behandling af myelomatose. "Men den medicin har nogle potentielt alvorlige bivirkninger, og kræftceller kan udvikle resistens over for dem over tid, " siger medforfatter Adibekian, lektor i kemi ved Scripps Research. "Der er behov for alternativer, mere specifikke proteasomhæmmere."
Kandidatstuderende Anton Shuster bemærkede, at holdets opdagelser blev muliggjort af et tæt samarbejde mellem laboratorier med forskellig ekspertise
"Ved at kombinere de to komplementære teknologiske platforme - kemoenzymatisk syntese fra Renata-laboratoriet og kemoproteomik fra Adibekian-laboratoriet - var vi i stand til at lykkes, " siger Shuster. "At have muligheden for at arbejde med forskere med forskellig forskningsbaggrund er det, der gør arbejdet hos Scripps Research særligt spændende."
Fremadrettet, forskerne planlægger at fortsætte strukturstyret design af lignende molekyler med alternative strukturelle egenskaber i jagten på nyttige forbindelser med overlegen anti-cancer aktivitet.
De metoder, de udviklede, vil sætte dem i stand til at ændre forskellige dele af strukturen med relativ lethed, Amatuni siger, giver mulighed for yderligere undersøgelse af biologisk aktivitet. "Vægten på translationel forskning hos Scripps Research muliggør denne opdagelse, " siger Adibekian. "Vi er begejstrede for at udvikle molekylet yderligere."
 Varme artikler
Varme artikler
-
 Brug af kvanteprikker og en smartphone til at finde dræberbakterierForskerne Anwar Sunna (til højre) og Vinoth Kumar Rajendran med deres smartphone-aktiverede MRSA-detektor. Kredit:Sunna Lab En kombination af quantum dot nanoteknologi og et smartphonekamera kan s
Brug af kvanteprikker og en smartphone til at finde dræberbakterierForskerne Anwar Sunna (til højre) og Vinoth Kumar Rajendran med deres smartphone-aktiverede MRSA-detektor. Kredit:Sunna Lab En kombination af quantum dot nanoteknologi og et smartphonekamera kan s -
 Forskere udforsker brugen af nye materialer til at skabe mere effektive solcellerPostdoc-forsker Sarah Wieghold og adjunkt Lea Nienhaus leder efter måder at skabe bedre solceller, der kan bruge infrarødt lys. Kredit:Florida State University Et team af forskere fra Florida Stat
Forskere udforsker brugen af nye materialer til at skabe mere effektive solcellerPostdoc-forsker Sarah Wieghold og adjunkt Lea Nienhaus leder efter måder at skabe bedre solceller, der kan bruge infrarødt lys. Kredit:Florida State University Et team af forskere fra Florida Stat -
 Brug af bakterier til at skabe et vandfilter, der dræber bakterierKredit: Miljøvidenskab og -teknologi Mere end én ud af 10 mennesker i verden mangler grundlæggende adgang til drikkevand, og i 2025, halvdelen af verdens befolkning vil bo i vandstressede områd
Brug af bakterier til at skabe et vandfilter, der dræber bakterierKredit: Miljøvidenskab og -teknologi Mere end én ud af 10 mennesker i verden mangler grundlæggende adgang til drikkevand, og i 2025, halvdelen af verdens befolkning vil bo i vandstressede områd -
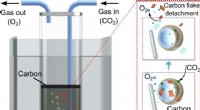 Flydende metal har vist sig at være en billig og effektiv CO2 -omformerUNSW -forskere har hjulpet med at vise, hvordan kuldioxid kan nedbrydes billigt og effektivt via en proces, der opløser fanget CO2 -gas i et opløsningsmiddel omkring nanopartikler af gallium. Kredit:U
Flydende metal har vist sig at være en billig og effektiv CO2 -omformerUNSW -forskere har hjulpet med at vise, hvordan kuldioxid kan nedbrydes billigt og effektivt via en proces, der opløser fanget CO2 -gas i et opløsningsmiddel omkring nanopartikler af gallium. Kredit:U
- I anmeldelse af 100 bedst sælgende billedbøger, kvindelige hovedpersoner er stort set usynlige
- Videnskabens viden skiftede langs religiøse, politiske tilhørsforhold
- Billede:Hubble ser stjerneglitter i et kosmisk tomrum
- Amazon var begejstret efter Premier League -debut
- Sjælden Groundcherry kunne snart være overalt,
- Assisterende rektorer har meget at tilbyde med hensyn til at fremme ligestilling og forbedre skoler,…


