Ny forskning viser begrænsningerne af koordination i kemi

Brint i sin plasmatilstand. Kredit:Alchemist-hp
En almindelig antagelse i kemi er, at koordinationstallet for en katalysators overflade bestemmer reaktiviteten af den reaktion, den katalyserer. Påfaldende nok, kemikere fra Leiden Universitet har nu bevist, at dette ikke er sandt for naturens mest simple kemiske reaktion:dissocieringen af brint. Forskerne formåede at måle de såkaldte absolutte reaktiviteter af denne reaktion, en første i videnskaben. De offentliggjorde deres resultater i Angewandte Chemie .
Hemmeligt våben
Katalysatorer er meget brugt i vores daglige liv, såsom platinkatalysatoren i din bils udstødning. Imidlertid, det er ofte ikke forstået, hvordan de præcist fungerer. Professor Ludo Juurlink og hans gruppe forsøger at ændre dette og har et hemmeligt våben til at gøre det:en buet platinoverflade. Sidste år, dette stykke udstyr gav dem to publikationer i førende tidsskrifter:i Videnskab de viste endelig, hvilken teoretisk model for reaktionen af brint på platin er korrekt og i PNAS de viste, hvordan ilt reagerer på platin. Nu, kemikerne brugte denne specielle platin til at ryste op i en vigtig etableret idé inden for kemi:koordination.
Zoomer ind på en katalysator
For at forklare dette, vi skal først tage et kig på overfladen af en katalysator, det er der kemiske reaktioner finder sted. Denne overflade består af atomer - platinatomer i denne undersøgelse - som er justeret på en bestemt måde. Hvert atom har et forskelligt koordinationsnummer, angiver hvor mange andre atomer der omgiver dette særlige atom. Hvis vi tager reaktionen af brint på platin som et eksempel, den generelle idé var som følger:koordinationsnummeret for atomerne på overfladen af platin bestemmer reaktiviteten over for molekylært brint.
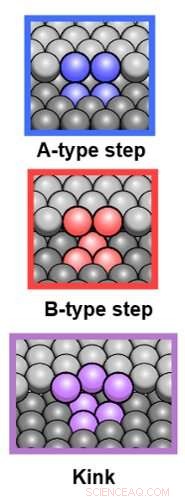
De tre typer af uregelmæssigheder. Kredit:Leiden Universitet
Leiden-holdet brugte to buede platinkrystaller til at teste denne hypotese. "Fordi platinoverfladen er buet, atomstrukturen ændrer sig meget gradvist langs overfladen, " forklarer gruppeleder Juurlink. "Du kan sammenligne denne struktur med en trappe, hvis trin mod kanterne bliver smallere og smallere. I midten, det ligner mere en balsal." Men hvorfor er det vigtigt? En katalysators overflade er ikke flad og glat, men uregelmæssig, med trin og knæk. Og netop ved disse uregelmæssigheder, kemiske reaktioner finder sted. Med den buede platin, forskerne efterligner denne effekt, samtidig med at man ved præcis, hvor mange trin eller knæk hver del af krystallen har. Dette gjorde det muligt for kemikerne at måle reaktiviteten af brint sammenlignet med tætheden af trin eller knæk på platin.
Skridt og knæk
"Vi identificerede tre typer uregelmæssigheder, " siger ph.d.-kandidat Sabine Auras, første forfatter til undersøgelsen. "Der er A-typen, B-typen, og den knækkede type." For hver type, hun målte reaktiviteten. Hvor overfladen har flere trin eller flere knæk, reaktiviteten øges. Indtil nu, intet nyt under solen. "Men vi fandt også ud af, at denne stigning er forskellig for hver type uregelmæssighed. Og denne forskel svarer ikke til, hvad man ville forvente med hensyn til koordinering." I stedet, holdet definerede tværsnit for interaktionen mellem brint og trin eller knæk, som er et vigtigt vartegn for andre forskere på området.
Langsigtet vision
Grundlaget for denne publikation i Angewandte Chemie blev lagt for fem år siden, da tidligere ph.d. kandidat Dima Bashlakov opdagede noget særligt, da han studerede en buet platinkrystal. "Jeg tror, vores forskning støtter ideen om, at videnskabsfinansiering aldrig bør fokusere på kortsigtede visioner eller kortsigtede resultater, " siger Juurlink. "Desværre nok, disse er begge aspekter, der synes så almindelige i forskningsapplikationer i disse dage."
Auras tilføjer:"Jeg forstår, at vi har et ansvar over for samfundet. Men med en vis grad af frihed, som langsigtet finansiering kan give, vi kan få helt unikke resultater. Man kan ikke altid styre videnskaben."
Sidste artikelForskere udvikler et strækkestativ til celler
Næste artikelAktiv læring fremskynder redox-flow batteri opdagelse
 Varme artikler
Varme artikler
-
 Oliefrøafgrøder affaldsprodukt giver forbindelser, der beskytter huden mod solenKredit:Oregon State University Meadowfoam, en indfødt Pacific Northwest-plante dyrket som en oliefrøafgrøde, er opstået som en potentiel ny kilde til beskyttelse mod solens skadelige virkninger på
Oliefrøafgrøder affaldsprodukt giver forbindelser, der beskytter huden mod solenKredit:Oregon State University Meadowfoam, en indfødt Pacific Northwest-plante dyrket som en oliefrøafgrøde, er opstået som en potentiel ny kilde til beskyttelse mod solens skadelige virkninger på -
 Acetone og Styrofoam ExperimentHvis du nogensinde har ønsket at gøre noget forsvinde som ved magi, er alt hvad du behøver, acetone og Styrofoam. Mens pyrofoam ikke nedbrydes hurtigt eller let, får acetone det til at synes at forsvi
Acetone og Styrofoam ExperimentHvis du nogensinde har ønsket at gøre noget forsvinde som ved magi, er alt hvad du behøver, acetone og Styrofoam. Mens pyrofoam ikke nedbrydes hurtigt eller let, får acetone det til at synes at forsvi -
 Det kræver to-en to-atomskatalysator, det vil sige - at lave ilt fra vandKredit:CC0 Public Domain Søgningen efter bæredygtige metoder til fremstilling af nye brændstoffer har bragt forskere tilbage til et af de mest rigelige materialer på jorden - rødligt jernoxid i fo
Det kræver to-en to-atomskatalysator, det vil sige - at lave ilt fra vandKredit:CC0 Public Domain Søgningen efter bæredygtige metoder til fremstilling af nye brændstoffer har bragt forskere tilbage til et af de mest rigelige materialer på jorden - rødligt jernoxid i fo -
 Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk
Forskere afslører dynamiske mekanismer af blyfri firdobbelte perovskit nanokrystallerEffektive selvlysende halogenid firdobbelt-perovskit nanokrystaller via trap-engineering til meget følsomme fotodetektorer. Kredit:YANG Bin og BAI Tianxin I de seneste år, blyfri halogenid perovsk
- Det sydlige Californiens embedsmænd erklærer vandforsyningsalarm
- Kemikalier af fremvoksende bekymringer kortlagt i tre store søer
- Kanariefugle i kulminen:Singapore-veer ringer handelsalarmklokker
- Befolkning er kun en del af historien om tornadoskader
- Vigtige buffere i levende systemer
- Forskere finder ud af, at naturbrande kan ændre arktiske vandskel i 50 år


