Lysfølsom trigger udviklet til den programmerede celledeling og død
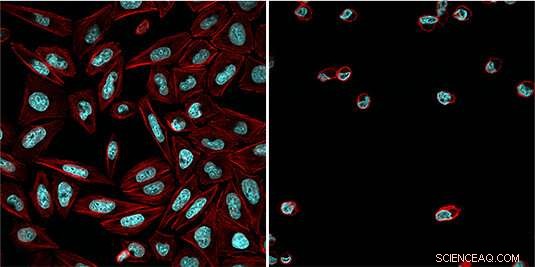
Celler behandlet med den lysafhængige hæmmer (actincytoskelet i rødt, DNA i blåt) efter udsættelse for blåt lys (højre) og uden at aktivere blålysstråling (venstre). Kredit:Esther Zanin
Ludwig Maximilian University-forskere har designet en lysfølsom hæmmer, der kan kontrollere celledeling og celledød-og giver en lovende tilgang til undersøgelser af essentielle cellulære processer og udvikling af nye tumorterapier.
Evnen til præcist at kontrollere biologiske og kemiske processer er et vigtigt element i både grundforskning og medicin. Lys repræsenterer en attraktiv stimulans i denne sammenhæng, da dens effekter kan præcist moduleres både rumligt og tidsmæssigt. Disse ønskelige egenskaber er grunden til, at udviklingen af lysstyrbare molekyler er blevet et så vigtigt mål for biologiske kemikere. Sådanne værktøjer lover at yde betydelige bidrag til belysning af grundlæggende cellulære funktioner, den detaljerede forståelse af medicinske lidelser og udformningen af nye terapeutiske strategier til bekæmpelse af dem. En gruppe forskere ledet af cellebiolog Esther Zanin ved LMU's Biocenter, i samarbejde med kemikeren Henry Dube (der flyttede i april i år fra LMU til universitetet i Erlangen-Nürnberg) nu har udviklet en lysfølsom kemisk hæmmer, der tillader dem at kontrollere to grundlæggende cellulære processer, celledeling og celledød, med lys.
Celledeling er en vital og yderst kompleks proces. Det er derfor underlagt stram regulering for at sikre, at cellerne kun deler sig på det rigtige tidspunkt og fejlfrit. Defekte celler elimineres ved programmeret celledød (også kendt som "apoptose"). Både korrekt celledeling og bortskaffelse af defekte celler afhænger af en molekylær maskine kaldet proteasomet, som specifikt nedbryder cellulære proteiner, der enten er beskadigede eller ikke længere er nødvendige.
"Vi har nu ændret en etableret og alsidig kemisk hæmmer af proteosomet ved at tilføje en lysfølsom beskyttelsesgruppe til det, "siger Zanin." Denne gruppe blokerer inhibitorens reaktive aldehydfunktion og forhindrer den i at binde sig til proteasomet. "I mørket, hæmmeren er derfor inaktiv, og proteasomet fungerer normalt. Imidlertid, eksponering af cellerne for blåt lys løsner den beskyttende gruppe, hvilket tillader inhibitoren at interagere med proteosomet og hæmme dets funktion. Da den aktiverende blå lysstråling kan målrettes nøjagtigt, inhibitorens virkning kan kontrolleres meget præcist. "På denne måde, vi er i stand til at standse divisionen af tumorceller på et bestemt trin i processen, og at udløse apoptose målrettet ”Forklarer Zanin.
Hun og hendes kolleger mener, at den nye lysfølsomme proteosomhæmmer vil vise sig at være et værdifuldt redskab til undersøgelse af en lang række dynamiske cellulære processer-f.eks. i forbindelse med udviklingen, hvor celler og væv undergår hurtige og ofte radikale ændringer i løbet af kort tid og på trange steder. Ud over, proteosomhæmmere har lovende anvendelser som terapeutiske midler - til behandling af kræft, for eksempel. "Evnen til at aktivere disse forbindelser specifikt både i tid og rum kan gøre dem mere effektive i fremtiden, samtidig reducere forekomsten af bivirkninger, "siger Zanin. Dog, at nå dette mål vil kræve yderligere arbejde, da den hæmmer, der anvendes i det nye studie, ikke er egnet til medicinsk brug i sin nuværende form.
 Varme artikler
Varme artikler
-
 En effektiv måde at fjerne atrazin og dets biprodukter i overfladevandKredit:Institut national de la recherche scientifique Atrazin, meget brugt som ukrudtsmiddel, er kendt for at have skadelige virkninger på akvatiske dyreliv og udgør en risiko for menneskers sundh
En effektiv måde at fjerne atrazin og dets biprodukter i overfladevandKredit:Institut national de la recherche scientifique Atrazin, meget brugt som ukrudtsmiddel, er kendt for at have skadelige virkninger på akvatiske dyreliv og udgør en risiko for menneskers sundh -
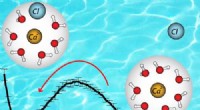 Udforskning af forholdet mellem to-kroppen og kollektivetDen frie energi er forskellig mellem ionparret (venstre) og ionen alene (højre). Det var ikke muligt at se denne forskel med tidligere tilgange. Kredit:American Chemical Society Fra batterier til
Udforskning af forholdet mellem to-kroppen og kollektivetDen frie energi er forskellig mellem ionparret (venstre) og ionen alene (højre). Det var ikke muligt at se denne forskel med tidligere tilgange. Kredit:American Chemical Society Fra batterier til -
 Konstrueret mikrobe kan være nøglen til at producere plastik fra planterUniversity of Wisconsin-Madison postdoc-forsker Alex Linz undersøger en tallerken strøget med N. aromaticivorans (i gult), en jordbakterie, der kunne gøre en vedvarende kilde-lignin fra planteceller
Konstrueret mikrobe kan være nøglen til at producere plastik fra planterUniversity of Wisconsin-Madison postdoc-forsker Alex Linz undersøger en tallerken strøget med N. aromaticivorans (i gult), en jordbakterie, der kunne gøre en vedvarende kilde-lignin fra planteceller -
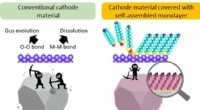 Bygger et bedre batteri, lag for lag(LEFT) Direkte kontakt med elektrolytter forårsager katodeerosion. (HØJRE) Dækkede katodens overflade med selvmonteret enkeltlag, både effekttætheden og cyklabiliteten kan forbedres i højspændings lit
Bygger et bedre batteri, lag for lag(LEFT) Direkte kontakt med elektrolytter forårsager katodeerosion. (HØJRE) Dækkede katodens overflade med selvmonteret enkeltlag, både effekttætheden og cyklabiliteten kan forbedres i højspændings lit
- Den røde farve påvirker investorernes adfærd, afslører finansiel undersøgelse
- Sådan fungerer militære robotter
- Australien, du har ufærdige forretninger. Det er tid til at lade vores ildfolk passe på dette land
- 3-D-printede polymerstents vokser med pædiatriske patienter og nedbrydes biologisk over tid
- Adgangskoder tjener et personligt formål
- Hvordan kan astronomer fortælle, hvad en fjerntliggende temperatur er?


