Forskere dyrker den mest naturtro knogle endnu fra vævede celler
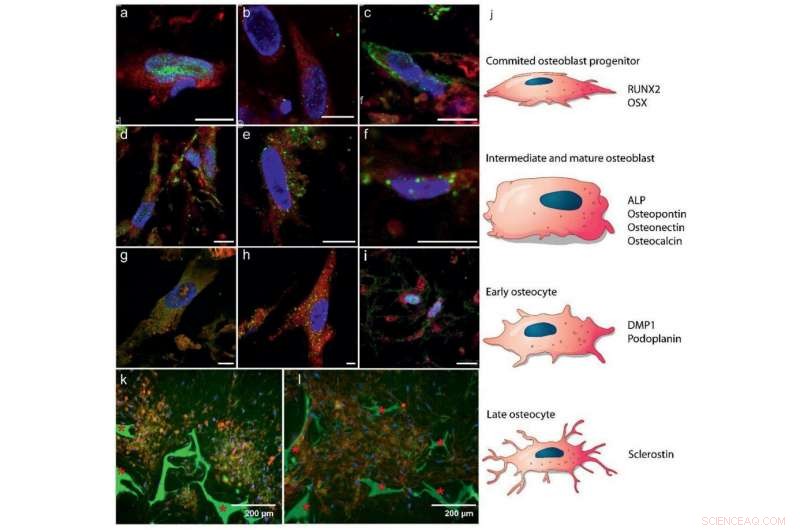
Differentiering af hBMSC'er til osteoblaster og osteocytter:a–i) Fluorescensimmunhistokemi billeddannelse, der viser markører for a–c) tidlige stadier af osteoblastdannelse, d–f) modne osteoblaster, og g–i) osteocytudvikling (5,55 mm glucose). Farvekode:rød - celle cytoplasma, blå cellekerner, grøn:a) RUNX2 (dag 7), b) OSX (dag 7), c) ALP (dag 26), d) osteocalcin (dag 26), e) osteopontin (dag 26), f) osteonectin (dag 21), g) DMP1 (dag 28), h) podoplanin (dag 28), og i) sklerostin (dag 28). Skala søjler:10 µm. Se figur S4, Understøttende information, for separate kanaler. j) Skematisk illustration af MSCs differentiering til osteoblaster og osteocytter, angiver, i hvilken tilstand hvilket proteinekspression forventes i a–i. k, l) Fluorescerende billeder, der indikerer selvorganiserede domæner af osteocytter indlejret i en mineraliseret matrix efter 8 uger (25 mm glukose), k) co-lokalisering af osteocytter (sklerostin, rød) og mineralsk (calcein, grøn), og l) kollagen (CNA35, rød) og mineralsk (calcein, grøn) * Angiver silkefibroin-stilladset.
Forestil dig at bruge stamceller fra din knoglemarv til at dyrke et stykke knoglevæv i laboratoriet, hvorefter læger undersøger, hvilke lægemidler der har den ønskede effekt på dine knogler. På denne måde der ville blive lavet en skræddersyet behandlingsplan for alle, hvor den bedste tilgang er klar på forhånd:personlig medicin, når det er bedst.
Den fremtidsvision er ikke længere science fiction, nu hvor forskere fra Eindhoven University of Technology og Radboud University Medical Center faktisk har indset den første del:at dyrke et naturtro stykke knoglevæv fra menneskelige stamceller. Det er den første organoid af knogler, en forenklet version af originalen, rapporterer forskerne i dag i tidsskriftet Avancerede funktionelle materialer .
Sammenhængende billede
"Med dette, vi præsenterer, for første gang, det fulde billede af tidlig knogledannelse, siger Sandra Hofmann, lektor i Bioengineering Bone fra TU/e. Og det er af stor betydning:Hvordan vores knogler er dannet er stadig stort set et mysterium. Knogle er et meget komplekst materiale, hvor utallige celler og processer interagerer, og omfatter en genial matrix af kollagen og mineral for at give styrke. Meget er kendt om de enkelte komponenter, men der har manglet et sammenhængende billede indtil nu.
Tre typer celler spiller hovedrollen i knogledannelsen:osteoblaster (som bygger knoglevæv), osteoklaster (som fjerner knogler) og osteocytter (som regulerer opbygning og nedbrydning af knogler). "De fleste undersøgelser indtil videre har fokuseret på en af disse typer celler, men det er ikke en god repræsentation af det rigtige væv, " siger Hofmann. "Vi præsenterer her et stykke vævet knogle (knogle i det tidlige stadie), der er udviklet fra stamceller og indeholder to typer af disse celler:osteoblaster og osteocytter. Vi ser nu, at vi udelukkende kan lave naturtro knogler med disse to celletyper."
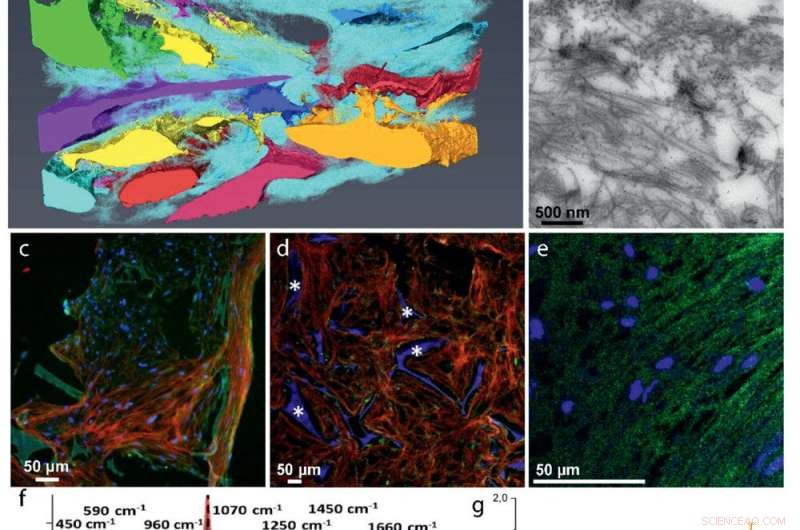
ECM-udvikling:a) 3D FIB/SEM-rekonstruktion viser indlejringen af cellerne i kollagenmatrixen (cyan). Diskrete celler er repræsenteret med forskellige farver. b) TEM-billede af et 70 nm-snit, der viser den tilfældige fordeling af kollagenfibriller. Kollagen type I blev identificeret ved immunmærkning. c–e) Fluorescerende immunhistokemi, der identificerer vigtige ikke-kollagene proteiner i den kollagene matrix:c) Co-lokalisering af osteocalcin (grøn) og kollagen (rød). d) Osteopontin (grøn) fordeling i kollagenmatrixen (rød). * Angiver silkefibroin stilladset. e) Samlokalisering af DMP1 (grøn) med kollagenstrukturen (se figur S5, Understøttende information, for kollagenbillede). f–g) Raman-mikrospektrometri af mineraliserede matricer. f) Lokaliserede Raman-spektre af mineraliseret kollagen fra udviklende zebrafiskknogle (rød), den 3D osteogene co-kultur (blå), og menneskelig knogle fra en 10 år gammel hun (grå g) Raman-afledt mineral/matrix-forhold af 4 mineraliseret væv fra zebrafisk (N =6, rød), Osteogen 3D-kultur (N =7, grøn), 10 år gammel kvindelig kvinde (N =1, grå), og 48+ år gammel mandlig mand (N =7, sort, taget fra ref. [36]). Søjler angiver prøvestandardafvigelser. h) Varmekortpræsentation af et 3D FIB/SEM-tværsnit, der viser uorganiserede kollagenfibriller med forskellige grader af mineralisering (Figur S10, Understøttende oplysninger). Pilespidser angiver ikke-mineraliserede kollagenfibriller (lyseblå), pil angiver mineraliseret kollagenfibril (orange). i) TEM-billede, der viser individuelle mineraliserede kollagenfibriller.
Bliver klogere af molekylær poking
"Og måske endnu vigtigere, vores system opfører sig ligesom knogle i tidlige stadier, " siger Anat Akiva, adjunkt Cellebiologi ved Radboudumc. "Vi viser, at begge typer celler producerer de proteiner, de har brug for for deres funktionalitet, og vi viser med den største detalje, at matrixen faktisk er den knoglematrix, vi ser i rigtigt væv."
Det faktum, at en forenklet fremstilling af knogledannelsen på molekylært niveau nu er mulig, giver hidtil usete muligheder, ifølge forskerne. "En knogle består af 99% kollagen og mineraler, men der er også yderligere 1 % af proteinerne, der er afgørende for vellykket knogledannelse, " forklarer professor Nico Sommerdijk fra Radboudumc. "Så hvad er disse proteiners rolle? Hvordan understøtter de knogledannelsen? Aldrig før har vi været i stand til at se på milepælene i denne proces på et molekylært niveau."
Og dermed de har umiddelbart en god indgang til at undersøge årsagen til genetiske knoglesygdomme som "brittle bone disease" og deres mulige behandlinger. "Husk, at oprindelsen til mange sygdomme er på molekylært niveau - og det samme er behandlingen, " siger Akiva. "Faktisk, vi har nu et simpelt system i et pålideligt miljø, hvor vi kan stikke rundt og se, hvordan knogleceller reagerer på de stimuli, vi giver."
 Varme artikler
Varme artikler
-
 Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha
Proteiner koreograferer den uendelig lille dans af levende celler og funktionelle biomaterialerBlomsterlignende mikrostrukturer dannes på en nanoporøs glasmonolit med 31nm-diameter porer. Kredit:Lehigh University, Thamma, Kowal, Falk, Jain Et tværfagligt forskerhold ved Lehigh University ha -
 Når man ændrer et atom, bliver molekyler bedreKredit:pexels/CC0 Udvikling og forbedring af lægemidler spiller den centrale rolle i den igangværende kamp mod sygdomme hos mennesker. Organisk syntese er det felt, der muliggør disse udviklinger,
Når man ændrer et atom, bliver molekyler bedreKredit:pexels/CC0 Udvikling og forbedring af lægemidler spiller den centrale rolle i den igangværende kamp mod sygdomme hos mennesker. Organisk syntese er det felt, der muliggør disse udviklinger, -
 Et skridt tættere på praktisk solbrintproduktion via kunstfærdigt modificeret hæmatitfotoanodeFigur 1. Skematisk synteseprocedure af Ta:Fe2O3@Fe2O3 homojunction nanorods. Brug af hybrid mikrobølgeglødning, hæmatit homojunction nanorod syntetiseres ved hydrotermisk genvækst af tyndt FeOOH lag p
Et skridt tættere på praktisk solbrintproduktion via kunstfærdigt modificeret hæmatitfotoanodeFigur 1. Skematisk synteseprocedure af Ta:Fe2O3@Fe2O3 homojunction nanorods. Brug af hybrid mikrobølgeglødning, hæmatit homojunction nanorod syntetiseres ved hydrotermisk genvækst af tyndt FeOOH lag p -
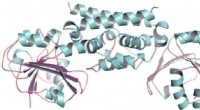 Peanut-familiehemmeligheden for fremstilling af kemiske byggesten afsløretDen tredimensionelle struktur af PDH-enzymet fra sojabønne, en bælgplante. Denne struktur hjalp med at vise, at kun én mutation tillod bælgfrugter at udvikle en ny måde at fremstille aminosyren tyrosi
Peanut-familiehemmeligheden for fremstilling af kemiske byggesten afsløretDen tredimensionelle struktur af PDH-enzymet fra sojabønne, en bælgplante. Denne struktur hjalp med at vise, at kun én mutation tillod bælgfrugter at udvikle en ny måde at fremstille aminosyren tyrosi
- Nogle overraskelser om nedbrydning af mikroplast i vores oceaner
- Håndplukkede specialafgrøder modne til præcisionslandbrugsteknikker
- Hvilke dyr har vinger?
- Team designer carbon nanostruktur stærkere end diamanter
- En ny dimension for batterier
- Video:Vi spurgte en NASA-forsker – lignede Mars nogensinde Jorden?


