Aktivering af synligt lys muliggør transformation af bordstabile sulfoner til værdifulde glykosider

Skematisk, der viser designet af et synligt lys-medieret system til at krydskoble forskellige elektrofiler med glycosylradikaler afledt af bench-stabile heteroarylsulfoner. Kredit:Nature Synthesis (2022). DOI:10.1038/s44160-022-00162-w
Kemikere fra National University of Singapore har udviklet en ny strategi til at generere terapeutisk relevante C-glykosider og S-glykosider gennem en katalysator- og overgangsmetalfri tilgang under synlig lysbelysning ved omgivelsestemperatur. Deres forskning vises i Nature Synthesis .
Glykosider spiller en uundværlig rolle i forskellige fysiologiske funktioner og findes i en lang række naturlige produkter og syntetiske forbindelser. C-glykosider er en vigtig klasse af glycosider, som består af en sukkerholdig enhed forbundet med en organisk del eller en anden sukkerholdig forbindelse gennem en carbon-carbon (C-C) binding. De besidder et utal af biologiske aktiviteter og er strukturelt forskellige. En bekvem måde at konstruere sådanne produkter på involverer den direkte forening af en glycosylprecursor (donor) med et carbonbaseret reagens.
Imidlertid er omfanget af C-glykosider, der kan tilgås ved hjælp af aktuelt rapporterede metoder, stærkt begrænset. Dette skyldes manglen på praktiske glycosyldonorer til rådighed for at lette mild C-C-kobling. En generel klasse af bænkstabile glycosyl-precursorer, der let kan syntetiseres og isoleres i stor skala, og alligevel tilstrækkeligt reaktive til at undergå hurtig og stereoselektiv krydskobling ved omgivende betingelser, er yderst ønskelig, men uhåndgribelig.
Et forskerhold ledet af adjunkt Koh Ming Joo, fra Institut for Kemi, National University of Singapore, har udtænkt robuste procedurer til at syntetisere faste heteroarylglycosylsulfoner på multigramskala. Holdet opdagede, at disse bænkstabile sulfoner også er redoxaktive. Ved at bruge synligt (blåt) lys og et Hantzsch-esterbaseret kompleks er forskerne i stand til at aktivere sulfonerne til at producere kemisk reaktive glycosylradikaler.
Disse radikaler reagerer let med forskellige elektrofiler. Med denne metode er de i stand til at opnå et bredere udvalg af værdifulde C-alkyl, C-alkenyl, C-alkynyl, C-heteroaryl og S-bundne glycosider på en effektiv og yderst selektiv måde. Forskerne brugte også ultraviolet/synlig absorptionsspektroskopiske og radikale urstudier for at få indsigt i mekanismen bag disse transformationer.
Prof Koh sagde:"Denne katalysator- og overgangsmetalfri metode overvinder effektivt tidligere begrænsninger i omfang, skalerbarhed og glycosyldonor-ustabilitet."
"Vi forventer, at denne generelle klasse af glycosyl-prækursorer og deres nyopdagede reaktivitet under synligt lys vil finde omfattende anvendelse i forskellige kulhydratsyntetiske applikationer, hvilket øger indsatsen mod opdagelsen af nye sukkerbaserede terapier og vores forståelse af biologiske processer," tilføjede Prof. Koh.
Forskerholdet planlægger at arbejde med virksomheder for at udnytte disse resultater til syntese af sukker-afledte forbindelser. + Udforsk yderligere
Titaniumkatalyse muliggør stereoselektiv syntese af C-glykosider og glycopeptider
 Varme artikler
Varme artikler
-
 Uendeligt genanvendelig polymer viser praktiske egenskaber af plastEugene Chens laboratorium har udviklet en fuldstændig genanvendelig polymer, vist her. Kredit:Bill Cotton/Colorado State University Verden blev forelsket i plastik, fordi de er billige, praktisk,
Uendeligt genanvendelig polymer viser praktiske egenskaber af plastEugene Chens laboratorium har udviklet en fuldstændig genanvendelig polymer, vist her. Kredit:Bill Cotton/Colorado State University Verden blev forelsket i plastik, fordi de er billige, praktisk, -
 Ikke alle naturens lagdelte strukturer er hårde som dyreskaller og gevirer, undersøgelse finderAnkerpiggene, der holder svampearten Euplectella aspergillum til havbunden, har en indviklet lagdelt indre struktur. Lignende lagdelte strukturer er kendt for at øge sejheden af materialer som knogl
Ikke alle naturens lagdelte strukturer er hårde som dyreskaller og gevirer, undersøgelse finderAnkerpiggene, der holder svampearten Euplectella aspergillum til havbunden, har en indviklet lagdelt indre struktur. Lignende lagdelte strukturer er kendt for at øge sejheden af materialer som knogl -
 Forskere skaber nyt byggemateriale af svamp, ris og glasSvampestensprototyper fremstillet af risskaller og affald af glasaffald. Kredit:Tien Huynh, Forfatter angivet Ville du bo i et hus lavet af svamp? Det er ikke kun et retorisk spørgsmål:svampe er n
Forskere skaber nyt byggemateriale af svamp, ris og glasSvampestensprototyper fremstillet af risskaller og affald af glasaffald. Kredit:Tien Huynh, Forfatter angivet Ville du bo i et hus lavet af svamp? Det er ikke kun et retorisk spørgsmål:svampe er n -
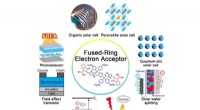 Fremskridt i elektronacceptorer med fusioneret ringStrukturen af ITIC og applikationer af FREAs. Kredit:College of Engineering, Peking Universitet Fra 1995-2015, fullerenderivater havde været de dominerende elektronacceptorer i organiske solcell
Fremskridt i elektronacceptorer med fusioneret ringStrukturen af ITIC og applikationer af FREAs. Kredit:College of Engineering, Peking Universitet Fra 1995-2015, fullerenderivater havde været de dominerende elektronacceptorer i organiske solcell
- Hvilke faktorer påvirker smeltepunktet?
- Hurtige tests til tidlig diagnose af hjerteanfald og identifikation af sepsis
- Drillede Ford lige en elektrisk Mustang, da Tesla debuterede Model Y?
- Forskere viser højtydende vejrtrækning i knogler
- Stigende havtemperatur truer Grønlands indlandsis
- Connecticuts skove i dag er langt fra gamle tårnhøje giganter


