Ny screeningsteknik sat til radikalt at fremskynde jagten på kræftbekæmpende stoffer

I en proces kendt som transkription transskriberes DNA til messenger-RNA (mRNA) af enzymet RNA-polymerase (RNAP). Under TBS sidder AP-1-molekyler (blå) på vigtige DNA-steder (gule), og fungerer som vejspærringer for denne proces, hvilket resulterer i celledød. Vejspærringen fjernes (billede til højre), når peptidmolekyler (røde og hvide) binder til AP-1, både slår den af DNA-strengen og sekvestrerer den. Så overlever cellen. Kredit:Neil Kad, professor i molekylær biofysik, University of Kent
Forskere har udviklet en ny teknik til at fremskynde opdagelsen af kræftbekæmpende lægemidler. Teknikken identificerer molekyler, der kan lukke farlige proteiner ned, før de forårsager sygdomsudløsende kaos, ved at blokere dem i at interagere med en celles DNA.
Den nye platform til opdagelse af lægemidler - kaldet Transcription Block Survival (TBS) - er udviklet af forskere ved universiteterne i Bath og Kent i Storbritannien og har potentialet til dramatisk at fremskynde jagten på helbredelse af dødelige kræftformer. Dette gennembrud har også bredere implikationer, da proteinerne involveret i kræft også spiller en central rolle i mange andre sygdomme, herunder osteoporose og inflammatoriske sygdomme som leddegigt og psoriasis.
"At identificere processer, der kan gøre det hurtigere for forskere at finde nye lægemiddelkandidater til alvorlige sygdomme, som vi er i stand til at gøre ved at bruge TBS, er en stor fordel for forskningen," siger hovedforsker professor Jody Mason, som er baseret på universitetets afdeling i biologi og biokemi.
Opdagelse af lægemidler er langsom, dyr og kompleks. Ofte er forskere på jagt efter at finde farmaceutiske molekyler, der kan binde sig til steder på sygdomsfremkaldende proteiner. Men binding til et målsted er ikke nok – et terapeutisk molekyle skal også have evnen til at lukke ned for det farlige protein. Det vigtigste er, at det skal lykkes i en levende celle uden for mange bivirkninger.
"En stor udfordring er at finde måder at sikre funktionelt tab af skadelig proteinaktivitet i en celles krævende miljø," siger professor Mason.
Han tilføjer, at "ved at bruge TBS-tilgangen er vi ved det allerførste gennemløb i stand til at eliminere molekyler, der klæber til cellemålet, men som i sidste ende ikke slår funktionen af det sygdomsfremkaldende protein ud. Ved at fjerne molekyler fra screeningsprocessen som i sidste ende har ringe eller ingen terapeutisk værdi, vil vi spare en masse tid og penge."
Selvom TBS kan anvendes på opdagelsen af lægemiddelkandidater til et vilkårligt antal sygdomme, er professor Masons nye forskning centreret omkring at finde molekyler kaldet peptider (korte kæder af aminosyrer - proteinernes byggesten), som permanent undertrykker aktiviteten af et protein kaldet Activator Protein-1 (AP-1). AP-1 er naturligt til stede i kroppen og er vigtig for at 'tænde' gener involveret i en række cellulære processer, men når den er ude af kontrol, bliver den en vigtig aktør inden for kræft.
Det hele er i bindingen
Gener virker ved at lave kopier af sig selv i en proces kendt som transskription. Disse kopier, som tager form af messenger-RNA (mRNA), omdanner derefter den genetiske information til proteiner - livets byggesten, der udfører instruktionerne kodet i generne. AP-1 fremmer væksten af kræftceller først ved at binde sig til genpromotorer i specifikke dele af en celles DNA og derefter kapre ekspressionen af nøglegener ved at tænde dem permanent. Med andre ord tvinger AP-1 et gen til at lave mRNA og tilsvarende proteiner på de forkerte tidspunkter og mængder.
Det er disse proteiner, når de overudtrykkes, der er impliceret i spredningen af kræft. Omvendt, gennem aktiviteten af et kræftbekæmpende peptid, kan AP-1 forhindres i at binde sig til en celles DNA, hvilket forhindrer den i at tænde for gener.
Undersøgelses første forfatter Dr. Andrew Brennan, også fra Baths Institut for Biologi og Biokemi, siger, at "ved at bruge TBS-screeningsplatformen kan forskere finde peptider, der binder AP-1 på en sådan måde, at de garanterer, at det ikke kan overstimulere kræftrelaterede gener . Disse peptider kan både blokere AP-1 fra at binde til DNA eller sparke AP-1 fra gener, som det allerede har parret med, hvilket giver dem mulighed for at slukke for kræftsignalet i sårbare celler."
Lægemiddelmolekyler, der arbejder dobbelt hårdt
Etablerede teknikker til lægemiddelscreening gør det allerede muligt for forskere at identificere kræft-slående peptider ved deres evne til at binde AP-1. En stor styrke og kendetegn ved den nye lægemiddelscreeningsteknik er imidlertid, at den giver forskere mulighed for at identificere peptider, der har en dobbelt funktion:de kan genkende/binde sig til AP-1 både før det har bundet sig til DNA, og når det er i en DNA-bundet tilstand, hvilket i sidste ende frigør AP-1 fra DNA og lukker dets funktion helt ned.
"Denne evne til at skelne mellem AP-1-bindere og dem, der er i stand til at lukke AP-1-funktionen, er unik for denne teknik og løser et problem, som indtil nu har hæmmet søgningen efter 'funktionelt aktive' hæmmere," siger professor Mason.
Et andet kendetegn ved TBS er, at screeningsteknikken sker i levende celler og uden at modificere hverken proteinmålet eller peptidbiblioteket med tags (molekylære mærker, der typisk tilføjes for at hjælpe med identifikationsprocessen), der kan ændre funktionen, et almindeligt problem med andre teknikker. De fleste etablerede screeningmetoder involverer testning af peptider in vitro (dvs. uden for levende celler), hvilket betyder, at målbinding er den eneste faktor, der overvejes. Dette kan resultere i falske positiver.
"Det, man ofte finder, når screening udføres ved hjælp af traditionelle metoder, er, at et peptid ser ud til at virke på et isoleret protein, men ikke har samme effekt, når det bruges i en cellulær sammenhæng, og det garanterer bestemt ikke det funktionelle tab af protein", siger professor Mason.
I dette værk, for nylig offentliggjort i JACS Au , har professor Mason og hans team screenet over 130.000 forskellige peptider for at identificere en, der er funktionelt aktiv (rød og hvid på billedet) i potent blokering af AP-1 (blå) fra binding til specifikke DNA-sekvenser (gul). Denne handling blokerer effektivt AP-1's evne til at fremme gentranskription.
Den patenterede TBS-tilgang kan anvendes til at finde terapeutiske molekyler, der kan målrette en bred vifte af DNA-bindende proteiner involveret i sygdom. + Udforsk yderligere
Ny metode til at generere potente, specifikke bindingsproteiner til nye lægemidler
 Varme artikler
Varme artikler
-
 Simpel kemi vil øge bæredygtigheden af betonproduktionKredit:University of Tokyo Forskere ved Institut for Industrividenskab, en del af University of Tokyo, har udviklet en ny metode til fremstilling af beton uden cement. De har direkte bundet sandpa
Simpel kemi vil øge bæredygtigheden af betonproduktionKredit:University of Tokyo Forskere ved Institut for Industrividenskab, en del af University of Tokyo, har udviklet en ny metode til fremstilling af beton uden cement. De har direkte bundet sandpa -
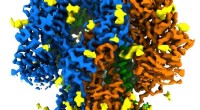 Forskere får det mest realistiske billede endnu af en proteinstruktur med spikes af coronavirusDette billede viser den detaljerede struktur af en spids fra en coronavirus, der forårsager forkølelsessymptomer - en mildere slægtning til den virus, der forårsager COVID-19. Pigge binder sig til rec
Forskere får det mest realistiske billede endnu af en proteinstruktur med spikes af coronavirusDette billede viser den detaljerede struktur af en spids fra en coronavirus, der forårsager forkølelsessymptomer - en mildere slægtning til den virus, der forårsager COVID-19. Pigge binder sig til rec -
 Forskere forudser nye superhårde materialerKredit:Pixabay/CC0 Public Domain En gruppe Skoltech -forskere brugte machine learning (ML) metoder til at forudsige superhårde materialer baseret på deres krystalstruktur. Forskningen blev offent
Forskere forudser nye superhårde materialerKredit:Pixabay/CC0 Public Domain En gruppe Skoltech -forskere brugte machine learning (ML) metoder til at forudsige superhårde materialer baseret på deres krystalstruktur. Forskningen blev offent -
 Modificeret bakterie omdanner petroleum direkte til byggesten til plastKredit:Wageningen UR En bakterie opfylder et længe næret ønske fra mange kemikere. E. coli bakterien, som er blevet modificeret for at udstyre den med specielle enzymer, har vist sig at lave bygge
Modificeret bakterie omdanner petroleum direkte til byggesten til plastKredit:Wageningen UR En bakterie opfylder et længe næret ønske fra mange kemikere. E. coli bakterien, som er blevet modificeret for at udstyre den med specielle enzymer, har vist sig at lave bygge
- Elektrokemi forstærkes i pharma
- Australias Wesfarmers sælger kæmpende Storbritanniens Homebase for £1
- Enkel epitelvæv: Definition, struktur og eksempler
- Hvordan COVID-19 har ændret det, vi ser, og hvordan vi ser det
- Forskere argumenterer for mere omfattende undersøgelser af Cascade-vulkaner
- Tilstoppede porer for øget effektivitet:Valleprotein stabiliserer nanotransporter, kontrollerer pH-…


