Hvordan nitrogen overføres af en katalysator
1. Haber-Bosch-proces:I denne proces reageres nitrogengas (N2) og hydrogengas (H2) sammen i nærvær af en katalysator, typisk jern(III)oxid med promotorer som kaliumoxid og aluminiumoxid, under højt tryk og temperatur for at producere ammoniak (NH3). Katalysatoren letter brydningen af den stærke tredobbelte binding i N2 og dannelsen af N-H-bindinger, der omdanner nitrogen til en mere reaktiv form.
2. Katalytisk ammoniakoxidation:Ammoniak kan oxideres til at producere salpetersyre (HNO3), en nøglekomponent i produktionen af gødning og sprængstoffer. Denne proces involverer reaktionen af ammoniak med oxygen i nærvær af en katalysator, såsom platin eller rhodium. Katalysatoren øger reaktionens effektivitet, hvilket muliggør omdannelse af ammoniak til nitrogenoxid (NO) og derefter til salpetersyre.
3. Katalytisk hydrogenering:Nitrogen kan også overføres ved katalytisk hydrogenering, som involverer tilsætning af hydrogen til en nitrogenholdig forbindelse. For eksempel ved fremstilling af hydrazin (N2H4) reageres nitrogengas med brint i nærværelse af en katalysator, såsom ruthenium eller cobalt. Katalysatoren letter brydningen af N-N-tripelbindingen og dannelsen af N-H-bindinger, hvilket resulterer i dannelsen af hydrazin.
4. Katalytisk nitrogenfiksering:Visse bakterier, såsom Rhizobium, har evnen til at omdanne atmosfærisk nitrogen til ammoniak gennem en proces kaldet nitrogenfiksering. Denne proces involverer enzymet nitrogenase, som fungerer som en katalysator for reduktion af N2 til NH3. Nitrogenase-enzymet indeholder jern og molybdæn som essentielle metal-cofaktorer, som muliggør interaktion med nitrogen- og brintmolekyler og letter nitrogenfikseringsreaktionen.
Dette er et par eksempler på, hvordan nitrogen kan overføres af en katalysator. Katalysatorer spiller en afgørende rolle i at forbedre effektiviteten og selektiviteten af kemiske reaktioner, der involverer nitrogen, hvilket muliggør produktion af forskellige nitrogenholdige forbindelser, der har betydelige industrielle og landbrugsmæssige anvendelser.
 Varme artikler
Varme artikler
-
 Ny genanvendelig hydrogel kunne høste rent, afsaltet vand fra fugtig luft over havoverfladerDen nye hydrogel udviklet af et team fra National University of Singapore, ledet af adjunkt Tan Swee Ching (yderst til højre), kan bruges til at høste rent vand fra fugtig luft over havoverflader, blo
Ny genanvendelig hydrogel kunne høste rent, afsaltet vand fra fugtig luft over havoverfladerDen nye hydrogel udviklet af et team fra National University of Singapore, ledet af adjunkt Tan Swee Ching (yderst til højre), kan bruges til at høste rent vand fra fugtig luft over havoverflader, blo -
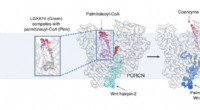 Nye cryo-EM-billeder kaster lys over Wnt-signaleringCryo-EM afslører, hvordan Wnt, et nøglesignalmolekyle for menneskelig udvikling og kræft, modificeres af et enzym ved navn PORCN. Kredit:UT Southwestern Medical Center Ved hjælp af UT Southwesterns
Nye cryo-EM-billeder kaster lys over Wnt-signaleringCryo-EM afslører, hvordan Wnt, et nøglesignalmolekyle for menneskelig udvikling og kræft, modificeres af et enzym ved navn PORCN. Kredit:UT Southwestern Medical Center Ved hjælp af UT Southwesterns -
 Mildere ammoniaksyntesemetode bør hjælpe miljøetProduktion af ammoniak via en kemisk looping-proces. Kredit:GAO Wenbo Et kinesisk forskerhold har udviklet en mildere måde at syntetisere ammoniak på ved at kræve lavere temperatur og tryk end den
Mildere ammoniaksyntesemetode bør hjælpe miljøetProduktion af ammoniak via en kemisk looping-proces. Kredit:GAO Wenbo Et kinesisk forskerhold har udviklet en mildere måde at syntetisere ammoniak på ved at kræve lavere temperatur og tryk end den -
 Video:Hvad gør tardigrader til så store overlevendeKredit:The American Chemical Society Tardigrader er bittesmå dyr, der kan leve i vanddråber stort set overalt. Når disse vanddråber tørrer ud, tardigrader gennemgår en forbløffende transformation
Video:Hvad gør tardigrader til så store overlevendeKredit:The American Chemical Society Tardigrader er bittesmå dyr, der kan leve i vanddråber stort set overalt. Når disse vanddråber tørrer ud, tardigrader gennemgår en forbløffende transformation
- Arbejde hjemmefra? Tæl dine virtuelle velsignelser
- Beskytter vores energiinfrastruktur mod cyberangreb
- New Zealanders tro på klimaændringer stiger
- Hvordan Microsoft kom ud af mørket for at omfavne skyen
- Læring på legepladsen:Hvordan skolefrikvarteret fremmer børns udvikling
- Ny nanopartikelplatform viser sig effektiv til levering af proteinbaserede lægemidler


