Vandets form:Sådan ser vandmolekyler ud på overfladematerialerne
På hydrofile overflader (overflader, der tiltrækker vand), har vandmolekyler tendens til at sprede sig og danne en tynd film. Vandmolekylerne er stærkt tiltrukket af overfladen, og de arrangerer sig selv på en måde, der maksimerer kontaktområdet mellem vand og overfladen. Denne tynde film kan være nogle få molekyler tyk og kan udvise unikke egenskaber, såsom forbedret overfladebefugtning og kapillærvirkning.
På hydrofobe overflader (overflader, der afviser vand), har vandmolekyler tendens til at danne dråber eller perler. Vandmolekylerne er ikke stærkt tiltrukket af overfladen, så de minimerer deres kontakt med overfladen ved at danne sfæriske dråber. Dråbernes form er påvirket af vandets overfladespænding og balancen mellem tiltrækningskræfterne mellem vandmolekyler og frastødende kræfter mellem vand og overfladen.
I lukkede rum, såsom nanoporer eller mellem to faste overflader, kan vandmolekyler danne ordnede strukturer. Indeslutningen pålægger vandmolekylerne geometriske begrænsninger, hvilket får dem til at arrangere i specifikke mønstre. Disse ordnede strukturer kan udvise unikke egenskaber, såsom ændringer i faseadfærd, forbedret termisk ledningsevne og ændret kemisk reaktivitet.
Under specifikke forhold, såsom ekstrem temperatur eller tryk, kan vandmolekyler også gennemgå faseovergange og danne forskellige krystalstrukturer. For eksempel kan is, som er en fast fase af vand, eksistere i forskellige krystallinske former, hver med sit eget særskilte molekylære arrangement.
Overordnet set er formen af vandmolekyler på overfladen af materialer påvirket af overfladeegenskaberne, miljøforholdene og de mikroskopiske interaktioner mellem vandmolekyler og overfladen. Disse interaktioner kan føre til en række forskellige vandstrukturer og adfærd, som spiller en afgørende rolle i mange videnskabelige og teknologiske anvendelser.
Sidste artikelMen hvad med flow? Effekten af hydrodynamik på væske-væske overgange
Næste artikelHvordan videnskabsmænd opfinder nye farver
 Varme artikler
Varme artikler
-
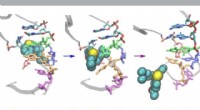 Supercomputere simulerer nye veje til potentiel behandling af RNA-virusStrukturelle ændringer i RNA under lægemiddelbinding/afbinding. Kredit:Lev Levintov, University of New Hampshire University of New Hampshire (UNH) forskere brugte for nylig Comet ved San Diego Sup
Supercomputere simulerer nye veje til potentiel behandling af RNA-virusStrukturelle ændringer i RNA under lægemiddelbinding/afbinding. Kredit:Lev Levintov, University of New Hampshire University of New Hampshire (UNH) forskere brugte for nylig Comet ved San Diego Sup -
 En mere følsom enhed til karakterisering af DNA i blodcirkulationenPrincippet for BIABoosters analysesystem. Fra en renset plasmaprøve, 1 µL analyseres med BIABooster-enheden, som koncentrerer sig, adskiller og detekterer størrelsesprofilen af det cirkulerende DNA.
En mere følsom enhed til karakterisering af DNA i blodcirkulationenPrincippet for BIABoosters analysesystem. Fra en renset plasmaprøve, 1 µL analyseres med BIABooster-enheden, som koncentrerer sig, adskiller og detekterer størrelsesprofilen af det cirkulerende DNA. -
 Guldnanopartikler øger lysemissionen fra wolframdisulfidFiguren viser fluorescensmikroskopibilledet af en trekantet WS2-flage. Indsatsen viser det optiske mikroskopibillede af monoflaken. (a) Når ophidset, den trekantede flage gløder og viser et fængslende
Guldnanopartikler øger lysemissionen fra wolframdisulfidFiguren viser fluorescensmikroskopibilledet af en trekantet WS2-flage. Indsatsen viser det optiske mikroskopibillede af monoflaken. (a) Når ophidset, den trekantede flage gløder og viser et fængslende -
 Ny teknik fremskynder produktionen af protein nano-panserKredit:Carnegie Mellon University Materials Science and Engineering Forskere fra Carnegie Mellon University har udviklet metoder, der fremskynder processen med at udvikle kemisk forbundne syntetis
Ny teknik fremskynder produktionen af protein nano-panserKredit:Carnegie Mellon University Materials Science and Engineering Forskere fra Carnegie Mellon University har udviklet metoder, der fremskynder processen med at udvikle kemisk forbundne syntetis
- Hvad er multiplikationens identitetsejendom?
- Hvad er karakteristika fælles for alle bakterier?
- Test, test, test:Sådan sikrer forskere, at LSST-kameraet er bedst muligt
- Unikt feltstudie viser, hvordan klimaændringer påvirker brandpåvirkede skove
- En lovende ny adfærdsmodel for naturbrande kan hjælpe brandledere i næsten realtid
- Hvad er antherens funktion på en blomst?


