Hvorfor tiltrækkes elektroner af protoner?
$$ F =k \frac{|q_1||q_2|}{r^2} $$
Hvor F er den elektrostatiske kraft, k er den elektrostatiske konstant, q_1 og q_2 er ladningernes størrelse, og r er afstanden mellem ladningerne.
I tilfælde af en elektron og en proton er q_1 =-1,6 × 10^-19 C (ladningen af en elektron) og q_2 =1,6 × 10^-19 C (ladningen af en proton). Afstanden mellem dem er typisk i størrelsesordenen 1 × 10^-10 m (Bohr-radius). Ved at sætte disse værdier ind i Coulombs lov får vi:
$$ F =(9 × 10^9 \frac{N m^2}{C^2}) \frac{(-1,6 × 10^{_19} C)(1,6 × 10^{-19} C)} {(1 × 10^{-10} m)^2} =-2,304 × 10^{−8} N $$
Dette negative tegn indikerer, at kraften er attraktiv. Størrelsen af denne kraft er meget lille, men den er nok til at holde elektronen i kredsløb omkring kernen af et atom.
 Varme artikler
Varme artikler
-
 Forskere finder ny form for hydrofobe molekyler i vandKredit:CC0 Public Domain Indlejringen af hydrofobe molekyler i vand ser helt anderledes ud end tidligere antaget. I vand, hydrofobe molekyler er omgivet af to forskellige vandpopulationer:den in
Forskere finder ny form for hydrofobe molekyler i vandKredit:CC0 Public Domain Indlejringen af hydrofobe molekyler i vand ser helt anderledes ud end tidligere antaget. I vand, hydrofobe molekyler er omgivet af to forskellige vandpopulationer:den in -
 Energihøstende plastik består syretestenDiego Rosas-Villalva forklarede, at holdet var overrasket over, at en så ekstremt tynd polymer var så effektiv til at forbedre enhedens levetid. Kredit:KAUST En polymer, der tidligere blev brugt t
Energihøstende plastik består syretestenDiego Rosas-Villalva forklarede, at holdet var overrasket over, at en så ekstremt tynd polymer var så effektiv til at forbedre enhedens levetid. Kredit:KAUST En polymer, der tidligere blev brugt t -
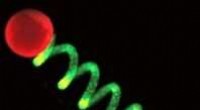 Protoceller springer i gangProtocelle-baseret mikroaktuator; enkelte gigantiske protoceller (røde) ses fastgjort i begge ender af en mekanisk energiforsynet hydrogelfilament (grøn) Naturkemi (2021). Doi:10.1038/s41557-021-007
Protoceller springer i gangProtocelle-baseret mikroaktuator; enkelte gigantiske protoceller (røde) ses fastgjort i begge ender af en mekanisk energiforsynet hydrogelfilament (grøn) Naturkemi (2021). Doi:10.1038/s41557-021-007 -
 Komposterbart biolæder tilbyder bæredygtige løsninger til tøjindustrien og videreMikrobiel biofabrikation og grøn forarbejdning inspireret af kulturarv tilbyder en vej til en cirkulær materialeøkonomi. Kredit:Theanne Schiros/Columbia Engineering og FIT Siden begyndelsen af de
Komposterbart biolæder tilbyder bæredygtige løsninger til tøjindustrien og videreMikrobiel biofabrikation og grøn forarbejdning inspireret af kulturarv tilbyder en vej til en cirkulær materialeøkonomi. Kredit:Theanne Schiros/Columbia Engineering og FIT Siden begyndelsen af de
- Hubble fastholder en mærkelig exoplanet med fjerntliggende kredsløb, der opfører sig som den læn…
- MorphoNet tilbyder en interaktiv måde at udforske biobilleddatarevolutionen på
- Maddikeanalyse går molekylært til retsmedicinske sager
- Sejr eller katastrofe? Amazons udtræk efterlader New York delt
- Udtalelse:Behandl amerikansk våbenvold som en sygdom
- Sammenligningen af et lysmikroskop til et elektronmikroskop


