Hvorfor har beryllium højt smeltepunkt og kogepunkt sammenlignet med andre jordalkalimetaller?
Derudover har beryllium et relativt højt kogepunkt på grund af dets høje ioniseringsenergi. Ioniseringsenergien er den energi, der kræves for at fjerne en elektron fra et atom. Jo højere ioniseringsenergi, jo stærkere tiltrækning mellem kernen og elektronerne. Denne stærke tiltrækning gør det sværere at adskille elektronerne fra kernen, hvilket resulterer i et højere kogepunkt.
Her er en tabel, der opsummerer smeltepunkter og kogepunkter for jordalkalimetallerne:
| Element | Smeltepunkt (°C) | Kogepunkt (°C) |
|---|---|---|
| Beryllium | 1.287 | 2.477 |
| Magnesium | 650 | 1.090 |
| Calcium | 842 | 1.484 |
| Strontium | 768 | 1.382 |
| Barium | 727 | 1.640 |
| Radium | 973 | 1.737 |
Som du kan se, har beryllium det højeste smeltepunkt og kogepunkt af alle jordalkalimetaller.
 Varme artikler
Varme artikler
-
 Ny måde at støde flåter af:Tør deres spyt opKredit:CC0 Public Domain Spyt fra en skovflåts bid kan overføre patogener, der forårsager alvorlige sygdomme, såsom Lyme sygdom, og betydelige landbrugstab. Nuværende insekticider har ulemper, så
Ny måde at støde flåter af:Tør deres spyt opKredit:CC0 Public Domain Spyt fra en skovflåts bid kan overføre patogener, der forårsager alvorlige sygdomme, såsom Lyme sygdom, og betydelige landbrugstab. Nuværende insekticider har ulemper, så -
 Et opløseligt smartwatch gør det nemmere at genbruge elektronikEt prototype smartwatch lavet med zink-sølv nanokomposit-kredsløb inde i en poly(vinylalkohol) kasse (øverst) opløses i vand inden for 40 timer (nederst). Kredit:Tilpasset fra ACS Applied Materials &I
Et opløseligt smartwatch gør det nemmere at genbruge elektronikEt prototype smartwatch lavet med zink-sølv nanokomposit-kredsløb inde i en poly(vinylalkohol) kasse (øverst) opløses i vand inden for 40 timer (nederst). Kredit:Tilpasset fra ACS Applied Materials &I -
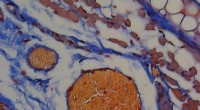 Ved hjælp af lys, røde blodlegemer og et honningbipeptid til at levere terapeutiske proteinerEt orange-rødt farvestof viser, at der dannes blodpropper i et musøre, hvor thrombin blev frigivet fra lysudløste RBCer. Skala bar, 50 μm. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/
Ved hjælp af lys, røde blodlegemer og et honningbipeptid til at levere terapeutiske proteinerEt orange-rødt farvestof viser, at der dannes blodpropper i et musøre, hvor thrombin blev frigivet fra lysudløste RBCer. Skala bar, 50 μm. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/ -
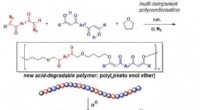 Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde
Ny syntetisk polymer nedbrydeligt under meget milde sure betingelserFremstilling af ny nedbrydelig syntetisk polymer. Kredit:Ehime University Et forskerhold ved Ehime University forberedte en ny type syntetisk polymer, som kan nedbrydes til en kombination af velde
- Delfiner udsat for olie fra Deepwater Horizon-udslip fundet at have ændringer i genaktiviteter
- Forskere foreslår en ny metode til at forbedre heterogen fotosyntese af azoforbindelser
- Naturens langsomme baner giver håb om arter, der føler sig varme af klimaændringer, andet pres
- Hvad er den virkelige historie om hajbestande i New Yorks farvande?
- Hvad er økonomisk traume? Og hvad skal man gøre ved det
- High School Biology Emner


