Hvad indeholder ioner?
Salte er forbindelser, der indeholder positivt ladede ioner (kationer) og negativt ladede ioner (anioner), der holdes sammen af elektrostatiske kræfter. Eksempler på salte omfatter natriumchlorid (NaCl), kaliumnitrat (KNO3) og calciumcarbonat (CaCO3).
Syrer er stoffer, der ved opløsning i vand frigiver hydrogenioner (H+). Eksempler på syrer omfatter saltsyre (HCl), svovlsyre (H2SO4) og salpetersyre (HNO3).
Basis er stoffer, der ved opløsning i vand frigiver hydroxidioner (OH-). Eksempler på baser omfatter natriumhydroxid (NaOH), kaliumhydroxid (KOH) og calciumhydroxid (Ca(OH)2).
Løsninger er homogene blandinger af to eller flere stoffer. Når et salt, syre eller base opløses i vand, adskilles ionerne og bliver spredt gennem opløsningen.
Ioniske væsker er væsker, der udelukkende består af ioner. De dannes typisk ved at smelte et salt eller ved at opløse et salt i et polært opløsningsmiddel. Ioniske væsker har en række anvendelser, herunder som elektrolytter i batterier og som opløsningsmidler i kemiske reaktioner.
Sidste artikelHvilke grundstoffer kan blandes med vand?
Næste artikelHvad er permeabilitetsværdien af germanium?
 Varme artikler
Varme artikler
-
 Lysfølsomt øverste lag af plastikfilm fremkalder bevægelseSkematisk af filmen (til venstre):Filmen er for det meste sammensat af en ikke-fotoresponsiv polymer (200 - 400 nm tyk), og et fotoresponsivt polymerlag eksisterer kun ved overfladen (nogle nm tykt).
Lysfølsomt øverste lag af plastikfilm fremkalder bevægelseSkematisk af filmen (til venstre):Filmen er for det meste sammensat af en ikke-fotoresponsiv polymer (200 - 400 nm tyk), og et fotoresponsivt polymerlag eksisterer kun ved overfladen (nogle nm tykt). -
 Hærforsker bruger matematik til at afdække ny kemiI fremtiden, materialeforskere vil bruge avanceret software til at specificere de egenskaber, de ønsker, og et program vil levere et udvalg af optimerede kemiske forbindelser. Kredit:US Army illustrat
Hærforsker bruger matematik til at afdække ny kemiI fremtiden, materialeforskere vil bruge avanceret software til at specificere de egenskaber, de ønsker, og et program vil levere et udvalg af optimerede kemiske forbindelser. Kredit:US Army illustrat -
 Bioinspirerede materialer-lån fra naturens legebogEt skibsskelet af havsvamp, der viser den komplekse karakter af dets struktur, som giver fantastisk styrke. Kredit:Michael Monn, Kesari Lab, Brown University Naturen giver utallige eksempler på un
Bioinspirerede materialer-lån fra naturens legebogEt skibsskelet af havsvamp, der viser den komplekse karakter af dets struktur, som giver fantastisk styrke. Kredit:Michael Monn, Kesari Lab, Brown University Naturen giver utallige eksempler på un -
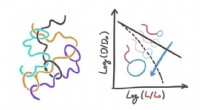 Haletudse på haletudser:Dynamikken i polymerer med en meget unik formDe er født fra foreningen mellem en cirkulær komponent og en lineær komponent og har helt særlige fysiske egenskaber. Under særlige forhold, faktisk, en opløsning af disse molekyler præsenterer sig se
Haletudse på haletudser:Dynamikken i polymerer med en meget unik formDe er født fra foreningen mellem en cirkulær komponent og en lineær komponent og har helt særlige fysiske egenskaber. Under særlige forhold, faktisk, en opløsning af disse molekyler præsenterer sig se
- Gårde skaber masser af data, men landmændene kontrollerer ikke, hvor det ender, og hvem der kan br…
- Holde celler sammen - hvordan vores krop modstår mekanisk stress
- Begyndte livet på land i stedet for i havet?
- Teknik til 3D-print af metaller på nanoskala afslører overraskende fordele
- Dynamisk vurdering kan hjælpe sprogelever til at få mere succes
- Nævn nogle almindelige alkalier og deres anvendelser?


