Hvad er de kemiske reaktioner i miljøet?
1. Fotosyntese:Dette er den proces, hvorved planter omdanner sollys til kemisk energi. Kuldioxid og vand bruges til at producere glukose og ilt.
6CO2 + 6H2O + lysenergi → C6H12O6 + 6O2
2. Cellulær respiration:Dette er den proces, hvorved organismer nedbryder glukose for at frigive energi. Ilt bruges til at producere kuldioxid og vand.
C6H12O6 + 6O2 → 6CO2 + 6H2O + energi
3. Nedbrydning:Dette er den proces, hvorved organisk stof nedbrydes af mikroorganismer til enklere stoffer. Denne proces frigiver næringsstoffer tilbage til jorden, som kan bruges af planter.
Organisk stof + mikroorganismer → CO2 + H2O + næringsstoffer
4. Forbrænding:Dette er den proces, hvorved brændstoffer, såsom træ, benzin og kul, reagerer med ilt for at producere varme og lys. Denne proces frigiver forurenende stoffer, såsom kuldioxid og nitrogenoxider, til atmosfæren.
Brændstof + O2 → CO2 + H2O + energi
5. Sur regn:Dette er den proces, hvorved svovldioxid og nitrogenoxider reagerer med vanddamp i atmosfæren for at producere sur regn. Dette kan skade planter, dyr og bygninger.
SO2 + H2O → H2SO3
NO2 + H2O → HNO3
6. Ozondannelse:Dette er den proces, hvorved ozon dannes i stratosfæren. Ozon beskytter Jorden mod skadelig ultraviolet stråling.
O2 + UV-lys → 2O
O + O2 → O3
7. Drivhusgasemissioner:Dette er den proces, hvorved menneskelige aktiviteter, såsom afbrænding af fossile brændstoffer, frigiver drivhusgasser til atmosfæren. Disse gasser fanger varme og bidrager til klimaændringer.
CO2 + H2O → H2CO3
CH4 + 2O2 → CO2 + 2H2O
N2O + O → 2NO
8. Vandforurening:Dette er den proces, hvorved forurenende stoffer, såsom spildevand, gødning og industriaffald, trænger ind i vandmasser. Dette kan skade akvatiske økosystemer og gøre vandet usikkert at drikke.
Forurenende stoffer + H2O → Skadelige stoffer
Dette er blot nogle få eksempler på de mange kemiske reaktioner, der opstår i miljøet. Disse reaktioner spiller en afgørende rolle i opretholdelsen af Jordens økosystemer og klima.
 Varme artikler
Varme artikler
-
 En bedre måde at lave akryl påKredit:CC0 Public Domain Akryl er en utrolig mangfoldig og nyttig familie af kemikalier, der bruges i alle slags produkter, fra bleer til neglelak. Nu, et team af forskere fra UConn og ExxonMobil
En bedre måde at lave akryl påKredit:CC0 Public Domain Akryl er en utrolig mangfoldig og nyttig familie af kemikalier, der bruges i alle slags produkter, fra bleer til neglelak. Nu, et team af forskere fra UConn og ExxonMobil -
 Forskere opfinder lette flydende metalmaterialerFigur 1. GB-eGaIn. Kredit:LIU Jing Flydende metal ved stuetemperatur, for eksempel Gallium-baseret legering, har høj elektrisk og termisk ledningsevne, og fremragende flydende. De kan bruges inden
Forskere opfinder lette flydende metalmaterialerFigur 1. GB-eGaIn. Kredit:LIU Jing Flydende metal ved stuetemperatur, for eksempel Gallium-baseret legering, har høj elektrisk og termisk ledningsevne, og fremragende flydende. De kan bruges inden -
 Forskningslaboratoriesimulator fuldfører væsentligt lægemiddelopdagelsesarbejde på få dageJohn Wise. Kredit:Southern Methodist University, Hillsman S. Jackson SMU-forskere har udviklet et sæt computerdrevne rutiner, der kan efterligne kemiske reaktioner i et laboratorium, at reducere d
Forskningslaboratoriesimulator fuldfører væsentligt lægemiddelopdagelsesarbejde på få dageJohn Wise. Kredit:Southern Methodist University, Hillsman S. Jackson SMU-forskere har udviklet et sæt computerdrevne rutiner, der kan efterligne kemiske reaktioner i et laboratorium, at reducere d -
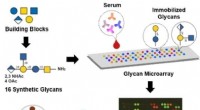 Forskere identificerer potentielle vaccinemål, der i stigende grad vedrører bakteriestammeGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202209556 Acinetobacter baumannii er et bakterielt patogen, der er ansvarlig for alvorlige hospitalsrelater
Forskere identificerer potentielle vaccinemål, der i stigende grad vedrører bakteriestammeGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202209556 Acinetobacter baumannii er et bakterielt patogen, der er ansvarlig for alvorlige hospitalsrelater
- Huse til en varmere fremtid er i øjeblikket begrænset af Australias bygningsregler
- Ny statistisk model forbedrer forudsigelseskraften af standardiserede testresultater
- Air France-KLM-chefen sætter job på spil i standoff med fagforeninger
- Vil du spille video uden plug-ins? Mozilla-OTOY-codec vender skuden
- Skriv ned de tre forskellige måder, hvorpå gammastråling interagerer med stof?
- Hvordan vi vælger:Anvendelse af beslutningsvidenskab på transportadfærd


