Hvis metal er gråt og ilt er en farveløs gas, hvorfor bliver rust rødbrun farve?
1. Oxidation:Jern gennemgår oxidation og mister elektroner til iltatomer. Denne proces omdanner elementært jern (Fe) til jernioner (Fe2+).
2. Hydration:Vandmolekyler omgiver jernionerne og danner hydratiserede ioner kaldet akvaterede jern(II)-ioner (Fe(H2O)6^2+).
3. Yderligere oxidation:Ved tilstedeværelse af ilt og fugt gennemgår de vandholdige jern(II)-ioner yderligere oxidation og mister flere elektroner til jern(III)-ioner (Fe3+).
4. Hydrolyse:Jern(III)-ionerne reagerer med vandmolekyler, undergår hydrolyse for at danne jern(III)hydroxid (Fe(OH)3).
5. Dehydrering og dannelse af jernoxid:Jern(III)hydroxid er oprindeligt et gelatineagtigt, grønbrunt bundfald. Over tid mister dette bundfald vandmolekyler gennem dehydrering og omdannes til jern(III)oxid (Fe2O3), som er den primære bestanddel af rust.
Den rødbrune farve af rust er karakteristisk for Fe2O3. Det er vigtigt at bemærke, at den nøjagtige farve og sammensætning af rust kan variere afhængigt af faktorer som metaltypen, miljøet og stadiet af oxidationsprocessen.
Sidste artikelHvordan laver man tøris?
Næste artikelHvad er de kemiske reaktioner i miljøet?
 Varme artikler
Varme artikler
-
 Mikrostruktureret materiale med rumlig variation har kun friktion i én retningEn sammenligning mellem ensartede funktioner (type 1), venstre, og en gruppe funktioner, der udviser envejsfriktion (type 2), ret, med resulterende kraft-rum-plots, der viser ydeevne, bund. I neutral
Mikrostruktureret materiale med rumlig variation har kun friktion i én retningEn sammenligning mellem ensartede funktioner (type 1), venstre, og en gruppe funktioner, der udviser envejsfriktion (type 2), ret, med resulterende kraft-rum-plots, der viser ydeevne, bund. I neutral -
 Mikrobielt tyveri muliggør nedbrydning af metan, giftig methylkviksølvForskere fik ny indsigt i de mekanismer, som nogle methan-fødende bakterier kaldet metanotrofer bruger til at nedbryde toksinet methylkviksølv. Kredit:Andy Sproles/ORNL, US Department of Energy; Jerem
Mikrobielt tyveri muliggør nedbrydning af metan, giftig methylkviksølvForskere fik ny indsigt i de mekanismer, som nogle methan-fødende bakterier kaldet metanotrofer bruger til at nedbryde toksinet methylkviksølv. Kredit:Andy Sproles/ORNL, US Department of Energy; Jerem -
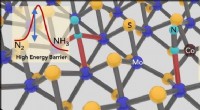 Ammoniaksyntese gjort let med 2-D katalysatorTilsætning af koboltatomer til fyldning af ledige pladser i 2D molybdendisulfidkrystaller øger materialets evne til at katalysere ammoniak fra dinitrogen. Forskere fra Rice University har udviklet en
Ammoniaksyntese gjort let med 2-D katalysatorTilsætning af koboltatomer til fyldning af ledige pladser i 2D molybdendisulfidkrystaller øger materialets evne til at katalysere ammoniak fra dinitrogen. Forskere fra Rice University har udviklet en -
 Ny metode til at forbinde præfabrikerede betonbjælker og søjlerAdjunkt Mostafa Tazarv fra Institut for Bygge- og Miljøteknik fører tilsyn med test af en ny metode til at forbinde præfabrikerede betonbjælker og søjler, der gør det muligt at reparere bygninger efte
Ny metode til at forbinde præfabrikerede betonbjælker og søjlerAdjunkt Mostafa Tazarv fra Institut for Bygge- og Miljøteknik fører tilsyn med test af en ny metode til at forbinde præfabrikerede betonbjælker og søjler, der gør det muligt at reparere bygninger efte
- Skalering af silicium kvantefotonisk teknologi
- Forskere udvikler miniaturiseret kernemagnetisk resonans til olie- og gasudforskning
- Angst i Alaska som endeløse efterskælv rasler indbyggerne
- Jord kan beholde cirka en fjerdedel af den månedlige nedbør
- Sparer tid i rummet
- Opdagelse af ældgamle klippeindtryk tyder på, at evnen til at danne forhornet hud går tilbage til…


