Vis, hvordan hver hvilke stærke elektrolytter bryder op i dets komponentioner ved opløsning i vand NaBr?
Når NaBr opløses i vand, nedbrydes det i dets bestanddele, Na+ og Br-. Na+-ionerne er positivt ladede, mens Br-ionerne er negativt ladede. Tiltrækningen mellem de positive og negative ioner er det, der holder forbindelsen sammen i sin faste tilstand. Men når forbindelsen er opløst i vand, omgiver vandmolekylerne ionerne og bryder krystalgitteret fra hinanden. Dette gør det muligt for ionerne at bevæge sig frit i opløsning.
Ligningen for dissociationen af NaBr i vand er:
$$NaBr_{(s)} \rightarrow Na^+_{(aq)} + Br^-_{(aq)}$$
 Varme artikler
Varme artikler
-
 Højtemperatursyntese under tryk hjælper med at kombinere egenskaber af metaller og keramikAnna Poznyak, leder af projektet og forsker ved NUST MISIS afdeling for funktionelle nanosystemer og højtemperaturmaterialer. Kredit:© Sergey Gnuskov/NUST MISIS Materialeforskere fra NUST MISIS og
Højtemperatursyntese under tryk hjælper med at kombinere egenskaber af metaller og keramikAnna Poznyak, leder af projektet og forsker ved NUST MISIS afdeling for funktionelle nanosystemer og højtemperaturmaterialer. Kredit:© Sergey Gnuskov/NUST MISIS Materialeforskere fra NUST MISIS og -
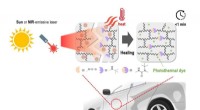 Beskyttende belægningsmateriale heler sig selv på 30 minutter, når det udsættes for sollysSelvhelbredende mekanisme af miljøvenligt beskyttende belægningsmateriale til køretøjer inklusive dynamisk polymernetværk og fototermisk farvestof. Kredit:Korea Research Institute of Chemical Technolo
Beskyttende belægningsmateriale heler sig selv på 30 minutter, når det udsættes for sollysSelvhelbredende mekanisme af miljøvenligt beskyttende belægningsmateriale til køretøjer inklusive dynamisk polymernetværk og fototermisk farvestof. Kredit:Korea Research Institute of Chemical Technolo -
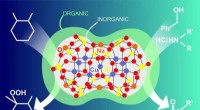 Kemikere syntetiserer en ny hybrid organisk-uorganisk katalysatorKredit:Natalia Deryugina RUDN -kemikere har syntetiseret metalkomplekser på basis af det organoelementale stof silsesquioxan, der består af en organisk og en uorganisk del. Sådanne hybridsystemer
Kemikere syntetiserer en ny hybrid organisk-uorganisk katalysatorKredit:Natalia Deryugina RUDN -kemikere har syntetiseret metalkomplekser på basis af det organoelementale stof silsesquioxan, der består af en organisk og en uorganisk del. Sådanne hybridsystemer -
 Forskere bruger 3D-tryk til at skabe metalliske glaslegeringer i løs vægtCylinderen vist her er en amorf jernlegering, eller metallisk glas, lavet ved hjælp af en additiv fremstillingsteknik. Kredit:Zaynab Mahbooba Forskere har nu demonstreret evnen til at skabe amorft
Forskere bruger 3D-tryk til at skabe metalliske glaslegeringer i løs vægtCylinderen vist her er en amorf jernlegering, eller metallisk glas, lavet ved hjælp af en additiv fremstillingsteknik. Kredit:Zaynab Mahbooba Forskere har nu demonstreret evnen til at skabe amorft
- Rise of the Robots:Kommer til en første-års Intro to Journalism-klasse nær dig
- Enkel skal af plantevirus udløser immunrespons mod kræft
- Hvor mange antal atomer har brint?
- Undersøgelse finder kønsbestemte lønforskelle i store offentlige myndigheder
- At føle hangry er normalt, og du kan beskylde din hjerne
- Naturforringelse kan forårsage et tab på 12% til UK BNP, tyder ny analyse


