Bestem den empiriske formel for at følge en forbindelse fremstillet af 26,19 nitrogen i massen 7,55 hydrogen og 66,26 chlor med en total molær på 53,50 g?
1. Omregn de givne masser til mol:
Mol nitrogen =26,19 g / 28,01 g/mol =0,935 mol
Mol hydrogen =7,55 g / 1,008 g/mol =7,49 mol
Mol klor =66,26 g / 35,45 g/mol =1,87 mol
2. Divider hvert antal mol med det mindste antal mol for at få det enkleste hele talforhold:
0,935 mol / 0,935 mol =1
7,49 mol / 0,935 mol ≈ 8
1,87 mol / 0,935 mol ≈ 2
3. Det enkleste hele talforhold er ca. 1:8:2.
4. Multiplicer de nedskrevne elementer med en passende faktor for at opnå hele tal. I dette tilfælde kan vi gange alle abonnementer med 2 for at få:
2(1) =2
2(8) =16
2(2) =4
Derfor er den empiriske formel for forbindelsen NH4Cl2.
Sidste artikelHvad er massen i g af 0,375 mol element k?
Næste artikelHvorfor må der tilsættes vand efter at syren er blevet pipetteret ind?
 Varme artikler
Varme artikler
-
 Multifunktionel katalysator til giftbestandige brintbrændselscellerReaktionsmekanisme med katalysator til brændselsceller, der bruger brint og kulilte som brændstof. Kredit:Kyushu University Efterspørgslen efter miljøvenlige brændstofkilder er stigende, efterhånd
Multifunktionel katalysator til giftbestandige brintbrændselscellerReaktionsmekanisme med katalysator til brændselsceller, der bruger brint og kulilte som brændstof. Kredit:Kyushu University Efterspørgslen efter miljøvenlige brændstofkilder er stigende, efterhånd -
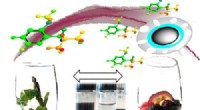 Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel
Magnetisk behandling kan hjælpe med at fjerne bismag fra vineKredit:American Chemical Society Magnetiske nanopartikler knyttet til polymerer er med succes blevet brugt til at målrette og fjerne uønskede smagsstoffer fra vin. Forskere ved University of Adel -
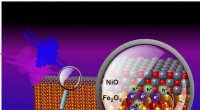 Styring af ladningsflow ved at styre elektronhullerForskere bruger ekstreme ultraviolette pulser (fuchsia linje) til at bestemme, hvordan synligt lys (blå linje) forårsager grænsefladehul (h + ) overførsel fra jernoxid (Fe 2 O 3 ) til nikkeloxid
Styring af ladningsflow ved at styre elektronhullerForskere bruger ekstreme ultraviolette pulser (fuchsia linje) til at bestemme, hvordan synligt lys (blå linje) forårsager grænsefladehul (h + ) overførsel fra jernoxid (Fe 2 O 3 ) til nikkeloxid -
 Livets oprindelse:Kemisk udvikling i en lille golfstrømVarme væsker møder et koldt hav:Lokale temperaturgradienter i porøse vulkanske sten på den tidlige Jord kunne have lettet selvreplikationen af RNA-strenge. Kredit:Picture Alliance Kemiske reakti
Livets oprindelse:Kemisk udvikling i en lille golfstrømVarme væsker møder et koldt hav:Lokale temperaturgradienter i porøse vulkanske sten på den tidlige Jord kunne have lettet selvreplikationen af RNA-strenge. Kredit:Picture Alliance Kemiske reakti
- Onlinespil træner spillerne i, hvordan de sorterer affald korrekt
- Første lys ved den mest kraftfulde laser i USA
- Tagsten i det kejserlige Kina:Oprettelse af Ximing-templers lotusmønstrede teglender
- Hvad er den årlige værdi af træer? 500 millioner dollars pr. megaby, siger undersøgelse
- Ikke-flygtig hukommelse baseret på ferroelektrisk-grafen felt-effekt transistorer er nu et skridt t…
- Super sniffer:Hundens næse inspirerer til nye gassensormaterialer


