Kan vi bruge en stærk opløsning af NaOH til at lave natriumekstrakt i stedet for metal?
Opløsning af stoffet:
1. Start med en koncentreret opløsning af natriumhydroxid (typisk 50 % eller højere).
2. I en passende reaktionsbeholder tilsættes en nøje afvejet mængde af det stof, du vil udvinde.
3. Sørg for korrekt blanding af stoffet i NaOH-opløsningen for at lette opløsningen.
Dannelse af natriumsalt:
4. Afhængigt af stoffets beskaffenhed vil det reagere med de hydroxidioner (OH-), der er til stede i NaOH-opløsningen.
5. Denne reaktion resulterer typisk i dannelsen af et natriumsalt af stoffet, der frigiver vand som et biprodukt.
Oprensning (hvis nødvendigt):
6. Afhængigt af den ønskede renhed kan du udføre yderligere oprensningstrin for at adskille natriumsaltet fra eventuelle urenheder.
Indhentning af natriumekstrakt:
7. Efter oprensning (hvis påkrævet) indeholder den resulterende opløsning natriumsaltet af stoffet.
8. Du kan genvinde dette natriumekstrakt ved forskellige metoder, såsom fordampning af opløsningsmidlet, udfældning eller ekstraktion ved hjælp af organiske opløsningsmidler.
Fordele ved at bruge NaOH frem for elementært natrium:
Sikker håndtering:Natriumhydroxid er mindre farligt end elementært natriummetal, som kan reagere kraftigt og udgøre sikkerhedsrisici, især ved håndtering af større mængder.
Kontrolleret reaktion:Reaktionen mellem stoffet og koncentreret NaOH-opløsning er generelt mere kontrolleret og forudsigelig sammenlignet med at bruge elementært natrium.
Solubilisering:Nogle stoffer reagerer muligvis ikke direkte med elementært natrium eller kræver barske forhold. Brug af NaOH giver mulighed for opløsning og omdannelse af stoffet til dets natriumsaltform.
Bemærk venligst, at de specifikke forhold, sikkerhedshensyn og passende procedurer kan variere afhængigt af arten af det stof, der udvindes. Henvis altid til relevant litteratur, rådfør dig med eksperter og sørg for passende sikkerhedsforanstaltninger, før du forsøger sådanne procedurer.
Sidste artikelHvordan brænder lithium i saltsyre?
Næste artikelEr CH3CH2CH2OH en stærk eller svag elektrolyt?
 Varme artikler
Varme artikler
-
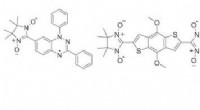 Overvindelse af udfordringerne med kontrolleret termisk aflejring af organiske diradikale stofferVenstre panel:Diradikalerne undersøgt i dette arbejde. Højre panel:Skitse af forskellige film (grøn farve) afsat på et underlag (grå farve). Kredit:Tuebingen Universitet Magnetisme er en egenskab
Overvindelse af udfordringerne med kontrolleret termisk aflejring af organiske diradikale stofferVenstre panel:Diradikalerne undersøgt i dette arbejde. Højre panel:Skitse af forskellige film (grøn farve) afsat på et underlag (grå farve). Kredit:Tuebingen Universitet Magnetisme er en egenskab -
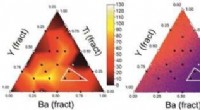 Opdager nye leads til funktionelle materialer styret af kunstig intelligensKredit:Wiley Søger efter blymaterialer med specifikke egenskaber, forskere har udviklet en arbejdsgang, der inkorporerer kunstig intelligens til at guide opdagelsen af en ny keramisk struktur me
Opdager nye leads til funktionelle materialer styret af kunstig intelligensKredit:Wiley Søger efter blymaterialer med specifikke egenskaber, forskere har udviklet en arbejdsgang, der inkorporerer kunstig intelligens til at guide opdagelsen af en ny keramisk struktur me -
 De miljømæssige omkostninger ved fast fashionIkke mere nøjes og repareres. Kredit:wwww.shutterstock.com Det er svært at elske vores tøj og blive ved med at have det på i længere tid, når vi står over for en fristende række af nyheder på tilb
De miljømæssige omkostninger ved fast fashionIkke mere nøjes og repareres. Kredit:wwww.shutterstock.com Det er svært at elske vores tøj og blive ved med at have det på i længere tid, når vi står over for en fristende række af nyheder på tilb -
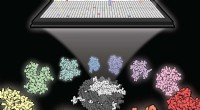 Scanner tusindvis af molekyler mod et uhåndgribeligt kræftmålEn ny undersøgelse udviklede et sæt metoder til at screene tusinder af små molekyler for at finde hæmmere af kræftmålet NSD2. Kredit:Matthew Hall, NCATS Forskere ved National Center for Advancing
Scanner tusindvis af molekyler mod et uhåndgribeligt kræftmålEn ny undersøgelse udviklede et sæt metoder til at screene tusinder af små molekyler for at finde hæmmere af kræftmålet NSD2. Kredit:Matthew Hall, NCATS Forskere ved National Center for Advancing
- Undersøgelse beskriver cellulære fabrikker mere detaljeret
- Kostændring – en løsning til at reducere vandforbruget?
- Apple tilbagekalder nogle bærbare MacBook Pro-computere på grund af brandfare
- Hvorfor Virgin Orbits nye præsident ikke er bekymret for en boble på det lille satellitmarked
- Hvilke forkastningsoverfladetræk kan fortælle os om fremtidige jordskælv
- Volkswagen står over for tysk retsopgør om dieselgate


