En opløsning af natriumcarbonat Na2CO3, der har en molaritet på 0,0100 M indeholder ækvivalenter ioner pr. liter opløsningen?
Natriumcarbonat opdeles i to natriumioner (Na+) og en carbonation (CO32-). Så for hvert mol natriumcarbonat, der opløses, produceres der to mol natriumioner og et mol carbonationer.
Derfor kan antallet af ækvivalenter pr. liter beregnes som følger:
Ækvivalenter pr. liter =(Molaritet af Na2CO3) × (Antal producerede ioner pr. mol Na2CO3)
Ækvivalenter pr. liter =(0,0100 M) × (3 ioner/mol Na2CO3)
Ækvivalenter pr. liter =0,0300 ækv./L
Så natriumcarbonatopløsningen med en molaritet på 0,0100 M indeholder 0,0300 ækvivalenter ioner pr. liter.
 Varme artikler
Varme artikler
-
 Forskere gør plastforurening til rengøringsmidlerKredit:CC0 Public Domain Forskere ved University of Bristol har opdaget en måde at genbruge en almindelig plast til at nedbryde skadelige farvestoffer i vores spildevand. Papiret offentliggjort i
Forskere gør plastforurening til rengøringsmidlerKredit:CC0 Public Domain Forskere ved University of Bristol har opdaget en måde at genbruge en almindelig plast til at nedbryde skadelige farvestoffer i vores spildevand. Papiret offentliggjort i -
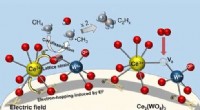 Ny, lavprisalternativ til ethylenproduktionReaktionsmekanismer for den oxidative kobling af methan (OCM) over Ce2(WO4)3-katalysatorer ved lave temperaturer i et elektrisk felt. Kredit:Waseda University Det øgede udbud og de optimerede omko
Ny, lavprisalternativ til ethylenproduktionReaktionsmekanismer for den oxidative kobling af methan (OCM) over Ce2(WO4)3-katalysatorer ved lave temperaturer i et elektrisk felt. Kredit:Waseda University Det øgede udbud og de optimerede omko -
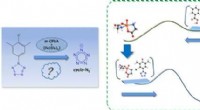 Forskere optrævler syntetisk mekanisme for arylpentazol og substituenteffekthttps://doi.org/10.1021/acs.jpclett.9b03762 Copyright © 2020 American Chemical Society For nylig, et forskerhold ledet af prof. Liu Jianyong og prof. Han Keli fra Dalian Institute of Chemical Phys
Forskere optrævler syntetisk mekanisme for arylpentazol og substituenteffekthttps://doi.org/10.1021/acs.jpclett.9b03762 Copyright © 2020 American Chemical Society For nylig, et forskerhold ledet af prof. Liu Jianyong og prof. Han Keli fra Dalian Institute of Chemical Phys -
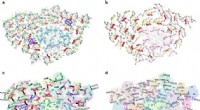 Strukturen af fotosystemprotein-superkompleks fra diatom afslører dets meget sofistikerede energi…Overordnet struktur af PSI-FCPI superkomplekset. Kredit:IBCAS Kiselalger er en gruppe af fytoplankton, der er vidt udbredt i hydrosfæren og endda i fugtig jord. De spiller vigtige roller i globale
Strukturen af fotosystemprotein-superkompleks fra diatom afslører dets meget sofistikerede energi…Overordnet struktur af PSI-FCPI superkomplekset. Kredit:IBCAS Kiselalger er en gruppe af fytoplankton, der er vidt udbredt i hydrosfæren og endda i fugtig jord. De spiller vigtige roller i globale
- Sådan fryser du varmeledning
- Indikatorer viser, at kartofler kan vokse på Mars
- Det britiske parlament beder Zuckerberg om at vidne i sager om misbrug af data
- En mulig ny måde at køle computerchips på
- Hvilken farve går rødkål, når du tilføjer alkali?
- Kvantecomputere er som kalejdoskoper:Hvorfor usædvanlige metaforer hjælper med at illustrere viden…


