Hvad er standardentalpiændringen for reaktion, der repræsenterer at bryde alle bindinger i gasformig benzen?
$$6(348\tekst{ kJ/mol})+6(413 \text{ kJ/mol)}=4554\tekst{ kJ/mol}$$
Standardentalpiændringen for reaktionen, der repræsenterer at bryde alle bindinger i gasformig benzen, er den negative af den samlede bindingsentalpi, så:
$$\Delta H°=-4554 \text{ kJ/mol} =\boxed{-1129 \text{ kJ/mol}}$$
Sidste artikelHvad er oxidationstallet for LiBr?
Næste artikelHvad er synonym for giftig?
 Varme artikler
Varme artikler
-
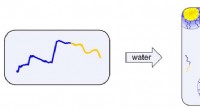 En ny, hurtigere måde at behandle diblok-polymermaterialer påDen blå ende af hver kæde er opløselig i vand, mens den gule ende ikke er det. De gule ender samler sig i et forsøg på at adskille fra vandet. Disse kugleformede klynger kaldes miceller. Kredit:Connor
En ny, hurtigere måde at behandle diblok-polymermaterialer påDen blå ende af hver kæde er opløselig i vand, mens den gule ende ikke er det. De gule ender samler sig i et forsøg på at adskille fra vandet. Disse kugleformede klynger kaldes miceller. Kredit:Connor -
 Innovation kan forbedre opdagelsen af COVID-19-infektionerKredit:Pixabay/CC0 Public Domain Et tværfagligt forskerhold ved National Institute of Standards and Technology (NIST) har udviklet en måde at øge følsomheden af den primære test, der bruges til
Innovation kan forbedre opdagelsen af COVID-19-infektionerKredit:Pixabay/CC0 Public Domain Et tværfagligt forskerhold ved National Institute of Standards and Technology (NIST) har udviklet en måde at øge følsomheden af den primære test, der bruges til -
 Forskere udvikler forbedret genbrugsproces for kulfiberKredit:Unsplash/CC0 Public Domain Genbrug af kompositmaterialer kan være op til 70 procent billigere og føre til en reduktion i CO på 90-95 procent 2 emissioner sammenlignet med standardfremstil
Forskere udvikler forbedret genbrugsproces for kulfiberKredit:Unsplash/CC0 Public Domain Genbrug af kompositmaterialer kan være op til 70 procent billigere og føre til en reduktion i CO på 90-95 procent 2 emissioner sammenlignet med standardfremstil -
 Kollagen kan modstå flere belastninger end hidtil kendtKredit:CC0 Public Domain Forskere ved Institut for Fysik ved Kings College i London har opdaget, at kollagenfibriller kan modstå en væsentlig større belastning end tidligere antaget, udvide vores
Kollagen kan modstå flere belastninger end hidtil kendtKredit:CC0 Public Domain Forskere ved Institut for Fysik ved Kings College i London har opdaget, at kollagenfibriller kan modstå en væsentlig større belastning end tidligere antaget, udvide vores
- Forskere genererer optiske skyrmions
- Amazons seneste milepæl:150 millioner Prime -medlemmer
- Hvordan vil du beskrive reproduktionssystemets funktion?
- Det seismiske smell af tropiske cykloner
- USA siger, at der ikke er grundlag for at sætte Boeing 737 MAX-jetfly på jorden efter styrt
- Fuldt epitaksielle mikrohulrum:Åbn døren for kvanteoptoelektroniske effekter i det GaN-baserede sy…


