Hvilke dele af atomet er involveret, når natrium reagerer med andre grundstoffer?
Natrium har en valenselektron i den yderste skal af sit atom. Denne elektron er relativt svagt bundet til atomets kerne, hvilket betyder, at den let kan fjernes eller deles med andre atomer. Når natrium reagerer med et andet grundstof, overføres eller deles natriums valenselektron typisk med det andet grundstof, hvilket resulterer i dannelsen af en kemisk binding.
Generelt har natrium en tendens til at reagere ved at miste sin ene valenselektron og blive positivt ladet (en natriumion). Denne proces kaldes ionisering. For eksempel, når natrium reagerer med klor, donerer natriumatomet sin valenselektron til kloratomet, hvilket resulterer i dannelsen af natriumchlorid (NaCl). Natriumatomet bliver til en natriumion (Na+), mens kloratomet får en elektron og bliver til en chloridion (Cl-).
At forstå opførselen af valenselektroner er afgørende for at forstå de kemiske reaktioner og egenskaber af ikke kun natrium, men også alle andre elementer. Kemiske reaktioner involverer overførsel, deling eller omlejring af valenselektroner mellem atomer, hvilket fører til dannelsen af nye bindinger og forbindelser med særskilte egenskaber.
Sidste artikelHvorfor skal du bruge koldt vand i perkolatoren?
Næste artikelHvad er brugen af natriumbicarbonat i toffee?
 Varme artikler
Varme artikler
-
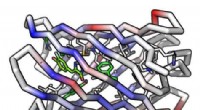 Fluorescensaktiverende beta-tøndeprotein lavet fra bunden for første gangEn computermodel af et beta-tønde-proteinmolekyle Kredit:Institute for Protein Design/UW Medicine For første gang, videnskabsmænd har skabt, helt fra bunden, et protein, der er i stand til at bind
Fluorescensaktiverende beta-tøndeprotein lavet fra bunden for første gangEn computermodel af et beta-tønde-proteinmolekyle Kredit:Institute for Protein Design/UW Medicine For første gang, videnskabsmænd har skabt, helt fra bunden, et protein, der er i stand til at bind -
 Opfindelsen af bittesmå organiske film kunne muliggøre ny elektronikForskere opdagede en ny metode til at samle tusindvis af organiske molekyler til en glat flad film, kun få nanometer tyk, vist her i denne illustration. Kredit:Baorui Cheng Den første mobiltelefon
Opfindelsen af bittesmå organiske film kunne muliggøre ny elektronikForskere opdagede en ny metode til at samle tusindvis af organiske molekyler til en glat flad film, kun få nanometer tyk, vist her i denne illustration. Kredit:Baorui Cheng Den første mobiltelefon -
 Smart dug kan finde frugt og hjælpe med at vande planterneDet smarte Capacitivo -stof kan identificere frugt og finde tabte genstande. Samlet set, systemet opnåede en 94,5% nøjagtighed i test. Kredit:Figur med tilladelse fra XDiscovery Lab. Forskere har
Smart dug kan finde frugt og hjælpe med at vande planterneDet smarte Capacitivo -stof kan identificere frugt og finde tabte genstande. Samlet set, systemet opnåede en 94,5% nøjagtighed i test. Kredit:Figur med tilladelse fra XDiscovery Lab. Forskere har -
 Forskere forenkler og strømliner organisk kemisk syntese dramatiskFor første gang opdagede forskere en enkel og yderst effektiv måde at fremstille visse former for organiske forbindelser på. Holdet fra Institut for Kemi ved University of Tokyo rapporterer, at deres
Forskere forenkler og strømliner organisk kemisk syntese dramatiskFor første gang opdagede forskere en enkel og yderst effektiv måde at fremstille visse former for organiske forbindelser på. Holdet fra Institut for Kemi ved University of Tokyo rapporterer, at deres
- Hvad er oxidationstallet for H2CO2?
- Vej, form og form:Synteseforhold definerer nanostrukturen af mangandioxid
- Flugtkunstnere:Hvordan vibriobakterier bryder ud af celler
- Genetiske test viser, at centrale australske palmer afveg fra det nordlige mere for nylig end antage…
- Ny tilgang til sammenhængende kontrol af et kvantesystem på tre niveauer
- Panelet diskuterer virkningerne af Red Tide på Florida


