Har ioniske forbindelser eller kovalent stærkere intermolekylære kræfter?
I ioniske forbindelser er de intermolekylære kræfter elektrostatiske tiltrækningskræfter mellem positivt og negativt ladede ioner. Disse kræfter er meget stærke og kræver en stor mængde energi at overvinde. I kovalente forbindelser er de intermolekylære kræfter meget svagere. De er forårsaget af tiltrækningen mellem de lidt positive og negative ender af polære molekyler. Disse kræfter er meget svagere end de elektrostatiske kræfter i ioniske forbindelser og kan let overvindes.
Sidste artikelEr attraktioner blandt ioner inden for et krystalgitter svage?
Næste artikelHvad er smelte- og kogepunktet for zinkoxid?
 Varme artikler
Varme artikler
-
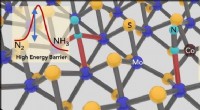 Ammoniaksyntese gjort let med 2-D katalysatorTilsætning af koboltatomer til fyldning af ledige pladser i 2D molybdendisulfidkrystaller øger materialets evne til at katalysere ammoniak fra dinitrogen. Forskere fra Rice University har udviklet en
Ammoniaksyntese gjort let med 2-D katalysatorTilsætning af koboltatomer til fyldning af ledige pladser i 2D molybdendisulfidkrystaller øger materialets evne til at katalysere ammoniak fra dinitrogen. Forskere fra Rice University har udviklet en -
 Forskere trykker på lasere for at efterligne hajhud, andre naturlige overfladerCraig Zuhlke (til venstre), en forskningsadjunkt, og Aaron Ediger, en færdiguddannet forskningsassistent, se, hvordan en laser modificerer en lille prøve af metal. Forskningen, ledet af Nebraskas Denn
Forskere trykker på lasere for at efterligne hajhud, andre naturlige overfladerCraig Zuhlke (til venstre), en forskningsadjunkt, og Aaron Ediger, en færdiguddannet forskningsassistent, se, hvordan en laser modificerer en lille prøve af metal. Forskningen, ledet af Nebraskas Denn -
 At se kemiske reaktioner med musik(Top) Lydkontrollerede spatiotemporale mønstre. Skematisk repræsentation af eksperimentel opsætning brugt til lydstyret spatiotemporal mønstergenerering. For mønstergenereringseksperimenter, O2-følsom
At se kemiske reaktioner med musik(Top) Lydkontrollerede spatiotemporale mønstre. Skematisk repræsentation af eksperimentel opsætning brugt til lydstyret spatiotemporal mønstergenerering. For mønstergenereringseksperimenter, O2-følsom -
 Laserbehandling viser potentiale for at reducere industriel kemisk behandling af køretøjerORNL-forsker Adrian Sabau beskriver komponenter i et laserinterferensstruktureringssystem, der blev brugt til at behandle aluminiumslegeringsplader til korrosionsbeskyttelse. Kredit:Carlos Jones/ORNL,
Laserbehandling viser potentiale for at reducere industriel kemisk behandling af køretøjerORNL-forsker Adrian Sabau beskriver komponenter i et laserinterferensstruktureringssystem, der blev brugt til at behandle aluminiumslegeringsplader til korrosionsbeskyttelse. Kredit:Carlos Jones/ORNL,
- Undersøgelse:Aerosoler har en overdreven indvirkning på ekstremt vejr
- Forskere udvikler en bedre måde at udnytte solpanelernes kraft på
- Skjolder op for at slå den globale opvarmning
- Mikrobielt fremstillede fibre:Stærkere end stål, hårdere end Kevlar
- Auto-Gopher – borer dybt for at udforske solsystemet
- Fysikere spørger:Kan vi gøre en partikelkolliderer mere energieffektiv?


