Kan anioner klassificeres som sure eller basiske?
Når en anion opløses i vand, kan den gennemgå en af to reaktioner:
1. Sure anioner: Disse anioner reagerer med vand og danner en syre og en hydroxidion. For eksempel, når kuldioxid (CO2) opløses i vand, reagerer det med vand og danner kulsyre (H2CO3) og hydroxidioner (OH-).
CO2 + H2O ⇌ H2CO3 + OH-
2. Grundlæggende anioner: Disse anioner reagerer med vand og danner en base og en hydrogenion. For eksempel, når natriumcarbonat (Na2CO3) opløses i vand, reagerer det med vand og danner natriumhydroxid (NaOH) og hydrogenioner (H+).
Na2CO3 + H2O ⇌ 2NaOH + H+
Styrken af en syre eller base bestemmes af, i hvor høj grad den dissocierer i vand. Stærke syrer og baser dissocierer fuldstændigt i vand, mens svage syrer og baser kun adskilles delvist.
Klassificeringen af anioner som sure eller basiske er vigtig for at forstå kemien i vandige opløsninger. For eksempel er pH-værdien af en opløsning bestemt af koncentrationen af hydrogenioner (H+). Tilsætning af en sur anion til en opløsning vil øge koncentrationen af H+ ioner og sænke pH, mens tilsætning af en basisk anion vil mindske koncentrationen af H+ ioner og hæve pH.
Sidste artikelEr jernoxid surt eller basisk?
Næste artikelEr Al203 og N203 en binær ionisk forbindelse eller kovalent forbindelse?
 Varme artikler
Varme artikler
-
 Forskere opdager materiale, der er ideelt til smarte solcellevinduerFremskyndede video af materiale, der skifter fra lav-T- til høj-T-fase. Kredit:Berkeley Lab Smarte vinduer, der er gennemsigtige, når det er mørkt eller køligt, men som automatisk bliver mørkere,
Forskere opdager materiale, der er ideelt til smarte solcellevinduerFremskyndede video af materiale, der skifter fra lav-T- til høj-T-fase. Kredit:Berkeley Lab Smarte vinduer, der er gennemsigtige, når det er mørkt eller køligt, men som automatisk bliver mørkere, -
 Magnetisk materialeanalyse har aldrig været så forståeligSpin struktur (tykke pile) omkring et sfærisk nanostørrelse hul eller pore (i blåt) i en magnetisk matrix (i lysegrå). Magnetisk SANS kan detektere og analysere sådanne strukturer. Kredit:University o
Magnetisk materialeanalyse har aldrig været så forståeligSpin struktur (tykke pile) omkring et sfærisk nanostørrelse hul eller pore (i blåt) i en magnetisk matrix (i lysegrå). Magnetisk SANS kan detektere og analysere sådanne strukturer. Kredit:University o -
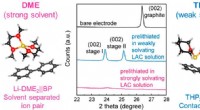 En innovativ proces forhindrer irreversibelt energitab i batterieren kemisk prelithieringsmetode til at maksimere ICE for blandingsanoderne ved hjælp af en reduktiv Li-arene kompleks løsning med reguleret solvationskraft, som gør det muligt for en fuld celle at udvi
En innovativ proces forhindrer irreversibelt energitab i batterieren kemisk prelithieringsmetode til at maksimere ICE for blandingsanoderne ved hjælp af en reduktiv Li-arene kompleks løsning med reguleret solvationskraft, som gør det muligt for en fuld celle at udvi -
 Biokemikere dykker ned i sundhedsmæssige fordele ved oliven og olivenolieOlivenolie hældes over mad. Kredit:Centers for Disease Control and Prevention. Sundhedsmæssige fordele ved oliven - og tilhørende naturprodukter som olivenolie - er længe blevet anerkendt og udråb
Biokemikere dykker ned i sundhedsmæssige fordele ved oliven og olivenolieOlivenolie hældes over mad. Kredit:Centers for Disease Control and Prevention. Sundhedsmæssige fordele ved oliven - og tilhørende naturprodukter som olivenolie - er længe blevet anerkendt og udråb
- Ny verdensrekord for direkte solvandsspaltningseffektivitet
- Skolelukninger kan have udslettet et års akademiske fremskridt for elever i Global South
- Brug af kulsyreholdigt vand i kromatografi giver en grønnere proces, viser ny undersøgelse
- NASA fanger den tropiske storm Franciscos tilgang til landgang i det sydlige Japan
- Udvikling af en måde at gøre oxygen injicerbar
- Amerikanske spådommere:Forvent næsten normal atlantisk orkansæson


