Har NH3 en polær binding?
Elektronegativiteten af nitrogen (N) er 3,0, mens elektronegativiteten for brint (H) er 2,1. Det betyder, at N har en stærkere tiltrækning af elektroner end H. Som følge heraf trækkes elektronparret i N-H-bindingen tættere på N, hvilket skaber en delvis negativ ladning på N og en delvis positiv ladning på H. Dette resulterer i en polær ladning. bånd.
Polariteten af N-H-bindingen giver også anledning til den samlede polaritet af NH3-molekylet. Nitrogenatomet har en delvis negativ ladning, mens de tre brintatomer har en delvis positiv ladning. Dette skaber en netto positiv ladning på hydrogensiden af molekylet og en netto negativ ladning på nitrogensiden. Dette gør NH3 til et polært molekyle.
 Varme artikler
Varme artikler
-
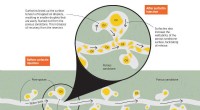 Manipulerer overfladespænding i væsker, der passer til forskellige industrielle behovKredit:Agency for Science, Teknologi og forskning (A*STAR), Singapore Hvad har opvaskemiddel og nonstick -pander tilfælles? Udover at den ene bruges til at rense den anden efter madlavning, begge
Manipulerer overfladespænding i væsker, der passer til forskellige industrielle behovKredit:Agency for Science, Teknologi og forskning (A*STAR), Singapore Hvad har opvaskemiddel og nonstick -pander tilfælles? Udover at den ene bruges til at rense den anden efter madlavning, begge -
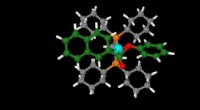 Enkel bytte til et grønnere værktøjskasseEn bidentat ligand (orange og grå) på nikkelatomet (blå) fremmer eliminering af carbonyl i esteren (grøn og rød) i denne overgangstilstand. Kredit:KAUST En metalkatalysator, der giver tydelige car
Enkel bytte til et grønnere værktøjskasseEn bidentat ligand (orange og grå) på nikkelatomet (blå) fremmer eliminering af carbonyl i esteren (grøn og rød) i denne overgangstilstand. Kredit:KAUST En metalkatalysator, der giver tydelige car -
 Eleven bruger planteaffald til at skabe et bæredygtigt alternativ til farvestofKredit:Imperial College London Kejserstuderende Nicole Stjernswärd bruger planteaffald til at skabe naturlige pulverpigmenter, der kan bruges til maling, blæk eller tekstiler. Historisk set kom f
Eleven bruger planteaffald til at skabe et bæredygtigt alternativ til farvestofKredit:Imperial College London Kejserstuderende Nicole Stjernswärd bruger planteaffald til at skabe naturlige pulverpigmenter, der kan bruges til maling, blæk eller tekstiler. Historisk set kom f -
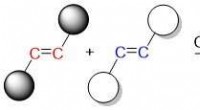 Jernkatalysator kunne gøre vigtige kemiske reaktioner billigere og mere miljøvenligeOlefinmetatesereaktionen producerer nye carbon-carbon dobbeltbindinger ved at bryde de oprindelige dobbeltbindinger og regenerere nye. Kredit:OIST En katalysator er en nøgleingrediens i mange kemis
Jernkatalysator kunne gøre vigtige kemiske reaktioner billigere og mere miljøvenligeOlefinmetatesereaktionen producerer nye carbon-carbon dobbeltbindinger ved at bryde de oprindelige dobbeltbindinger og regenerere nye. Kredit:OIST En katalysator er en nøgleingrediens i mange kemis
- Et stænk er alt i vinklen
- Axing Lightning til iPhone ville betyde hidtil uset e-affald, siger Apple
- Materialeforskere viser måde at lave holdbare kunstige sener fra forbedrede hydrogeler
- Sådan fungerer isskulptur
- Forskere ser på jordbund og lærer, hvordan skove påvirker luftkvaliteten, klimaændringer
- Oplyser vejen til superopløsningsbilleddannelse med forbedrede rhodaminfarvestoffer


