Hvorfor er det muligt for et oxygenatom at danne en dobbelt kovalent binding, men ikke klorbinding?
 Varme artikler
Varme artikler
-
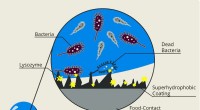 Ny dobbeltvirkende belægning forhindrer bakterier i at krydskontaminere friske produkterSkematisk, der viser Dr. Mustafa Akbuluts dobbeltfunktionsbelægning, der er både superhydrofob og antimikrobiel. Kredit:Texas A&M University College of Engineering I løbet af deres rejse fra de åb
Ny dobbeltvirkende belægning forhindrer bakterier i at krydskontaminere friske produkterSkematisk, der viser Dr. Mustafa Akbuluts dobbeltfunktionsbelægning, der er både superhydrofob og antimikrobiel. Kredit:Texas A&M University College of Engineering I løbet af deres rejse fra de åb -
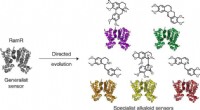 Forskere kaprer bakterier for at lette lægemiddelfremstillingenKredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01072-w For mere overkommelige, bæredygtige medicinmuligheder, end vi har i dag, kan den medicin, vi tager til behandling af forhøjet b
Forskere kaprer bakterier for at lette lægemiddelfremstillingenKredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01072-w For mere overkommelige, bæredygtige medicinmuligheder, end vi har i dag, kan den medicin, vi tager til behandling af forhøjet b -
 Laserbaseret teknik til at belyse exosomers mysterierExosomer er små vesikler frigivet af celler, der menes at være vigtige for cellekommunikation og regulering. De vil sandsynligvis også spille en rolle i tumorprogression og kræft. Kredit:Shutterstock
Laserbaseret teknik til at belyse exosomers mysterierExosomer er små vesikler frigivet af celler, der menes at være vigtige for cellekommunikation og regulering. De vil sandsynligvis også spille en rolle i tumorprogression og kræft. Kredit:Shutterstock -
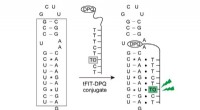 Ny måde at identificere influenza A-virus lyser op, når specifikke virusmål er til stedeSkematisk illustration af fluorescensføling af panhandle-strukturen af IAV RNA-promotorregionen (angivet i boksen). Kredit:tFIT-DPQ sonde. Influenza A-virus, som er ansvarlig for sæsonbestemte in
Ny måde at identificere influenza A-virus lyser op, når specifikke virusmål er til stedeSkematisk illustration af fluorescensføling af panhandle-strukturen af IAV RNA-promotorregionen (angivet i boksen). Kredit:tFIT-DPQ sonde. Influenza A-virus, som er ansvarlig for sæsonbestemte in
- Roll-to-roll proces udskriver tusindvis af billige, fleksible hukommelseselementer
- Undersøgelse afslører vigtige kursusfunktioner, der tiltrækker forskellige studerende
- At bygge bro over kløften:Dataloger udvikler model til at forbedre vanddata fra satellitter
- Forskere udvikler ny metode til at detektere ilt på exoplaneter
- Hvor kan vand i gasform findes?
- Vi lægger alle for meget vægt på testresultater


