Er HC1 en ionbinding eller en kovalent binding?
For at bestemme typen af binding mellem to atomer skal vi overveje deres elektronegativitet. Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en kemisk binding. Forskellen i elektronegativitet mellem to atomer bestemmer bindingens polaritet.
I tilfælde af HCl er elektronegativiteten af brint 2,20, mens elektronegativiteten af chlor er 3,00. Forskellen i elektronegativitet mellem brint og klor er 0,80. Denne forskel er stor nok til at skabe en polær kovalent binding, hvor elektronerne deles ulige mellem de to atomer.
Brintatomet har en svag positiv ladning, mens kloratomet har en svag negativ ladning. Denne polaritet er det, der giver HCl dets sure egenskaber. Når HCl opløses i vand, donerer brintatomet sin proton (H+) til vandmolekylet og danner H3O+ og Cl-ioner.
 Varme artikler
Varme artikler
-
 Video:Hvorfor ændrer salt smagen af alting?Kredit:The American Chemical Society Hvis din kaffe er for bitter, tilsæt en knivspids salt. Hvis din salat ikke er sur nok, tilsæt et nip salt. Hvis din øl er for bitter, tilsæt en knivspids salt.
Video:Hvorfor ændrer salt smagen af alting?Kredit:The American Chemical Society Hvis din kaffe er for bitter, tilsæt en knivspids salt. Hvis din salat ikke er sur nok, tilsæt et nip salt. Hvis din øl er for bitter, tilsæt en knivspids salt. -
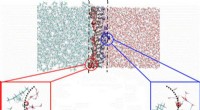 Toppe af vandige bølger kan transportere vitale kemikalier i industriel separationsprocesHvordan molekyler bevæger sig og organiserer sig i vand, når væsken møder olien, afhænger af, om kemikaliet er på toppen eller truget af en lille bølge af vand ved grænsefladen. Kredit:US Department o
Toppe af vandige bølger kan transportere vitale kemikalier i industriel separationsprocesHvordan molekyler bevæger sig og organiserer sig i vand, når væsken møder olien, afhænger af, om kemikaliet er på toppen eller truget af en lille bølge af vand ved grænsefladen. Kredit:US Department o -
 Forskere rapporterer om en bedre måde at skabe organisk bioelektronik påDette billede viser ledende polymermikrokopper, der bruges til organisk bioelektronik og lægemiddelleveringsapplikationer. Kredit:Milad Khorrami &Mohammad Reza Abidian, University of Houston Med s
Forskere rapporterer om en bedre måde at skabe organisk bioelektronik påDette billede viser ledende polymermikrokopper, der bruges til organisk bioelektronik og lægemiddelleveringsapplikationer. Kredit:Milad Khorrami &Mohammad Reza Abidian, University of Houston Med s -
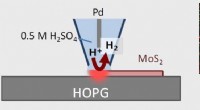 Billedbehandlingsteknik giver katalytisk 2-D materialeteknik et bedre udsynScanning elektrokemisk cellemikroskopi (SECCM) muliggør billeddannelse og kvantitativ analyse af hydrogenudviklingsreaktion (HER) katalytisk aktive steder i 1H MoS 2 monolag. Kredit:Kanazawa Univers
Billedbehandlingsteknik giver katalytisk 2-D materialeteknik et bedre udsynScanning elektrokemisk cellemikroskopi (SECCM) muliggør billeddannelse og kvantitativ analyse af hydrogenudviklingsreaktion (HER) katalytisk aktive steder i 1H MoS 2 monolag. Kredit:Kanazawa Univers
- Dybhavsminedrift:Er det en miljømæssig forbandelse eller kan det redde os?
- Blåt pigment fra manipulerede svampe kan hjælpe med at gøre tekstilindustrien grøn
- Hvorfor kommer Andromeda imod os?
- Hvordan tre timer kunne lægge op til en bedre pension
- Hvis du tilføjer en lille mængde saltsyre til 4 liter vand, hvilken type opløsning ville du forve…
- Navngivning af unavngivne bakteriearter i big data-alderen


