Hvordan adskiller kaliumhydroxid sig fra fortyndet salpetersyre?
1. Kemisk formel :
- Kaliumhydroxid:KOH
- Fortyndet salpetersyre:HNO3 (med vand)
2. Fysiske egenskaber :
- Udseende :
- KOH:Hvidt eller farveløst, krystallinsk fast stof
- Fortyndet HNO3:Farveløs til bleggul væske
- Lugt :
- KOH:Lugtfri
- Fortyndet HNO3:Skarp, skarp lugt
3. pH-niveau :
- KOH:Stærkt basisk (pH> 11)
- Fortyndet HNO3:Stærkt surt (pH <1)
4. Opløselighed :
- KOH:Meget opløseligt i vand, opløses i kaliumioner (K+) og hydroxidioner (OH-).
- Fortyndet HNO3:Fuldstændig opløselig i vand og danner hydroniumioner (H3O+) og nitrationer (NO3-).
5. Reaktivitet :
- KOH er meget reaktivt :
- Reagerer med syrer og danner salte og vand.
- Ætsende på hud og væv, kan forårsage alvorlige forbrændinger.
- Fortyndet HNO3 er moderat reaktivt :
- Reagerer med metaller og danner salte og brintgas.
- Kan reagere med organiske forbindelser og forårsage oxidationsreaktioner.
6. Ansøgninger :
- KOH :
- Anvendes til fremstilling af sæbe og vaskemidler.
- Elektrolyt i alkaliske batterier.
- Produktion af kunstgødning.
- Fortynd HNO3 :
- Anvendes til fremstilling af kunstgødning.
- Laboratoriereagens til syre-base reaktioner og metalopløsning.
- Ætsning og gravering af metaller.
7. Sikkerhed :
- Begge forbindelser kræver korrekt håndtering og sikkerhedsforanstaltninger på grund af deres ætsende natur.
- KOH kan være ætsende og forårsage hudirritation, mens fortyndet HNO3 kan frigive giftige dampe.
Det er vigtigt at bemærke, at egenskaberne af fortyndet salpetersyre kan variere afhængigt af dens koncentration. Oplysningerne her gælder for fortyndet salpetersyre, typisk med en koncentration på omkring 10% til 20%.
Sidste artikelOpnåede atomerne stabilitet efter ionbinding Forklar?
Næste artikelHvor mange mol CH4 er der i 6,07 g (CH4)?
 Varme artikler
Varme artikler
-
 En blidere, mere præcis laserskæringsteknikPac-Man udskæring ved laserskæring. Kredit:H. Borchers et al. Laserskæringsteknikker drives normalt af højenergistråler, så varme, at de smelter de fleste materialer. Nu har forskere fra McGill Uni
En blidere, mere præcis laserskæringsteknikPac-Man udskæring ved laserskæring. Kredit:H. Borchers et al. Laserskæringsteknikker drives normalt af højenergistråler, så varme, at de smelter de fleste materialer. Nu har forskere fra McGill Uni -
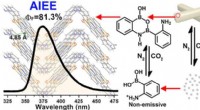 Nyt aggregationsinduceret aromatisk molekyle med forbedret emission opdaget2-APBA-dimeren, der har tendens til at aggregere til en meget ordnet struktur, er AIEE-aktiv. Kredit:LI Xiaopei Aggregations-inducerede molekyler med øget emission (AIEE), nye selvlysende material
Nyt aggregationsinduceret aromatisk molekyle med forbedret emission opdaget2-APBA-dimeren, der har tendens til at aggregere til en meget ordnet struktur, er AIEE-aktiv. Kredit:LI Xiaopei Aggregations-inducerede molekyler med øget emission (AIEE), nye selvlysende material -
 Naturinspireret krystalstruktur forudsigelseForskere fra Rusland fandt en måde at forbedre forudsigelsesalgoritmerne for krystalstruktur, gør opdagelsen af nye forbindelser flere gange hurtigere. Kredit:MIPT Forskere fra Rusland har rappo
Naturinspireret krystalstruktur forudsigelseForskere fra Rusland fandt en måde at forbedre forudsigelsesalgoritmerne for krystalstruktur, gør opdagelsen af nye forbindelser flere gange hurtigere. Kredit:MIPT Forskere fra Rusland har rappo -
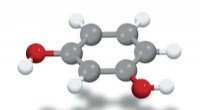 Selektiv syntese af meta-isomerer nu muligFigur 1:En molekylær model af 1,3-dihydroxybenzen (grå kugler:carbonatomer; røde kugler:oxygenatomer; hvide kugler:hydrogenatomer), meta-isomeren af dihydroxybenzen. Et team på RIKEN har udviklet en
Selektiv syntese af meta-isomerer nu muligFigur 1:En molekylær model af 1,3-dihydroxybenzen (grå kugler:carbonatomer; røde kugler:oxygenatomer; hvide kugler:hydrogenatomer), meta-isomeren af dihydroxybenzen. Et team på RIKEN har udviklet en
- EU sætter højere mål for vedvarende energi i 2030
- Molekyler udviser ikke-gensidige interaktioner uden eksterne kræfter, finder ny undersøgelse
- Hvordan røg genereret fra store naturbrande kan påvirke det lokale vejr og gøre brande værre
- Livet på Mars:simulerer Red Planet-base i israelsk ørken
- Undersøgelse:Grøn te kan ændre, hvordan vi opfatter smag
- Hvilket metal danner 3 ioner?


