Hvad er konjugeret syre-basepar?
Her er en forenklet forklaring:
1. Syre: En syre er et stof, der kan donere en proton (H+ ion) i en kemisk reaktion.
2. Base: En base er et stof, der kan acceptere en proton (H+ ion) i en kemisk reaktion.
3. Konjugeret syre: Når en base accepterer en proton, bliver den til den konjugerede syre.
4. Konjugeret base: Når en syre donerer en proton, kaldes den dannede art den konjugerede base.
Lad os for eksempel overveje følgende reaktion:
Syre (HA): HCl (saltsyre)
Basis (B): NH3 (ammoniak)
Reaktion: HCl + NH3 → NH4+ (ammoniumion) + Cl- (chloridion)
I denne reaktion donerer HCl en proton til NH3 og danner den konjugerede syre NH4+ (ammoniumion). Samtidig dannes Cl- (chloridion) som konjugatbasen af HCl.
NH4+-ionen er den konjugerede syre af NH3, og Cl- er den konjugerede base af HCl.
I det væsentlige består et konjugeret syre-base-par af en art, der kan donere en proton, og dens tilsvarende art, der accepterer den proton. Disse par spiller en afgørende rolle i mange kemiske reaktioner, såsom syre-basereaktioner, protonoverførselsreaktioner og buffersystemer.
Sidste artikelHvad er et konjugeret syrepar?
Næste artikelHvordan udvindes guld fra aurinchlorid?
 Varme artikler
Varme artikler
-
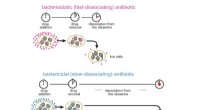 At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv
At lære antibiotika at være mere effektive dræbereForskning viser, at langvarig hæmning af proteinsyntese fører til celledød. Kredit:Proceedings of the National Academy of Sciences Forskning fra University of Illinois i Chicago tyder på bindingsv -
 Immunterapi for dødelige bakterier viser tidligt lovendeVed at stimulere immunsystemet til at ødelægge patogener, Marcos Pires håber at udvikle alternative behandlinger for bakterier, der er resistente over for antibiotika. Kredit:Douglas Benedict/Academic
Immunterapi for dødelige bakterier viser tidligt lovendeVed at stimulere immunsystemet til at ødelægge patogener, Marcos Pires håber at udvikle alternative behandlinger for bakterier, der er resistente over for antibiotika. Kredit:Douglas Benedict/Academic -
 Nyt tekstil kan holde dig kølig i varmen, varm i kuldenEn mikrostruktureret fiber (til venstre) indeholder porer (til højre), der kan fyldes med et faseskiftende materiale, der absorberer og frigiver termisk energi. Kredit: ACS anvendte materialer og græn
Nyt tekstil kan holde dig kølig i varmen, varm i kuldenEn mikrostruktureret fiber (til venstre) indeholder porer (til højre), der kan fyldes med et faseskiftende materiale, der absorberer og frigiver termisk energi. Kredit: ACS anvendte materialer og græn -
 Præcis definerede polymerkæder er nu en realitetDen nye molekyleforbindelsesteknik kan forestilles som tre adskilte jernbanevogne, hver har to unikke koblinger i hver ende, kun tillader dem at blive koblet i en bestemt rækkefølge. Kredit:Takeharu H
Præcis definerede polymerkæder er nu en realitetDen nye molekyleforbindelsesteknik kan forestilles som tre adskilte jernbanevogne, hver har to unikke koblinger i hver ende, kun tillader dem at blive koblet i en bestemt rækkefølge. Kredit:Takeharu H
- Sådan fungerer speciel relativitet
- David vs. Goliat:Hvad en lille elektron kan fortælle os om universets struktur
- Hurtig, pålidelig test for forurening af mikroorganismer
- Mars Relay Network forbinder Jorden med NASAs robotudforskere
- 3D-udskrivning hierarkiske flydende krystal-polymerstrukturer
- Bæredygtighed i populistisk tid


