Beregn antallet af molekyler i 9 g CO2?
1. Bestem den molære masse af CO2:
Den molære masse af CO2 er summen af de molære masser af et carbonatom (12,01 g/mol) og to oxygenatomer (2 x 16,00 g/mol):
Molær masse af CO2 =12,01 g/mol + 2 x 16,00 g/mol =44,01 g/mol
2. Omregn den givne masse af CO2 til mol:
Antal mol CO2 =Masse CO2 / Molær masse CO2
Antal mol CO2 =9 g / 44,01 g/mol =0,2045 mol
3. Avogadros nummer:
Avogadros tal (Nₐ) repræsenterer antallet af partikler (atomer, molekyler eller ioner), der er til stede i et mol af et stof. Det har en værdi på 6,022 x 10^23 partikler/mol.
4. Beregn antallet af molekyler:
Antallet af molekyler i 0,2045 mol CO2 kan beregnes ved at gange antallet af mol med Avogadros tal:
Antal molekyler =Antal mol x Avogadros antal
Antal molekyler =0,2045 mol x 6,022 x 10^23 molekyler/mol ≈ 1,23 x 10^23 molekyler
Derfor er der cirka 1,23 x 10^23 molekyler i 9 g CO2.
Sidste artikelHvad er forskellen mellem nitrogen og nitro?
Næste artikelHvad er mere reatice fluor eller klor?
 Varme artikler
Varme artikler
-
 Innovativ behandling forhindrer spredning af bakterier på tværs af metaloverfladerDette billede viser en peptidfrigivelsestest, med den øgede lilla farve, der viser, at flere peptider frigives. Kredit:Purdue University Forskere ved Purdue University har udviklet en behandling t
Innovativ behandling forhindrer spredning af bakterier på tværs af metaloverfladerDette billede viser en peptidfrigivelsestest, med den øgede lilla farve, der viser, at flere peptider frigives. Kredit:Purdue University Forskere ved Purdue University har udviklet en behandling t -
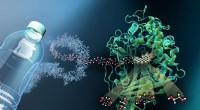 Forskere karakteriserer molekylær sakse til plastaffaldBilledet viser strukturen af MHETase bundet til en ikke-hydrolyserbar PET-afledt ligand (MHETA). Symbolske polymerfibre forbinder MHETA med en typisk PET-flaske, hvilket indikerer det store potentia
Forskere karakteriserer molekylær sakse til plastaffaldBilledet viser strukturen af MHETase bundet til en ikke-hydrolyserbar PET-afledt ligand (MHETA). Symbolske polymerfibre forbinder MHETA med en typisk PET-flaske, hvilket indikerer det store potentia -
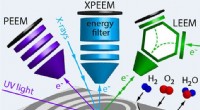 Tre mikroskoper ser mere end toGrafisk abstrakt. Kredit:ACS Catalysis (2022). DOI:10.1021/acscatal.2c03692 Man skal se meget nøje for at forstå, hvilke processer der finder sted på overfladerne af katalysatorer. Faste katalysato
Tre mikroskoper ser mere end toGrafisk abstrakt. Kredit:ACS Catalysis (2022). DOI:10.1021/acscatal.2c03692 Man skal se meget nøje for at forstå, hvilke processer der finder sted på overfladerne af katalysatorer. Faste katalysato -
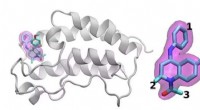 Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
- Hvordan geparder finder hinanden efter adskillelse
- Stort fremskridt i forståelsen af, hvordan nanotråde dannes
- Fremskynde udviklingen af fusionskraft for at skabe ubegrænset energi på Jorden
- Hvilket hovedvæv beklæder kroppens hulrum og dækker den ydre overflade?
- Hvad Facebooks 'privatlivsvision' egentlig betyder
- Astronomer kan have afsløret, hvordan galakser ændrer deres form


