Hvad sagde atomteorien?
1. Lov om bevarelse af messen :Under en kemisk reaktion er den samlede masse af produkterne altid lig med den samlede masse af reaktanterne. Dette princip fastslog, at stof ikke kan skabes eller ødelægges under kemiske ændringer.
2. Lov om bestemte proportioner :Når grundstoffer kombineres for at danne forbindelser, gør de det i faste og bestemte forhold efter masse. Forholdet mellem grundstoffernes masser i en forbindelse er konstant uanset mængden af forbindelsen.
3. Lov om flere proportioner :Når to grundstoffer danner mere end én forbindelse, er masserne af det ene grundstof, der kombineres med en fast masse af det andet grundstof, i simple, hele talforhold.
4. Atomstruktur :Alt stof består af bittesmå partikler kaldet atomer. Atomer er de grundlæggende byggesten i stof og er udelelige med kemiske midler.
5. Atomers uforgængelighed :Atomer kan ikke skabes eller ødelægges under kemiske reaktioner. De kan kun omarrangeres til at danne forskellige stoffer.
6. Atomernes homogenitet :Alle atomer i et givet grundstof er identiske med hensyn til deres masse, størrelse og andre grundlæggende egenskaber.
7. Forbindelsers heterogenitet :Forbindelser dannes, når atomer af forskellige grundstoffer kombineres. Atomerne i en forbindelse holdes sammen af kemiske kræfter.
Daltons atomteori revolutionerede forståelsen af stoffets natur og lagde grunden til moderne kemi.
Sidste artikelHvad er dårligt ved opløsningsmidler?
Næste artikelHvad er bindingen for C2Br4?
 Varme artikler
Varme artikler
-
 I glødende farver:At se spredningen af narkotikapartikler i et retsmedicinsk laboratoriumNIST-forskere brugte glødende pulver til at forstå, hvordan lægemiddelpartikler kan spredes på overflader i et retskemisk laboratorium. Kredit:E. Sisco, M. Staymates/NIST Da to videnskabsmænd fra
I glødende farver:At se spredningen af narkotikapartikler i et retsmedicinsk laboratoriumNIST-forskere brugte glødende pulver til at forstå, hvordan lægemiddelpartikler kan spredes på overflader i et retskemisk laboratorium. Kredit:E. Sisco, M. Staymates/NIST Da to videnskabsmænd fra -
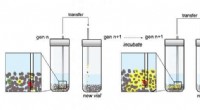 Livlig kemi skabt i laboratoriesøgning efter måder at studere livets oprindelse påForskerne udsatte deres kemiske supper for en form for selektion ved at tage en lille mængde materiale fra et hætteglas og placere det i et nyt hætteglas med frisk pyrit og kemikalier. Efter flere gen
Livlig kemi skabt i laboratoriesøgning efter måder at studere livets oprindelse påForskerne udsatte deres kemiske supper for en form for selektion ved at tage en lille mængde materiale fra et hætteglas og placere det i et nyt hætteglas med frisk pyrit og kemikalier. Efter flere gen -
 Faraday stoffer? MXene-belagt stof kan indeholde elektronisk interferens i bærbare enhederDrexel University-forskere rapporterer, at stof belagt med MXene er 99,9 % effektivt til at blokere elektromagnetisk interferens. Kredit:Drexel University Forskere ved Drexel Universitys College o
Faraday stoffer? MXene-belagt stof kan indeholde elektronisk interferens i bærbare enhederDrexel University-forskere rapporterer, at stof belagt med MXene er 99,9 % effektivt til at blokere elektromagnetisk interferens. Kredit:Drexel University Forskere ved Drexel Universitys College o -
 Yderligere to polymorfer fundet for rød-orange-gulKredit:ACS En trio af forskere ved Université de Montréal har opdaget yderligere to polymorfer for ROY, hvilket bringer det samlede antal til 10. I deres papir udgivet i Journal of the American C
Yderligere to polymorfer fundet for rød-orange-gulKredit:ACS En trio af forskere ved Université de Montréal har opdaget yderligere to polymorfer for ROY, hvilket bringer det samlede antal til 10. I deres papir udgivet i Journal of the American C
- Huawei beder retten om at smide forbud mod amerikanske telekommunikationsmidler tilbage
- NASA undersøger brugen af medicinsk-lignende værktøjer til at studere prøver af solsystemet
- Quo vadis Antarktis bundvand?
- Unik modeltagningsteknik identificerer sodforureningskilde over Kina
- Astronomer producerer det største 3D-katalog over galakser
- Forskelle mellem Abalone & Paua


