Hvad er stærkest ionisk eller kovalent?
Der er dog nogle undtagelser fra denne regel. For eksempel er nogle kovalente bindinger, såsom tredobbeltbindingen i kuldioxid, stærkere end nogle ionbindinger, såsom bindingen mellem natrium og chlorid. Dette skyldes, at styrken af en binding afhænger af en række faktorer, herunder elektronegativiteten af de involverede atomer, størrelsen af atomerne og antallet af elektroner i bindingen.
Generelt er ionbindinger stærkere end kovalente bindinger, men der er nogle undtagelser fra denne regel.
Sidste artikelHvad er forholdet mellem metallisk bindingsstyrke og fordampningsentalpi?
Næste artikelHvorfor er metaller fleksible?
 Varme artikler
Varme artikler
-
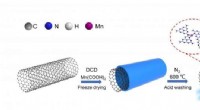 Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne
Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne -
 Flydende krystallers overraskende styrkeForskere er et skridt tættere på at udvikle længerevarende og sikrere batterier ved hjælp af flydende krystaller. Kredit:Pixabay Dendritter er de ødelæggende biprodukter af cyklussen med opladning
Flydende krystallers overraskende styrkeForskere er et skridt tættere på at udvikle længerevarende og sikrere batterier ved hjælp af flydende krystaller. Kredit:Pixabay Dendritter er de ødelæggende biprodukter af cyklussen med opladning -
 Maskinlæring til solenergi er en supercomputer dræberKredit:CC0 Public Domain Supercomputere kunne finde sig selv uden for et job takket være en række nye maskinlæringsmodeller, der producerer hurtige, nøjagtige resultater med en normal bærbar compu
Maskinlæring til solenergi er en supercomputer dræberKredit:CC0 Public Domain Supercomputere kunne finde sig selv uden for et job takket være en række nye maskinlæringsmodeller, der producerer hurtige, nøjagtige resultater med en normal bærbar compu -
 Voksende krystaller til at generere tilfældige talKredit: Stof (2020). DOI:10.1016/j.matt.2020.01.024 Et team ved University of Glasgow har udviklet en ny måde at generere tilfældige tal ved at bruge tilfældigheden i krystalvækst. I deres papir
Voksende krystaller til at generere tilfældige talKredit: Stof (2020). DOI:10.1016/j.matt.2020.01.024 Et team ved University of Glasgow har udviklet en ny måde at generere tilfældige tal ved at bruge tilfældigheden i krystalvækst. I deres papir
- Modi siger, at Indien vil sende bemandet flyvning ud i rummet i 2022
- Verdens første -- Lokaliseret levering af et lægemiddel mod kræft af fjernstyrede mikrobærere
- Billeddannelsesmetoden evaluerer cellefunktionelle ændringer og sårheling
- Hvordan Auroras virker
- Nye kirigami-inspirerede modeller forudsiger, hvordan nye metamaterialer opfører sig
- Sådan tegner man mængden af mængder efterspørgt på en Supply & Demand Graph


