Hvad er procentdelen af vand til nærmeste tiendedel i denne forbindelse BaOH2 8H2O?
Procentdel af vand =(Vandmasse / Molær masse af forbindelse) * 100
Først skal vi beregne molmassen af forbindelsen BaOH2 8H2O:
Molær masse af BaOH2 8H2O =(137,33 g/mol) + (2 * 17,01 g/mol) + (8 * 18,02 g/mol) =315,47 g/mol
Nu kan vi beregne massen af vand i forbindelsen:
Vandmasse =8 * (18,02 g/mol) =144,16 g
Endelig kan vi beregne procentdelen af vand i forbindelsen:
Procentdel vand =(144,16 g / 315,47 g) * 100 =45,7 %
Derfor er procentdelen af vand i BaOH2 8H2O til nærmeste tiendedel 45,7%.
Sidste artikelKan en eksoterm reaktion have positiv entalpi?
Næste artikelGiv testen for kuldioxid?
 Varme artikler
Varme artikler
-
 Hvad en krystal afslører om behandling af nukleare materialerOptisk mikroskopbillede af en enkelt radioaktiv mikrokrystal. Kredit:Jordan Corbey | PNNL Mens man studerede gamle forurenede jordprøver fra Plutonium Finishing Plants affaldskrybbe på Hanford Sit
Hvad en krystal afslører om behandling af nukleare materialerOptisk mikroskopbillede af en enkelt radioaktiv mikrokrystal. Kredit:Jordan Corbey | PNNL Mens man studerede gamle forurenede jordprøver fra Plutonium Finishing Plants affaldskrybbe på Hanford Sit -
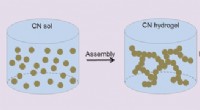 Carbonitrid aerogeler formidler den fotokatalytiske omdannelse af vandKredit:Wiley Nanokemi opfylder makrostrukturer:Kinesiske forskere rapporterer syntesen af en makroskopisk aerogel fra carbonitrid-nanomaterialer, som er en glimrende katalysator for den vandopde
Carbonitrid aerogeler formidler den fotokatalytiske omdannelse af vandKredit:Wiley Nanokemi opfylder makrostrukturer:Kinesiske forskere rapporterer syntesen af en makroskopisk aerogel fra carbonitrid-nanomaterialer, som er en glimrende katalysator for den vandopde -
 Indlejret dråbeprint-teknologi udskriver og behandler kontrollerbart dråber, der er suspenderet på…Den nye indlejrede metode til udskrivning af dråber suspenderer 3D-arrays af dråber i en unikt isoleret tilstand, der giver mulighed for præcis behandling og eksperimentering Kredit:Singapore-MIT Alli
Indlejret dråbeprint-teknologi udskriver og behandler kontrollerbart dråber, der er suspenderet på…Den nye indlejrede metode til udskrivning af dråber suspenderer 3D-arrays af dråber i en unikt isoleret tilstand, der giver mulighed for præcis behandling og eksperimentering Kredit:Singapore-MIT Alli -
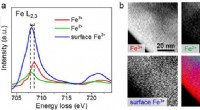 Effektiv brintomdannelse gennem solvandsopdeling ved hjælp af hæmatitmesokrystalbaserede fotoanode…Figur 1:STEM-EELS-analyse viser fordelingen af jernoxid og iltfaciliteter (Vo) i mesokrystaller. (a) EEL (Electron Energy Loss) spektre af Fe L 2, 3 ved hjælp af multivariat analyse. (b) Billede a
Effektiv brintomdannelse gennem solvandsopdeling ved hjælp af hæmatitmesokrystalbaserede fotoanode…Figur 1:STEM-EELS-analyse viser fordelingen af jernoxid og iltfaciliteter (Vo) i mesokrystaller. (a) EEL (Electron Energy Loss) spektre af Fe L 2, 3 ved hjælp af multivariat analyse. (b) Billede a
- Fremmede bortførelser:Er du i gode hænder?
- Faldende bibestande:Et naturligt fænomen eller en advarsel?
- Russisk forsøg på at kontrollere et kredsende radioteleskop mislykkes
- Oversvømmelser i Pakistan:Hvilken rolle spillede klimaændringer?
- Ultrafølsomme magnetoplasmoniske sensorer
- Global opvarmning:Flere insekter, spise flere afgrøder


