Hvad er produktet af C14H30, der brændes som brændstof og zinkmetal, der falder ned i en opløsning af kobber 2-nitrat?
2C14H30 (l) + 45O2 (g) -> 28CO2 (g) + 30H2O (g)
Når zinkmetal hældes i en opløsning af kobber(II)nitrat, opstår der en redoxreaktion. Zinkmetal oxideres og taber elektroner, mens kobber(II)ioner reduceres og får elektroner. Reaktionen kan repræsenteres som:
Zn (s) + Cu(NO3)2 (aq) -> Zn(NO3)2 (aq) + Cu (s)
I denne reaktion virker zinkmetal som et reduktionsmiddel, der donerer elektroner til kobber(II)-ioner, mens kobber(II)-ioner fungerer som et oxidationsmiddel, der accepterer elektroner fra zinkmetal.
 Varme artikler
Varme artikler
-
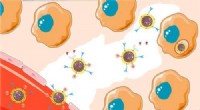 Bro over tumorvoldgrave med potente lægemiddelleveringspartiklerKredit:American Chemical Society På trods af store anstrengelser, kræft er fortsat en formidabel sygdom, med hver malign subtype, der reagerer forskelligt på terapeutika. En forhindring, der er sp
Bro over tumorvoldgrave med potente lægemiddelleveringspartiklerKredit:American Chemical Society På trods af store anstrengelser, kræft er fortsat en formidabel sygdom, med hver malign subtype, der reagerer forskelligt på terapeutika. En forhindring, der er sp -
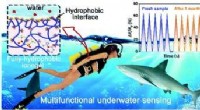 Fuldt hydrofob ionogel udviklet til bærbar undervandssensor og kommunikatorGrafisk abstrakt. Kredit:DOI:10.1039/D1MH00998B Smart Polymer Materials-gruppen ledet af professor Chen Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske
Fuldt hydrofob ionogel udviklet til bærbar undervandssensor og kommunikatorGrafisk abstrakt. Kredit:DOI:10.1039/D1MH00998B Smart Polymer Materials-gruppen ledet af professor Chen Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske -
 Syntese af UV-absorbere fra cashewnøddeskalvæskeForskere fra Mainz og Johannesburg med en prøve af udgangsmaterialet til UV-absorber fra cashewnøddeskalvæske. Kredit:Opatz Lab Forskere ved Johannes Gutenberg University Mainz (JGU) i Tyskland, i
Syntese af UV-absorbere fra cashewnøddeskalvæskeForskere fra Mainz og Johannesburg med en prøve af udgangsmaterialet til UV-absorber fra cashewnøddeskalvæske. Kredit:Opatz Lab Forskere ved Johannes Gutenberg University Mainz (JGU) i Tyskland, i -
 Enkeltelektrodemateriale strømliner funktioner til en lille chipDenne illustration viser elektrokemisk energilagring på chip integreret med tyndfilmselektronik på transistorniveau ved hjælp af et enkelt-elektrodemateriale til alle enheder. Kredit:WILEY‐VCH Verlag
Enkeltelektrodemateriale strømliner funktioner til en lille chipDenne illustration viser elektrokemisk energilagring på chip integreret med tyndfilmselektronik på transistorniveau ved hjælp af et enkelt-elektrodemateriale til alle enheder. Kredit:WILEY‐VCH Verlag
- Sådan fungerer flaskevand
- Byd på at stoppe dødbringende madlavningsmetoder, der fremmer den globale opvarmning
- Singapore Airlines lancerer verdens længste flyvning
- Forskning afslører, hvordan forurenende stoffer påvirker tidlig embryoudvikling
- Forskere udvikler farveændrende stof
- Hvordan udligning af kønsbestemte lønforskelle fordeler opgaver mere ligeligt


