Hvorfor mister natrium en elektron og opnår 1 ladning?
Grunden til at natrium mister sin yderste elektron er, at det ikke er særlig stærkt tiltrukket af kernen. Det skyldes, at den yderste elektron er langt fra kernen, og tiltrækningskraften mellem kernen og elektronen aftager, når afstanden mellem dem øges. Derudover er den yderste elektron afskærmet fra kernen af de andre elektroner i atomet. Denne afskærmningseffekt reducerer også tiltrækningskraften mellem kernen og den yderste elektron.
Som et resultat af disse faktorer holdes natriums yderste elektron svagt og kan let fjernes fra atomet. Når natrium mister denne elektron, bliver den positivt ladet, fordi den nu har en proton mere end elektron.
 Varme artikler
Varme artikler
-
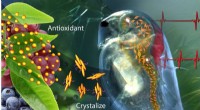 Smart antioxidantholdig polymer reagerer på kroppens kemi, miljøEt nyt lægemiddelleveringssystem, der indeholder krystalliseret catechin - en antioxidant, der findes i grøn te og frugt - kan mærke problemer og reagere ved at frigive antioxidant for at genoprette e
Smart antioxidantholdig polymer reagerer på kroppens kemi, miljøEt nyt lægemiddelleveringssystem, der indeholder krystalliseret catechin - en antioxidant, der findes i grøn te og frugt - kan mærke problemer og reagere ved at frigive antioxidant for at genoprette e -
 Forskere rapporterer højtydende solid-state natrium-ion batteriKredit:CC0 Public Domain Solid-state natrium-ion-batterier er langt sikrere end konventionelle lithium-ion-batterier, som udgør en risiko for brand og eksplosioner, men deres ydeevne har været for
Forskere rapporterer højtydende solid-state natrium-ion batteriKredit:CC0 Public Domain Solid-state natrium-ion-batterier er langt sikrere end konventionelle lithium-ion-batterier, som udgør en risiko for brand og eksplosioner, men deres ydeevne har været for -
 Opsnuse forfalskede spiritusEn bærbar enhed med en avanceret sensor kan opsnuse forfalskede spiritus. Kredit:Kenneth S. Suslick, Ph.D. Udvandet eller falsk spiritus kan høste økonomiske belønninger for ondsindede personer, m
Opsnuse forfalskede spiritusEn bærbar enhed med en avanceret sensor kan opsnuse forfalskede spiritus. Kredit:Kenneth S. Suslick, Ph.D. Udvandet eller falsk spiritus kan høste økonomiske belønninger for ondsindede personer, m -
 Strukturel model for fysiologiske tau-mikrotubuli-interaktioner kaster lys over neurologiske sygdomm…Liz Kellogg, postdoktor ved UC Berkeley, og tilknyttet Lawrence Berkeley National Laboratory, og Eva Nogales, senior fakultetsforsker i Biosciences -området ved Berkeley Lab, udførelse af cryo-EM for
Strukturel model for fysiologiske tau-mikrotubuli-interaktioner kaster lys over neurologiske sygdomm…Liz Kellogg, postdoktor ved UC Berkeley, og tilknyttet Lawrence Berkeley National Laboratory, og Eva Nogales, senior fakultetsforsker i Biosciences -området ved Berkeley Lab, udførelse af cryo-EM for
- Havniveaustigning driver spildevandslækage til kystvande
- Hvad er de tre elementer i en løftestang?
- Klimafølsomhed – reducere usikkerheden ved usikkerhed
- Forskere opfinder en måde at se attosekonde elektronbevægelser med en røntgenlaser
- I Paris, Airbnb får skylden for alle former for dårligdomme
- Er ruststøv skadeligt?


