Hvordan laver man 1,0M saltsyre ud fra koncentreret syre?
Materialer:
- Koncentreret saltsyre (HCl)
- Deioniseret vand
- Sikkerhedsbriller
- Laboratoriefrakke eller forklæde
- Handsker
- Gradueret cylinder eller bæger
- Rørestav
Procedure:
1. Sikkerhed først:
- Bær sikkerhedsbriller, laboratoriefrakke eller forklæde og handsker for at beskytte dig mod stænk og dampe.
- Arbejd i et godt ventileret område.
2. Beregn den nødvendige mængde koncentreret HCl:
- Bestem den nødvendige mængde koncentreret HCl ved hjælp af fortyndingsformlen:
$$C_1 V_1 =C_2 V_2$$
hvor:
- $$C_1$$ er koncentrationen af koncentreret HCl (normalt 11,6 M)
- $$V_1$$ er mængden af koncentreret HCl, du skal tage
- $$C_2$$ er den ønskede koncentration (1,0 M)
- $$V_2$$ er det endelige volumen af den fortyndede opløsning
3. Forbered fortyndingsopløsningen:
- Brug en målecylinder eller et bægerglas til at måle det beregnede volumen af koncentreret HCl.
- Tilsæt langsomt den koncentrerede HCl til en lille mængde deioniseret vand i et bægerglas, under konstant omrøring. Denne indledende fortynding hjælper med at forhindre sprøjt og overdreven varmeudvikling.
4. Tilføj mere vand for at nå det endelige volumen:
- Overfør den fortyndede HCl fra bægerglasset til en målekolbe.
- Skyl bægerglasset med en lille mængde deioniseret vand, og tilsæt skyllevandet til målekolben.
- Tilsæt deioniseret vand til målekolben, indtil opløsningen når 1,0 L-mærket (eller den mængde, du ønsker).
- Bland grundigt ved at dreje kolben forsigtigt for at sikre ensartet koncentration i hele opløsningen.
Mærkning:
- Mærk målekolben tydeligt med angivelse af, at den indeholder 1,0 M saltsyre, og datoen for fremstillingen.
Bemærk:
- Tilsæt altid syre til vand, ikke omvendt. Tilsætning af vand direkte til koncentreret syre kan forårsage kraftig kogning, sprøjt og endda frigive skadelige dampe.
Husk at følge sikker laboratoriepraksis og håndtere koncentrerede syrer med største omhu.
Sidste artikelHvad er tætheden af grafenoxid eller ghraphen?
Næste artikelEr smeltning af is i en limonade en kemisk forandring?
 Varme artikler
Varme artikler
-
 Indtageligt medicinsk udstyr kan brydes ned med lysLet nedbrydelige hydrogeler som dynamiske triggere i GI-enheder. (A) Skematisk af ballonindsættelse og inflation (venstre), nedbrydning via enten en endoskopisk eller usammenhængende LED lyskilde (mid
Indtageligt medicinsk udstyr kan brydes ned med lysLet nedbrydelige hydrogeler som dynamiske triggere i GI-enheder. (A) Skematisk af ballonindsættelse og inflation (venstre), nedbrydning via enten en endoskopisk eller usammenhængende LED lyskilde (mid -
 Keramiske honningkage luftfiltre kan reducere byforureningPrototype luftfiltreringsstationer placeret i Paris, Frankrig, hjalp med at holde niveauet af partikler under tærsklerne fra Verdenssundhedsorganisationen. Kredit:Forureningsbegivenhed i Paris af Tang
Keramiske honningkage luftfiltre kan reducere byforureningPrototype luftfiltreringsstationer placeret i Paris, Frankrig, hjalp med at holde niveauet af partikler under tærsklerne fra Verdenssundhedsorganisationen. Kredit:Forureningsbegivenhed i Paris af Tang -
 ArtSea Ink:en farverig, tangbaseret blæk til 3D-printGlimmerpulver blev spredt i alginatopløsninger for at gøre levende, perlemorsfarvede blæk til 3D-print. Kredit:Tilpasset fra ACS Omega Nogle kunstnere omfavner 3D-print som et nyt medie, giver dem
ArtSea Ink:en farverig, tangbaseret blæk til 3D-printGlimmerpulver blev spredt i alginatopløsninger for at gøre levende, perlemorsfarvede blæk til 3D-print. Kredit:Tilpasset fra ACS Omega Nogle kunstnere omfavner 3D-print som et nyt medie, giver dem -
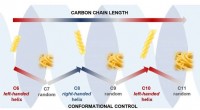 Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University
Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University
- At træffe den bedste beslutning:Matematik viser, at forskellige tænkere har lige bedre resultater
- Falsk eller ægte? Ny undersøgelse finder, at forbrugere er på vagt over for manipulerede billeder
- Hvad er lavet af mellet?
- Hurtig ødelæggelse af jordlignende atmosfærer af unge stjerner
- Sådan formater du en MOV til Overspændingsbeskyttelse
- NASA vurderer kraftige orkanen Teddys ekstreme nedbør


