Hvad giver pH og poh op til ved 25 grader c?
En opløsnings pH er defineret som den negative logaritme af hydrogenionkoncentrationen, mens pOH defineres som den negative logaritme af hydroxidionkoncentrationen. Forholdet mellem pH og pOH kan udtrykkes som følger:
$$pH + pOH =14$$
Denne ligning gælder ved alle temperaturer, men værdierne af pH og pOH, der svarer til neutralpunktet, vil variere afhængigt af temperaturen. Ved 25 grader Celsius har neutralpunktet en pH på 7 og en pOH på 7.
At kende forholdet mellem pH og pOH kan være nyttigt til at forstå surheden eller basiciteten af en opløsning og til at udføre beregninger, der involverer hydrogenion- og hydroxidionkoncentrationer.
Sidste artikelHvad er størrelsen af et toksin?
Næste artikelHvad er opløseligheden af urinstof i vand ved 25 grader Celsius?
 Varme artikler
Varme artikler
-
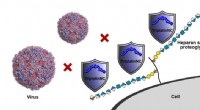 Metalbaserede forbindelser baner vejen for nye antivirale behandlingerTriplatinNC, repræsenteret i blåt, binder sig til celleoverfladereceptorer for at beskytte celler mod virusinfektion (her to enterovirus 71 partikler, repræsenteret til venstre). Kredit:Benjamin Baill
Metalbaserede forbindelser baner vejen for nye antivirale behandlingerTriplatinNC, repræsenteret i blåt, binder sig til celleoverfladereceptorer for at beskytte celler mod virusinfektion (her to enterovirus 71 partikler, repræsenteret til venstre). Kredit:Benjamin Baill -
 Ny algoritme forudsiger optimale materialer blandt alle mulige forbindelserResultaterne af en Mendelevian-søgning efter hårde og superhårde materialer Kredit:Zahed Allahyari og Artem R. Oganov / NPJ Computational Materials Skoltech-forskere har tilbudt en løsning på prob
Ny algoritme forudsiger optimale materialer blandt alle mulige forbindelserResultaterne af en Mendelevian-søgning efter hårde og superhårde materialer Kredit:Zahed Allahyari og Artem R. Oganov / NPJ Computational Materials Skoltech-forskere har tilbudt en løsning på prob -
 Forskere forenkler små strukturer konstruktion dryp for drypDer vises tre laboratorieprøver i faldende størrelse. Ringene blev hærdet i en centrifuge ved hjælp af acceleration til at kontrollere længdeskalaen af dråbestrukturer, som kan bruges til at oprette
Forskere forenkler små strukturer konstruktion dryp for drypDer vises tre laboratorieprøver i faldende størrelse. Ringene blev hærdet i en centrifuge ved hjælp af acceleration til at kontrollere længdeskalaen af dråbestrukturer, som kan bruges til at oprette -
 Forskere ved ESS, Svensk vandforskning, ORNL bruger VISION til at se på almindelige forurenende sto…Brug af neutronspredning, Monika Hartl fra European Spallation Source studerer, hvordan vandfiltre interagerer med forurenende stoffer for at optimere filterdesign og forbedre vandbehandlingsmetoder.
Forskere ved ESS, Svensk vandforskning, ORNL bruger VISION til at se på almindelige forurenende sto…Brug af neutronspredning, Monika Hartl fra European Spallation Source studerer, hvordan vandfiltre interagerer med forurenende stoffer for at optimere filterdesign og forbedre vandbehandlingsmetoder.
- Forståelse af ændringer i ekstrem nedbør
- Inflation af onlinevurderinger kan være gavnlig og skadelig
- Med laserlys, forskere laver første røntgenholografiske billeder af vira
- Milepæl for næste generation af solid-state batterier til at drive fremtidige langdistance elektri…
- Hvad er en forhistorisk værktøjskasse, og hvordan kan den omskrive menneskets historie?
- Total solformørkelse 21. august kl.


