Hvordan måler man hastigheden af en kemisk reaktion?
1. Koncentrationsændring over tid:En måde at måle reaktionshastigheden på er at overvåge ændringen i koncentrationen af reaktanterne eller produkterne over tid. Dette kan gøres ved hjælp af forskellige analytiske teknikker såsom spektroskopi (f.eks. UV-Vis spektroskopi), kromatografi eller titrering.
2. Gasudvikling:Hvis en reaktion producerer en gas, kan reaktionshastigheden måles ved at måle mængden af gas produceret over tid. Denne metode er almindeligt anvendt i reaktioner, der involverer produktion af gasser såsom kuldioxid eller brint.
3. Kalorimetri:Denne teknik måler den varme, der absorberes eller frigives under en reaktion. For eksoterme reaktioner (hvor varme frigives) kan reaktionshastigheden bestemmes ved at overvåge temperaturændringen over tid.
4. Elektrisk ledningsevne:I visse reaktioner, der involverer ioner, kan ændringer i elektrisk ledningsevne indikere reaktionshastigheden. Dette skyldes, at koncentrationen af ioner i opløsningen ændres, efterhånden som reaktionen skrider frem, hvilket påvirker den elektriske ledningsevne.
5. Radioaktivt henfald:Hvis reaktionen involverer radioaktive stoffer, kan henfaldshastigheden bruges til at bestemme reaktionshastigheden. Denne metode er især nyttig i reaktioner, hvor halveringstiden for det radioaktive stof er kendt.
6. Spektrofotometri:Denne teknik måler ændringerne i absorbans eller transmittans af lys, efterhånden som reaktionen skrider frem. Det bruges almindeligvis i reaktioner, hvor en af reaktanterne eller produkterne har en tydelig farve eller absorberer lys ved en bestemt bølgelængde.
7. Elektrokemiske metoder:Elektrokemiske teknikker som amperometri eller potentiometri kan bruges til at overvåge ændringen i elektrisk strøm eller potentiale under en reaktion, hvilket gør det muligt at bestemme reaktionshastigheden.
8. pH-ændring:I reaktioner, der involverer syre-base-interaktioner eller producerer/forbruger hydrogenioner (H+), kan reaktionshastigheden overvåges ved at måle ændringen i pH.
Det er vigtigt at bemærke, at valget af metode afhænger af den specifikke reaktion og arten af de involverede reaktanter og produkter. Derudover kan de eksperimentelle betingelser (f.eks. temperatur, tryk, koncentration) også påvirke reaktionshastigheden og bør kontrolleres omhyggeligt.
Sidste artikelHvad er produktet af Zn plus HCl?
Næste artikelHvad sker der med volumen, hvis antallet af mol gas falder?
 Varme artikler
Varme artikler
-
 Vurdering af virkningen af tabsmekanismer i solcellekandidat antimonsulfidselenidKredit:Pixabay/CC0 Public Domain Mens klimaændringer fortsætter med at præsentere sig selv som den mest presserende trussel, vores planet står over for, presser forskere på for at finde effektive o
Vurdering af virkningen af tabsmekanismer i solcellekandidat antimonsulfidselenidKredit:Pixabay/CC0 Public Domain Mens klimaændringer fortsætter med at præsentere sig selv som den mest presserende trussel, vores planet står over for, presser forskere på for at finde effektive o -
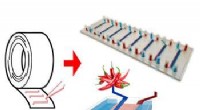 Ved hjælp af almindelig tape, forskere laver chip, der kan fremskynde udviklingen af lægemidlerEt forenklet skema af det tape-baserede barriere-on-a-chip system. Kredit:KTH Kgl. Teknologisk Institut Med almindelig dobbeltklæbende tape, forskere i Sverige samlede en chip-baseret model af en
Ved hjælp af almindelig tape, forskere laver chip, der kan fremskynde udviklingen af lægemidlerEt forenklet skema af det tape-baserede barriere-on-a-chip system. Kredit:KTH Kgl. Teknologisk Institut Med almindelig dobbeltklæbende tape, forskere i Sverige samlede en chip-baseret model af en -
 Hvordan kommer kalium ind i cellerne?Udadgående og indadgående åbningsstrukturer af KdpFABC i cellemembranen. Kredit:Inga Hänelt forskningsgruppe. Kredit:Goethe-Universität Frankfurt am Main I årtier, man antog, at proteinkanaler og
Hvordan kommer kalium ind i cellerne?Udadgående og indadgående åbningsstrukturer af KdpFABC i cellemembranen. Kredit:Inga Hänelt forskningsgruppe. Kredit:Goethe-Universität Frankfurt am Main I årtier, man antog, at proteinkanaler og -
 Langvarig og præcis dosering af medicin takket være en olie-hydrogelblandingProfessor Job Boekhoven og Caren Wanzke ved det tekniske universitet i München opdagede et nyt materialesystem, der kan frigive lægemidler med en konstant frigivelseshastighed over en afstemmelig peri
Langvarig og præcis dosering af medicin takket være en olie-hydrogelblandingProfessor Job Boekhoven og Caren Wanzke ved det tekniske universitet i München opdagede et nyt materialesystem, der kan frigive lægemidler med en konstant frigivelseshastighed over en afstemmelig peri
- Sjældne sygdomme i bronzealderen
- Kvantemagnetometre opdager de mindste materialefejl på et tidligt tidspunkt
- Et fjerde tørt år sandsynligvis i Californien, siger embedsmænd
- Kemisk krigsførelse på revet:Hvordan visse tangarter skader koraller
- Sådan repareres naturen og undgå menneskelig elendighed:FN-rapport
- Hvad er betingelserne, når man tilføjer grus til is, og det virker?


