Hvad sker der, når opløsninger af natriumcarbonat og saltsyre blandes?
Na2CO3(aq) + 2HCl(aq) → 2NaCl(aq) + H2O(l) + CO2(g)
Her er en beskrivelse af, hvad der sker under reaktionen:
1. Danning af natriumchlorid (NaCl) :
- Natriumionerne (Na+) fra natriumcarbonat og chloridionerne (Cl-) fra saltsyre kombineres og danner natriumchlorid (NaCl).
- Natriumchlorid er en opløselig forbindelse og dissocierer til sine ioner i den vandige opløsning.
2. Udgivelse af vand (H2O) :
- Reaktionen giver også vand (H2O) som et af produkterne.
- Hydrogenionerne (H+) fra saltsyre og carbonationerne (CO3^2-) fra natriumcarbonat reagerer og danner vandmolekyler.
3. Udvikling af kuldioxid (CO2) :
- Reaktionen fører til dannelse af kuldioxidgas (CO2) som et biprodukt.
- Kuldioxid er en farveløs og lugtfri gas, der slipper ud af opløsningen og forårsager opbrusning og bobler.
4. pH-ændringer:
- I starten er opløsningen af natriumcarbonat basisk på grund af tilstedeværelsen af carbonationer.
- Når saltsyre tilsættes, reagerer hydrogenionerne (H+) med carbonationerne, hvilket får opløsningen til at blive sur.
- Opløsningens pH vil afhænge af de relative mængder af natriumcarbonat og saltsyre, der anvendes.
5. Saltdannelse:
- I sidste ende resulterer reaktionen i dannelsen af natriumchlorid (NaCl), som er et neutralt salt.
Reaktionen mellem natriumcarbonat og saltsyre er et klassisk eksempel på en syre-base reaktion, hvor en syre (HCl) reagerer med en base (Na2CO3) for at danne et salt (NaCl) og vand. Denne type reaktion er almindeligt forekommende i kemi og har forskellige anvendelser, herunder i produktion af salte, neutralisering af syrer eller baser, og i industrielle processer.
 Varme artikler
Varme artikler
-
 Sniffing ud af hvilke plantebaserede burgere der lugter mest af ægte oksekødKredit:CC0 Public Domain For mange kødspisere, sommergriller ville ikke være det samme uden den læskende aroma af burgere, der tilberedes på grillen. Men mange mennesker er nu åbne for at prøve pl
Sniffing ud af hvilke plantebaserede burgere der lugter mest af ægte oksekødKredit:CC0 Public Domain For mange kødspisere, sommergriller ville ikke være det samme uden den læskende aroma af burgere, der tilberedes på grillen. Men mange mennesker er nu åbne for at prøve pl -
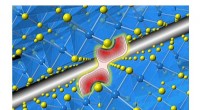 Præcisionseksperimenter afslører huller i van der Waals teoriKredit:University of Tsukuba Opdagelsen af grafen, med sit høje styrke-til-vægt-forhold, fleksibilitet, elektrisk ledningsevne, og evnen til at danne en uigennemtrængelig barriere, førte til en
Præcisionseksperimenter afslører huller i van der Waals teoriKredit:University of Tsukuba Opdagelsen af grafen, med sit høje styrke-til-vægt-forhold, fleksibilitet, elektrisk ledningsevne, og evnen til at danne en uigennemtrængelig barriere, førte til en -
 En motorvej for elektroner i oxidheterostrukturerFigur illustrerer vigtigheden af stærk (elektronisk) screening ved bestemmelse af elektronmobiliteten ved grænseflader af oxidheterostrukturer. Den betydelige forbedring af elektronmobilitet kan mul
En motorvej for elektroner i oxidheterostrukturerFigur illustrerer vigtigheden af stærk (elektronisk) screening ved bestemmelse af elektronmobiliteten ved grænseflader af oxidheterostrukturer. Den betydelige forbedring af elektronmobilitet kan mul -
 Vandledninger kan spille en større rolle i cellulær funktionKredit:CC0 Public Domain Hver af vores celler er omgivet af en kompleks membran, der fungerer som en biologisk grænse, lade ioner og næringsstoffer som salt, kalium og sukker ind og ud. Beskyttern
Vandledninger kan spille en større rolle i cellulær funktionKredit:CC0 Public Domain Hver af vores celler er omgivet af en kompleks membran, der fungerer som en biologisk grænse, lade ioner og næringsstoffer som salt, kalium og sukker ind og ud. Beskyttern
- Kvantekoaksialkabel:Enhed beviser solcellepotentiale for uorganiske nanotrådarrays med høj båndga…
- Oversvømmelser dræber ni i det sydlige Thailand
- Kontinentale piruetter:Supervulkan, der blev fodret fra jordens kappe, fik skorpe -plader til at rot…
- Engineering team udvikler strålingsresistente computere, der er i stand til højtydende computere i…
- Natur Ph.D. undersøgelse sætter fokus på mental sundhed, chikane og studiegæld
- Kan vi se kvantekorrelationer på makroskopisk skala?


